Druhý zákon termodynamiky, rovnice, príklady

- 2673
- 272
- Blažej Hrmo
Ten Druhý zákon termodynamiky má niekoľko foriem prejavu. Jeden z nich uvádza, že žiadny tepelný stroj nie je schopný úplne premeniť všetku energiu, ktorú absorbuje na použiteľnú prácu (formulácia Kelvin-Planck). Ďalším spôsobom, ako uviesť, je povedať, že skutočné procesy sa vyskytujú v takom zmysle, že kvalita energie je nižšia, pretože Entropia Má tendenciu sa zvyšovať.
Tento zákon, známy tiež ako druhý princíp termodynamiky, bol vyjadrený rôznymi spôsobmi s časom, od začiatku 19. storočia po súčasnosť, hoci jeho pôvod pochádza z vytvorenia prvých parných strojov v Anglicku, Na začiatku 18. storočia.
 postava 1. Pri výstavbe stavebných blokov na podlahu by bolo veľmi prekvapujúce, keby ste si objednali. Zdroj: Pixabay.
postava 1. Pri výstavbe stavebných blokov na podlahu by bolo veľmi prekvapujúce, keby ste si objednali. Zdroj: Pixabay. Ale aj keď sa to vyjadruje mnohými spôsobmi, vo všetkých myšlienkach, že záležitosť má tendenciu poruchy a že žiadny proces 100%, pretože straty budú vždy existovať vždy.
Všetky termodynamické systémy dodržiavajú tento princíp, počnúc samotným vesmírom až po šálku rannej kávy, ktorá ticho čakajú na stole výmeny tepla s prostredím.
Káva, ako plynie čas, ochladí, až kým nebude v tepelnej rovnováhe s prostredím, takže by bolo veľmi prekvapujúce, keby sa jedného dňa vyskytol opak a atmosféra by sa ochladila, zatiaľ čo sa káva zohrieva pre seba. Je nepravdepodobné, že sa to stane, niektorí povedia, že je to nemožné, ale stačí si predstaviť, že bude mať predstavu o zmysle, v ktorom sa veci dejú spontánne.
V inom príklade, ak posunieme knihu na povrch stola, nakoniec sa zastaví, pretože jej kinetická energia sa stratí vo forme tepla v dôsledku trenia.
Prvý a druhý zákon termodynamiky bol zriadený okolo roku 1850, vďaka vedcom, ako je Lord Kelvin -tvorca pojmu „termodynamika“ -, William Rankine -Auttor prvého formálneho textu termodynamiky -a Rudolf Clausius Clausius.
[TOC]
Vzorce a rovnice
Entropia -bez začiatku -Helps nás vytvára zmysel, v ktorom sa veci dejú. Vráťme sa k príkladu telies v tepelnom kontakte.
Keď sa do kontaktu spoja dva objekty pri rôznych teplotách a nakoniec po chvíli dosiahnu tepelnú rovnováhu, sú k ne.
Označovanie entropie ako Siež, Zmena v entropii ΔS systému je daný:

Zmena entropie ΔS Označuje stupeň poruchy v systéme, ale v používaní tejto rovnice existuje obmedzenie: je použiteľná iba na reverzibilné procesy, tj tie, v ktorých sa systém môže vrátiť do svojho pôvodného stavu bez toho, aby zanechal známku toho Stalo-.
V nezvratných procesoch sa druhý termodynamický zákon prejavuje nasledovne:
Môže vám slúžiť: Reynoldsovo číslo: Na čo je to, ako sa vypočíta, cvičenia
Reverzibilné a nezvratné procesy
Kávová šálka sa vždy ochladí a je dobrým príkladom nezvratného procesu, pretože sa vždy vyskytuje v jednom smere. Ak sa do kávy pridá krém a premiešajte, získa sa veľmi príjemná kombinácia, ale bez ohľadu na to, ako sa znova miešajú, káva a smotana už nebudú, pretože miešanie je nezvratné.
 Obrázok 2. Rozbitie pohárov je nezvratný proces. Zdroj: Pixabay.
Obrázok 2. Rozbitie pohárov je nezvratný proces. Zdroj: Pixabay. Aj keď väčšina denných procesov je nezvratná, niektoré sú takmer Zvrátený. Reverzibilita je idealizácia. Aby bol systém vykonaný, musí sa systém meniť veľmi pomaly, takže v každom bode je vždy v rovnováhe. Týmto spôsobom je možné ho vrátiť do predchádzajúceho stavu bez toho, aby ste nechali známku okolo.
Procesy, ktoré sú dosť blízko k tomuto ideálu, sú efektívnejšie, pretože dodávajú väčšie množstvo práce s menšou spotrebou energie.
Trecia sila je zodpovedná za veľkú nezvratnosť, pretože teplo generované nie je požadovaný typ energie. V knihe, ktorá sa posúva cez stôl.
Aj keď sa kniha vráti na svoju pôvodnú pozíciu, tabuľka bude horúca ako stopa príchodu a pokračovania v nej.
Teraz pozorujte žiarovku: Väčšina práce vykonanej prúdom, ktorý prechádza cez vlákno, je zbytočná v horúčave Joule Effect. Na vyžarovanie svetla sa používa iba malé percento. V obidvoch procesoch (kniha a žiarovka) sa entropia systému zvýšila.
Žiadosti
Ideálny motor je ten, ktorý je postavený prostredníctvom reverzibilných procesov a chýba mu trenie, ktoré spôsobujú odpad z energie, otáčanie takmer Všetka tepelná energia v použiteľnej práci.
Slovo zdôrazňujeme takmer, pretože ani ideálny motor, ktorým je Carnot's, má 100% účinnosť. Druhý zákon termodynamiky nie je týmto spôsobom.
Karnot
Carnot's Engine je najefektívnejší motor, ktorý možno navrhnúť. Pracuje medzi dvoma teplotnými ložiskami v dvoch izotermálnych procesoch - pri konštantnej teplote - a dvoma adiabatickými procesmi - bez prenosu tepelnej energie-.
Grafy nazývané PV -tlače diagramy - objem - objasnite situáciu:
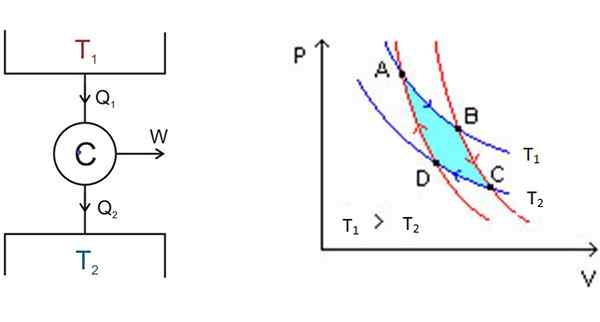 Obrázok 3. Vľavo schéma motorov Carnot a vpravo diagram P-V. Zdroj: Wikimedia Commons.
Obrázok 3. Vľavo schéma motorov Carnot a vpravo diagram P-V. Zdroj: Wikimedia Commons. Vľavo, na obrázku 3 je motorická schéma Carnot C, ktorá sa tepla q1 ložiska pri teplote t1, previesť toto teplo na prácu w a dajte odpadu2 na najchladnejšie ložisko, ktoré je pri teplote t2.
Počnúc od A, systém sa rozširuje, až kým nedosiahne B, absorbuje teplo na pevnú teplotu t1. V B, systém začína adiabatickú expanziu, v ktorej sa teplo nevyhralo ani nestratilo, aby sa dostal na C.
V C začína ďalší izotermický proces: dať teplo ďalšiemu chladnejšiemu tepelnému ložisku, ktorý je na T2. Keď sa to stane, systém je stlačený a bod D sa dosiahne. Tam začína druhý adiabatický proces, ktorý sa vráti do východiskového bodu. Týmto spôsobom je cyklus dokončený.
Môže vám slúžiť: prenos tepla jazdou (s príkladmi)Účinnosť spoločnosti Carnot závisí od teploty v Kelvin od dvoch tepelných ložísk:
Maximálna účinnosť = (qvstup - OtázkaVÝCHOD) /Qvstup = 1 - (t2/T1)
Carnotova veta uvádza, že je to najúčinnejší tepelný stroj, ale neponáhľajte sa ju kúpiť. Pamätáte si, čo sme povedali o reverzibilite procesov? Musia sa stať veľmi, veľmi pomaly, takže výstupný výkon tohto stroja je prakticky nulová.
Ľudský metabolizmus
Ľudské bytosti potrebujú energiu, aby udržali všetky svoje systémy fungovanie, a preto sa správajú ako tepelné stroje, ktoré prijímajú energiu a transformujú ju na mechanickú energiu, napríklad na pohyby.
Účinnosť a ľudského tela, keď vykonávate prácu.
Ako priemerná sila Pm Je to práca vykonaná v časovom intervale Δt, Dá sa vyjadriť ako:
Pm = W/Δt
Jo ΔU/ΔT Je to miera, ku ktorej sa energia pridáva, zostáva účinnosť tela:

Prostredníctvom mnohých testov s dobrovoľníkmi sa získala efektívnosť až 17%, čo dodáva asi 100 wattov energie na niekoľko hodín.
Samozrejme to bude do značnej miery závisieť od vykonanej úlohy. Pedalovanie bicykla má o niečo väčšiu účinnosť, približne 19 %, zatiaľ čo opakujúce sa úlohy, ktoré zahŕňajú čepele, vrcholy a motyky, majú účinnosť tak nízku ako približne 3 %.
Príklady
Druhý termodynamický zákon je implicitný vo všetkých procesoch, ktoré sa vyskytujú vo vesmíre. Entropia vždy rastie, aj keď v niektorých systémoch sa zdá, že klesá. Aby sa to zvýšilo inde, takže v celkovej rovnováhe je pozitívna.
- Pri učení sa tam entropia. Existujú ľudia, ktorí sa veci učia dobre a rýchlo, okrem toho, že si ich môžete ľahko zapamätať. Hovorí sa, že sú to ľudia s nízkym učením entropie, ale sú určite menej početné ako ľudia s vysokou entropiou: tí, ktorí si najviac pamätajú veci, ktoré študujú.
- Spoločnosť s dezorganizovanými pracovníkmi má viac entropie ako spoločnosť, v ktorej pracovníci vykonávajú riadne úlohy. Je zrejmé, že posledne menovaný bude efektívnejší ako prvý.
- Trečné sily vytvárajú menšiu účinnosť vo fungovaní strojov, pretože zvyšujú množstvo rozptýlenej energie, ktorú nemožno efektívne používať.
- Spustenie kocky má väčšiu entropiu ako hodenie mince do vzduchu. Koniec koncov, spustenie meny má iba 2 možné výsledky, zatiaľ čo spustenie kocky je 6. Čím viac udalostí je pravdepodobné, tým viac entropie existuje.
Môže vám slúžiť: Aké sú prvky pohybu?Vyriešené cvičenia
Cvičenie 1
Valec s piestom je naplnený zmesou kvapaliny a vodnej pary pri 300 K a 750 kJ tepla sa prenáša do konštantného tlakového procesu. Výsledkom je, že kvapalina vo vnútri valca sa odparuje. Vypočítajte zmenu entropie v procese.
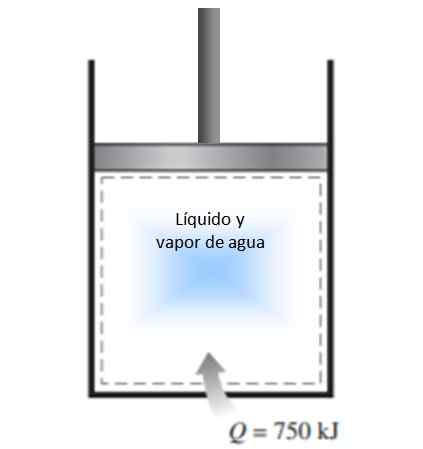 Obrázok 4. Obrázok pre príklad vyriešený 1. Zdroj: f. Zapata.
Obrázok 4. Obrázok pre príklad vyriešený 1. Zdroj: f. Zapata. Riešenie
Proces opísaný vo vyhlásení sa vykonáva pri konštantnom tlaku v uzavretom systéme, ktorý nezažije hromadnú výmenu.
Pretože ide o odparovanie, počas ktorej sa teplota nemení (počas fázových zmien je teplota konštantná), je možné použiť definíciu zmeny entropie uvedenej vyššie a teplota môže vynechať integrál:

ΔS = 750.000 j / 300 k = 2500 j / k.
Pretože systém prichádza do systému, zmena entropie je pozitívna.
Cvičenie 2
Plyn trpí zvýšením tlaku o 2.00 až 6.00 Atmosféra (ATM), udržiavanie konštantného objemu 1.00 m3, a potom sa rozbaliť pri konštantnom tlaku, až kým nedosiahne objem 3.00 m3. Nakoniec sa vráťte do svojho pôvodného stavu. Vypočítajte, koľko práce sa vykonáva v 1 cykle.
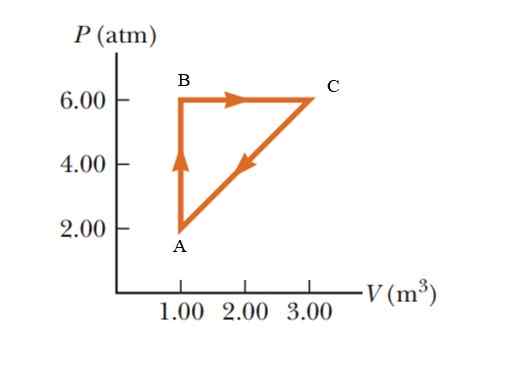 Obrázok 5. Termodynamický proces v plyne napríklad príklad 2. Zdroj: Serway -Vulle. Základy fyziky.
Obrázok 5. Termodynamický proces v plyne napríklad príklad 2. Zdroj: Serway -Vulle. Základy fyziky. Riešenie
Je to cyklický proces, v ktorom je vnútorná variácia energie neplatná, podľa prvého zákona termodynamiky, preto Q = w. V diagrame p -V (tlak - objem) je práca vykonaná počas cyklického procesu rovnocenná s oblasťou zamknutou krivkou. Na poskytnutie výsledkov v medzinárodnom systéme je potrebné zmeniť jednotky v tlaku prostredníctvom nasledujúceho konverzného faktora:
1 bankomat = 101.325 kPa = 101.325 PA.
Oblasť uzavretá grafom zodpovedá ploche trojuholníka, ktorého základňa (3 - 1 m3) = 2 m3 a ktorej výška je (6 - 2 atm) = 4 atm = 405.300 PA
WABCA = ½ (2 m3 x 405300 PA) = 405300 J = 405.3 kJ.
Cvičenie 3
Hovorí sa, že jedným z najúčinnejších strojov, ktoré boli postavené, je parná turbína poháňaná uhlím na rieke Ohio, ktorá sa používa na riadenie elektrického generátora pracujúceho medzi 1870 a 430 ° C.
Vypočítajte: a) maximálna teoretická účinnosť, b) mechanický výkon dodávaný strojom, ak je absorbovaný 1.40 x 105 J energie každú sekundu z horúcej nádrže. Je známe, že skutočná účinnosť je 42.0%.
Riešenie
a) Maximálna účinnosť sa vypočíta s vyššie uvedenou rovnicou:
Maximálna účinnosť = (qvstup - Otázka VÝCHOD) /Qvstup = 1 - (t2/T1)
Aby ste prešli Celzia do Kelvinu, stačí pridať 273.15 pri teplote Celzia:
Vynásobenie 100% máte maximálnu percentuálnu účinnosť, čo je 67.2%
c) Ak je skutočná účinnosť 42%, existuje maximálna účinnosť 0.42.
Dodávaný mechanický výkon je: p = 0.42 x 1.40 x10 5 J/s = 58800 w.
Odkazy
- Bauer, w. 2011. Fyzika pre inžinierstvo a vedy. Zväzok 1. MC Graw Hill.
- Cengel a. 2012. Termodynamika. 7mamička Vydanie. McGraw Hill.
- Figueroa, D. (2005). Séria: Fyzika pre vedu a inžinierstvo. Zväzok 4. Tekutiny a termodynamika. Editoval Douglas Figueroa (USB).
- Rytier, r. 2017. Fyzika pre vedcov a inžinierstvo: Strategický prístup.
- López, C. Prvý zákon termodynamiky. Získané z: CulturacieCientificA.com.
- Serway, r. 2011. Základy fyziky. 9nat Učenie sa.
- Univerzita. Tepelné stroje. Získané z: Laplace.my.je


=0.672)