Pravidlo Markovnikov
- 4567
- 731
- JUDr. Rudolf Čapkovič
Čo je to pravidlo Markovnikov?
Ten Pravidlo Markovnikov Je to empirické pravidlo, formulované v roku 1869 ruským chemikom Vladimírom Markovnikovom, ktorý sa používa na predpovedanie regioselektivity produktov elektrofilného pridávania. Dokonca aj dnes je stále v platnosti a odhaľuje jeho jednoduchosť v tom, ako prichádza mechanizmus niekoľkých organických reakcií.
Toto pravidlo sa vzťahuje najmä na alkény v ich hydrohalogenačných reakciách. Umožňuje teda predpovedať, aké budú väčšinové výrobky, keď alkény a alkynes reagujú s HX (HF, HCL, HBR a HI).
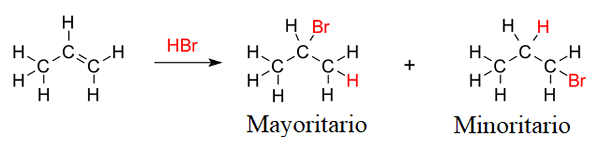 Ocenenie Markovnikovovho vlády pri hydrohalogenácie propeno. Zdroj: V8rik, CC BY-SA 3.0, cez Wikimedia Commons
Ocenenie Markovnikovovho vlády pri hydrohalogenácie propeno. Zdroj: V8rik, CC BY-SA 3.0, cez Wikimedia Commons Predpokladajme napríklad hydrobromáciu propeno alebo propylénu (vynikajúci obraz). Markovnikovovo pravidlo predpovedá, že väčšinovým produktom bude výrobok, v ktorom bude atóm brómy spojený s uhlíkom centra; Zatiaľ čo v menšom produkte, bróm končí až do uhlíka s dvojitou väzbou.
Všimnite si, že väčšina produktu má atóm vodíka spojený s koncovým uhlíkom. Tento posledný bod je najjednoduchší na zapamätanie si: vodík HX ide do uhlíka dvojitej väzby, ktorá má viac väzieb vodíka alebo C-H.
Zásady Pravidlo Markovnikov
Elektrofilné prírastky
Na dvojité väzby alkénov alebo alkínov. HX má zlý atóm elektrónov, ktorý je H, a atóm bohatý na elektróny, čo je x.
Preto môže byť HX reprezentovaný ako HΔ+-XΔ-, Byť regiónom HΔ+ Citlivý na prijímanie elektrónov v tomto prípade dvojité spojenie alkénu, ktorý sa uskutočnil elektrofylický útok (pozri obrázok nižšie).
Môže vám slúžiť: kyselina fenylactová: štruktúra, vlastnosti, použitia, efektyStabilita
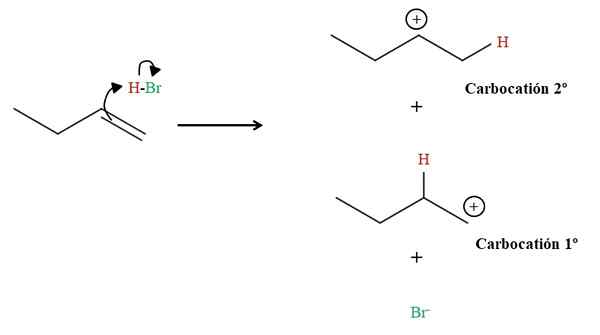
 Tvorba dvoch karbocacií v skrytej 1-buténe. Zdroj: Gabriel Bolívar cez Molview.
Tvorba dvoch karbocacií v skrytej 1-buténe. Zdroj: Gabriel Bolívar cez Molview. Ako je uvedené vyššie, 1-buténový dvojitý väzb napadne vodík HBO. Pritom elektróny väzby H-Bld „otvorené“ smerom k atómu Bromínu, ktoré tvoria karbonáž a anión BR-. Existuje však možnosť vytvorenia dvoch karbocacií: jedna primárna (1.) a druhá sekundárna (2.).
Každá karbocation je sprostredkovateľská zlúčenina, z ktorej bude konečný produkt odvodený. Ak existujú dve karbocations, potom budeme mať dva produkty: 2-Bromobutano a 1-Bromobutano. Br- Pôsobí ako nukleofil, ktorý útočí na jednu z dvoch karbocacií:
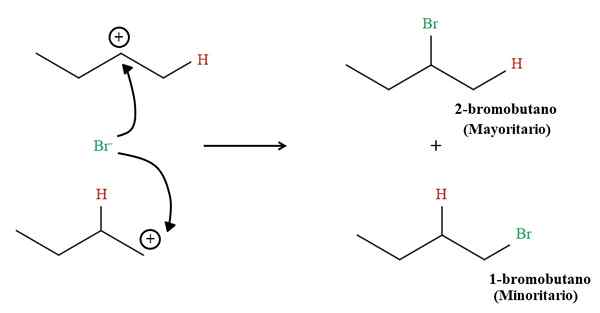 1-buténové hydrobromačné výrobky. Zdroj: Gabriel Bolívar cez Molview.
1-buténové hydrobromačné výrobky. Zdroj: Gabriel Bolívar cez Molview. Podiel oboch výrobkov však nie je 50%; 2-Bromobutano sa vyskytuje oveľa väčší ako 1-brómobután.
Dôvodom je to, že druhý karbocation je stabilnejší ako 1. karbocation, pretože jeho pozitívne zaťaženie je lepšie stabilizované susednými atómami uhlíka; Zatiaľ čo v karbocation 1, atóm vodíka neprispieva takmer žiadnou elektronickou hustotou k tomuto pozitívnemu zaťaženiu (na indukciu alebo hyperkonjugáciu).
Bohatí sa stávajú bohatšími
Markovnikovova vláda sa zrodila z konečných pozorovaní a od nich by sa z nich mohli uvažovať o vyššie uvedených mechanizmoch, aby ich vysvetlili.
Bez potreby vždy zachytiť tieto mechanizmy alebo odpočítať stabilitu sprostredkovateľských karbocations, použije sa jednoduché pravidlo: v elektrofilnom pridávaní sú atómy vodíka smerované k dvojitému uhlíkovi s dvojitým s viacerými atómami vodíka viacerých vodíkových atómov. Tak najviac hydrogenovaného uhlíka sa stáva ešte viac hydrogenovaným.
Môže vám slúžiť: Čo sú vodné anomálie?Na druhej strane, atóm X, v tomto prípade BR, končí v uhlíku dvojitého väzby, ktorý má viac väzieb C-C alebo ktorý je viac nahradený inými atómami, ktoré nie sú vodíkom. Pretože v 1-buténe je jeho terminálny uhlík = cho cho2, Toto je ten, kto prijíma vodík na transformáciu do skupiny -ch3.
Príklady
Prípad pravidla Markovnikov uplatňovaný v hydrobromačnej reakcii bol uvedený vyššie. Platí tiež pre hydrokloklináciu, hydroiodáciu, hydroamináciu a hydratačné reakcie, buď pre alkény alebo alkíny.
V nasledujúcej časti sa budú považovať za cvičenia niekoľko ďalších príkladov.
Vyriešené cvičenia
Cvičenie 1
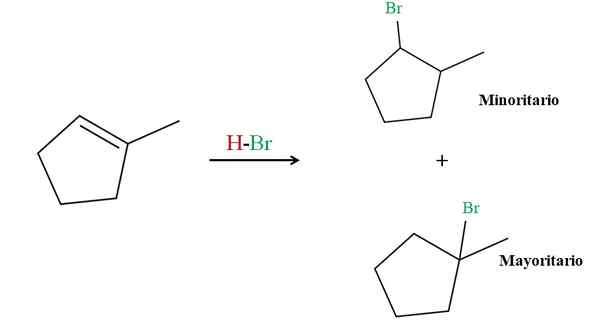 Hydrobromácia 2-metylcipenténu. Zdroj: Gabriel Bolívar cez Molview.
Hydrobromácia 2-metylcipenténu. Zdroj: Gabriel Bolívar cez Molview. Markovnikovovo pravidlo hovorí, že HBR H pre hornú reakciu musí ísť do uhlíka s dvojitou väzbou s väčšími atómami vodíka. V tomto prípade zodpovedá vyššie uvedeným uhlíkom, pretože uhlík vpravo, spojený s Cho3, Nemá ani atómy vodíka.
HBR vodík teda ide do uhlíka vyššie, zatiaľ čo BR končí spojený s uhlíkom vpravo (väčšinový produkt). Na druhej strane, ak je vodík spojený s uhlíkom napravo, BR je nasmerovaný na uhlík vyššie (menší produkt).
Všimnite si, že väčšinový produkt pozostáva z 3. halogenidu, stabilnejší podľa definície a stabilizačných účinkov čiastočného pozitívneho zaťaženia; Zatiaľ čo menšinový produkt je druhým, menej stabilným halogenidom.
Oba výrobky, väčšina a menšie. Tento typ menšinového produktu proti Markovnikovovmu pravidlu je známy ako produkt Antimarkovnikov.
Môže vám slúžiť: Referenčná elektróda: Charakteristiky, funkcie, príkladyCvičenie 2
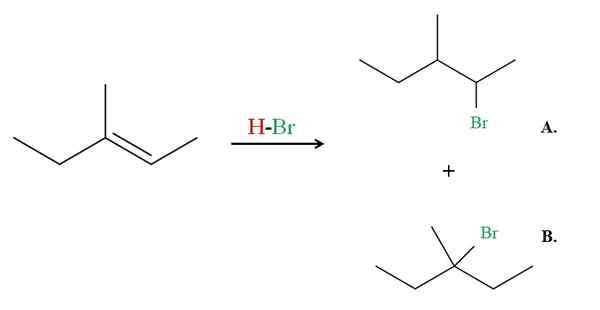 Hydrobromácia 3-metyl-2-penténu. Zdroj: Gabriel Bolívar cez Molview.
Hydrobromácia 3-metyl-2-penténu. Zdroj: Gabriel Bolívar cez Molview. Teraz pozri príklad 3-metyl-2-penténu.
Ak je pozorovaný, pravý uhlík dvojitého väzby má H, zatiaľ čo ten vľavo. Preto HBR pôjde do tohto uhlíka, uhlík musí ísť do stredu, aby spôsobil produkt B. Produkt B je väčšina, pretože opäť je to tretí halogenid, produkt je haluro 2.
Cvičenie 3
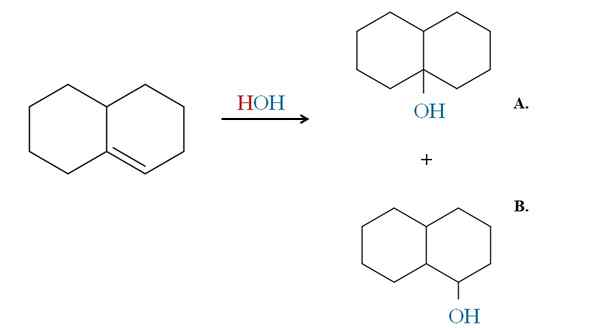 Príklad pravidla Markovnikov v hydratácii cyklického alkénu. Zdroj: Gabriel Bolívar cez Molview.
Príklad pravidla Markovnikov v hydratácii cyklického alkénu. Zdroj: Gabriel Bolívar cez Molview. Predchádzajúce príklady by vygenerovali rovnaké výrobky, ak by sa namiesto HBR použili HCL a HI. To isté je rovnaké ako pri h2O v hydratačnej reakcii katalyzovanej kyselinou a teplom. Oh prichádza nahradiť atóm HX.
Preto nám Markovnikovove pravidlo hovorí, že v elektrofilnom prídavke vyššie prejde OH do uhlíka najviac nahradeného dvojitého väzby s menším vodíkom.
Produkt A je teda väčšina a produkt B menšina. Všimnite si, že produkt A je tretí alkohol a produkt B A 2. alkohol.
Odkazy
- Morrison, r. Tón. a Boyd, R, N. (1987). Organická chémia. 5. vydanie. Redakčný Addison-Wesley Inter-American.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. (10. vydanie.). Wiley Plus.
- Wikipedia. (2020). Markovnikovova vláda. Zdroj: In.Wikipedia.orgán
- Steven a. Hardinger. (2017). Ilustrovaný glosár organickej chémie: Markovnikovova vláda. Získané z: Chem.UCLA.Edu
- Gamini Gunawardena. (24. augusta 2020). Markovnikovova vláda. Chémia librettexts. Získané z: Chem.Librettexts.orgán
- Redaktori Enyclopaedia Britannica. (17. september 2013). Markovnikovova vláda. Získané z: Britannica.com
- DR. Siež. Gevorg. (2020). Organická chémia: Markovnikovovo pravidlo s praktickými problémami. Získané z: ChemistroySteps.com

