Charakteristiky Hososiderina, choroby a diagnostika
- 4002
- 227
- Tomáš Klapka
Ten Hososiderina Je to pigment v hrudkách alebo granuloch, kde sa železo skladuje v živočíšnych tkanivách. Tieto granule sú pre telo málo asimilovateľné, sú uložené vo vnútri buniek a zvyčajne sa objavujú po závažných krvácajúcich udalostiach.
Napriek svojej železitej povahe majú halmosiderínové korpuscles svoju zle definovanú molekulárnu povahu. Je však známe, že sa skladajú z feritínu, denaturovaného feritínu a iných materiálov. Okrem toho sú HALS Harsiderina vždy proti.
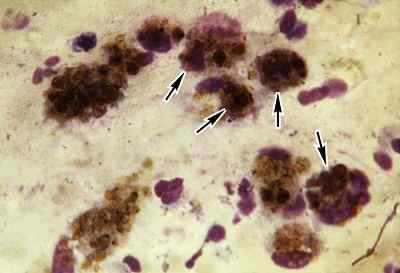
 Hyosiderin Corpuscles (Zdroj: Elsadono [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)] Via Wikimedia Commons) Hyosidein sa najčastejšie vyskytuje v makrofágoch nazývaných „siderofágy“. Sú to makrofágy zodpovedné za fagocytizáciu červených krviniek (erytrocyty) a vďaka tejto fagocytóze sa železo uvoľňuje vo vnútri a ukladá v organele nazývanej „siderosóm“.
Hyosiderin Corpuscles (Zdroj: Elsadono [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)] Via Wikimedia Commons) Hyosidein sa najčastejšie vyskytuje v makrofágoch nazývaných „siderofágy“. Sú to makrofágy zodpovedné za fagocytizáciu červených krviniek (erytrocyty) a vďaka tejto fagocytóze sa železo uvoľňuje vo vnútri a ukladá v organele nazývanej „siderosóm“.
Siderofágy sú bunky produkované kostnou dreni, zodpovednou za uloženie železa na jeho zásobovanie do erytrocytových kmeňových buniek počas tvorby červených krviniek (erytropoéza).
Vzhľad siderofágu svedčí o krvácaní patologickým činidlom alebo nejakým mechanickým stresom. Všeobecne platí, že siderofágy sa objavujú 48 hodín po krvácaní a môžu pretrvávať 2 až 8 týždňov po krvácaní.
Herididerin sa deteguje krvami, tkanivami alebo látkami z rôznych oblastí tela. Tieto vzorky krvi sú ošetrené metódami farbenia, kde sa siderofágy ľahko identifikujú podľa intenzívnej modrej veľkosti a sfarbenia.
[TOC]
Charakteristika
Harsiderín predstavuje súbor štruktúr, ktoré slúžia ako intracelulárne ložisko železa, ktoré sú nerozpustné vo vode a ktoré sa skladujú v systéme phazo endoteliálneho retikula, pečene a kostnej drene. Každý Hososiderina Graneu môže mať vo vnútri až 4500 atómov železa.
Predpokladá sa, že železo uložené v granulách hyerin je tvorené železným fosfátom. Táto zlúčenina je hlavnou zložkou feritínových usadenín bunkového železa.
Môže vám slúžiť: Flora a fauna z HidalgoLady železa v tvare feritínu sú však oveľa menšie a asimilovateľné bunkami ako granule hyerrínu. Zistilo sa, že bunky s feritínom tiež zdieľajú prítomnosť hemosiderínových granúl.
50% ústavy ložísk hemosiderínu pozostáva výlučne v atómoch železa.
Vedci, ktorí pozorovali zŕn hemosiderínu prostredníctvom elektronickej mikroskopie, zistili, že ide o feritínové komplexy, denaturovaný feritín, proteín, uhľohydráty, lipidy a iné materiály.
Hyerrínové granule môžu mať veľkosť, ktorá prechádza z 1 nanometrov do viac ako 20 nanometrov, čo sú veľké kryštály alebo granule. Predpokladá sa, že sú pre bunku iba asimilovateľné peroxidáciou lipidov vyvolanej železom.
Navrhlo sa, že harsiderín predstavuje „ochranný“ biologický mechanizmus, pretože dostupnosť železa, ktorý podporuje reakcie, ktoré spôsobujú voľné radikály vo vnútri buniek vo vnútri buniek, sa znižuje.
Choroby
Úplné fungovanie mechanizmov regulácie železa v tele zvierat je základom pre zdravie, pretože zlyhanie železa vytvára anémiu; Zatiaľ čo preťaženie železa v systéme podporuje akumuláciu HALS v tkanivách.
Táto akumulácia hemosiderínu môže spôsobiť poškodenie tkaniva a spôsobí ochorenie nazývanú „hososideróza“. Toto ochorenie sa vyznačuje spôsobovaním cirhózy pečene, pravdepodobne sprevádzaných karcinómami pečene.
Hemochromatóza, ktorá spočíva v defekte v Lokus HLA-A V krátkom ramene chromozómu 6 môžete predložiť nedostatky v slizničnom regulačnom systéme a správať sa, akoby došlo k trvalému nedostatku železa, a to aj s bohatým príjmom tejto minerálnej minerály.
Môže vám slúžiť: Zvieratá stavovcovToto ochorenie sa môže vyskytnúť dvoma spôsobmi v dôsledku primárnej alebo sekundárnej hemochromatózy. Primárna hemochromatóza je autozomálne recesívne ochorenie. V tomto prípade majú ľudia tendenciu ukladať železo v tkanivách vo forme hemosiderínov nekontrolovaným spôsobom.
Primárna hemochromatóza však môže byť kontrolovaná transfúziami a extrakciami v krvi. Toto v prípade, že je diagnostikovaná skoro, predtým, ako dôjde k nadmernému akumulácii hemosiderínov v tkanivách osoby.
Sekundárna hemochromatóza sa vyskytuje, keď je regulačný systém železa ohromený nadmerným množstvom železa v dôsledku smrti a deštrukcie erytrocytov, určitých ochorenia pečene alebo chronického zvýšenia požitia železa.
Diagnostika
Harsiderins sú diagnostikované z mnohých rôznych hľadísk. Pre patológov sú to hrudky.
Pre elektronických mikroskopistov sú hrudky hyosiderínu elektrodenózne súpravy, ktoré sú vo vnútri siderosómov (telá, ktoré načítajú pigmenty).
Napriek rôznym pozíciám o granulách Hosiderínu sa však všetci zhodujú v tom, že sú nerozpustné granule bohaté na železo a že ich nadmerný obsah je škodlivý pre zdravie organizmu.
Granule harsiderínu tvoria obzvlášť veľké skupiny v bunkách a môžu sa ľahko zafarbiť do tkanív, ktoré sa majú jasne pozorovať pod svetelným mikroskopom.
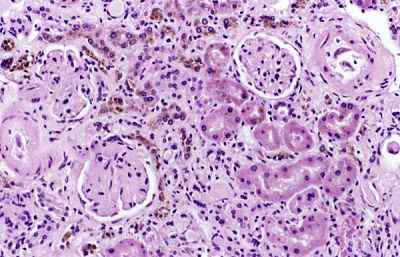 Fotografie tkaniva s korpuscyklami hrdinov (červenkasté sfarbenie) prostredníctvom mikroskopu (zdroj: Invictahog ~ Commonswiki (Talk | Conribs) prostredníctvom Wikimedia Commons)
Fotografie tkaniva s korpuscyklami hrdinov (červenkasté sfarbenie) prostredníctvom mikroskopu (zdroj: Invictahog ~ Commonswiki (Talk | Conribs) prostredníctvom Wikimedia Commons) Harsiderinove granule sú zafarbené Pruskou modrou reakciou pomocou techniky nazývanej Perl Stain. Pomocou tejto techniky boli opísané rozdiely medzi jadrami Hej izolovaných s rôznymi podmienkami: napríklad:
Môže vám slúžiť: Flora a fauna de morelos- Jadrá pacientov, ktorí majú sekundárnu hemochromatózu, majú kryštalickú štruktúru podobnú chemickej receptúre a-feooh chemického vzorca a-feooh
- Prítomní.
V normálnych bunkách ľudskej sleziny, ktoré uchovávali železo v niektorých nosiderínových granuloch, sa pozoruje, že jadrá sú kryštalický ferrihydrit, veľmi podobné jadrám molekúl feritínu.
Pomocou elektronickej mikroskopie.
Všeobecne platí, že častice halmosiderínu ľudí s primárnou hemochromatózou merajú medzi 5,3 a 5, 8 nanometrov; Medzitým u pacientov so sekundárnou hemochromatózou merajú priemer 4,33 a 5 nanometrov.
Táto informácia je relevantná na určenie typu ochorenia, ktoré majú pacienti. Okrem toho je potvrdené genetickou analýzou, čo je genetické zloženie organizmovej bunky v týchto chorých tkanivách.
Odkazy
- Hnedá, w. H. (1910). Zmeny obsahu hososiderínu v pečeni králika počas autolýzy. Journal of Experimental Medicine, 12 (5), 623-637.
- Ganong, W. F. (1999). Lekárska fyziológia. Preskúmanie lekárskej fyziológie, 19.
- Hall, J. A. (2015). Elektronická kniha Guyton a Hall učebnica lekárskej fyziológie. Elsevier Health Sciences.
- Iancu, T. C. (1992). Feritín a hososiderín v patologických tkanivách. Recenzie elektrónovej mikroskopie, 5 (2), 209-229.
- Richter, G. W. (1958). Elektrónová mikroskopia v nemocnici: Komplencia feritínu a výskyt kryštalických latier v ložiskách hadicích. The Journal of Cell Biology, 4 (1), 55-58.
- Zamboni, P., Izzo, m., Fogato, L., Carandina, s., & Spustenie, v. (2003). Hosesiderín moču: nový marker na vyhodnotenie závažnosti chronického žilového ochorenia. Journal of Vascular Surgery, 37 (1), 132-136.
- « Neistý koncept koncepcie, príklady a spôsoby, ako im zabrániť
- Štruktúra pankreatickej lipázy, funkcie, normálne hodnoty »

