Štruktúra kyseliny perracetovej, vlastnosti, získanie, použitie, použitia
- 936
- 113
- Ing. Ervín Petruška
On kyselina peracetová Je to kvapalná organická zlúčenina, ktorej chemický vzorec je C2H4Ani3. Je to peroxid kyseliny octovej, takže je známy tiež ako kyselina perxyoctová. Jeho molekula je podobná ako u chyselej kyseliny octovej3COOH, ale s ďalším kyslíkom v karboxyl.
Patrí do triedy organických peroxidov, ktoré sú molekuly vyrobené človekom. Germidálne a sterilizačné vlastnosti ich vodných roztokov sú známe od roku 1902. Táto akcia môže v niektorých prípadoch uplatniť pri koncentráciách až 0,001%.
 Kyselina peracetová. Autor: Marilú Stea.
Kyselina peracetová. Autor: Marilú Stea. Vďaka tejto vlastnosti je na klinikách a nemocniciach široko používané na sterilizáciu zdravotníckeho zariadenia s ďalšou výhodou, že ich výrobky rozkladu nie sú pre človeka toxické.
Roztoky PAA sú silne oxidujúce, charakteristika, ktorá sa používa na bielenie papierovej buničiny alebo práčovne. Vzťahuje sa tiež na vykonávanie chemických reakcií, v ktorých je potrebná táto vlastnosť, ako je epoxidácia a hydroxylácia.
Jeho oxidačná a dezinfekčná akcia sa používa pri čistení zariadení, kde sa spracúvajú jedlo a nápoje. Okrem toho je pre niektoré kovy korozívne a pri skladovaní sa musí udržiavať mimo organických alebo ľahko oxiditeľných zlúčenín.
Odkazujte, že vaše koncentrované roztoky môžu byť výbušné, a preto sa musí prednostne pripraviť a uložiť na chladných miestach. Jeho korozívna sila sa vzťahuje aj na pokožku, sliznice a tkanivá ľudskej bytosti, takže sa musí manipulovať opatrne a ochranným zariadením.
[TOC]
Štruktúra
Kyselina perxyaktová má molekulu veľmi podobnú ako u kyseliny octovej, ale s ďalším kyslíkom v štruktúre skupiny -cOOH, pretože má 3 atómy kyslíka namiesto dvoch.
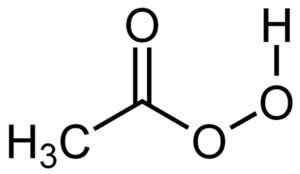 Štruktúra kyseliny peracetovej. Autor: SU-NO-G. Zdroj: sám vyrobený. Zdroj: Wikipedia Commons.
Štruktúra kyseliny peracetovej. Autor: SU-NO-G. Zdroj: sám vyrobený. Zdroj: Wikipedia Commons. Menovanie
- Kyselina peracetová
- Kyselina perxyaktová
- Kyselina etanooperoxoová
- Paa (anglická skratka Kyselina peroxactová).
Vlastnosti
Fyzický stav
Číra bezfarebná tekutina s ostrou vôňou octu.
Molekulová hmotnosť
76,05 g/mol
Bod varu
110 ° C (s výbuchom)
Bod vzplanutia
40,5 ° C (metóda otvoreného pohára)
Samostatná teplota
200 ° C (je to teplota spontánne)
Hustota
1 226 g/cm3 pri 15 ° C
Hrebeň
3 280 cp pri 25,6 ° C
Index lomu
1 3974 až 20 ° C
Rozpustnosť
Je miešateľný s vodou v akomkoľvek pomere. Je rozpustný v polárnych organických rozpúšťadlách, ako je etanol. Mierne rozpustné v aromatických rozpúšťadlách. Veľmi rozpustné v kyseline éteru a kyseliny sírovej.
pH
Menej ako 2.
Disociačná konštanta
Pkdo = 8,20 až 25 ° C (je slabšia ako kyselina octová, ktorú má PKdo = 4,8)
Chemické vlastnosti
Ako kyselina je PAA oveľa slabšia ako kyselina, z ktorej pochádza kyselina octová.
Predstavuje vysoký potenciál ako oxidant. Je vysoko reaktívny, takže je ťažké uložiť, a to obmedzilo jeho použitie.
Jeho degradačné produkty sú kyselina octová chc3Cooh, kyslík alebo2, Peroxid vodíka H2Ani2 a voda h2Ani. H2Ani2 zase degraduje vodu a kyslík. Všetky tieto zlúčeniny sú bezpečné na životné prostredie.
Je to epoxidačné a hydroaxílové činidlo pre olefinické väzby (dvojité odkazy C = C). To znamená, že aktívne sa podieľa na tvorbe epoxidov v dvojitých väzbách organických molekúl a pri pridávaní skupín -OH v týchto.
PAA je korozívny voči niektorým kovom, ako je hladká oceľ, galvanizované železo, meď, mosadz a bronz. Ostatné kovy sú odolné, napríklad nehrdzavejúca oceľ, čistý hliník a tlmivé železo.
Môže vám slúžiť: chemická zlúčeninaÚtok Syntetické a prírodné ďasná a extrahuje plastifikátor niektorých vinylových polymérov.
Má ostrú a akerovú vôňu pripomínajúcu vôňu kyseliny octovej (kyselina octová je hlavnou zložkou octu).
Získanie
Reakciou ľadovcovej kyseliny octovej (bezvodý, tj bez vody) s peroxidom vodíka H2Ani2 V prítomnosti minerálnej kyseliny (ako je kyselina sírová H2SW4), súčasť oxidovanej kyselinou octovou a vodné roztoky kyseliny peria, kyselina octová a H sa získavajú2Ani2.
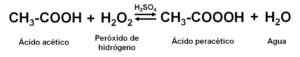 Získanie roztokov kyseliny vodnej permanentu. Autor: Marilú Stea
Získanie roztokov kyseliny vodnej permanentu. Autor: Marilú Stea H2SW4 pôsobí ako katalyzátor alebo reakčný urýchľovač. Používajú sa stabilizačné činidlá, ako je kyselina pyridín-2,6-dikarboxylová kyselina.
Ak sú tieto roztoky destilované, je možné získať vyššiu koncentráciu Perture.
Môže sa tiež získať oxidáciou acetaldehydu ch3Cho s ozónom alebo3, alebo reakciou anhydridu octovej (CH3Co)2Alebo s h2Ani2.
Ďalším spôsobom, ako ho získať priamo na mieste, kde sa vyžaduje, je pridanie tetra-acetyl-etylendiamínu (TAED) do alkalického roztoku H2Ani2.
Žiadosti
V medicíne ako zariadenia sterilizátor
PAA pôsobí ako dezinfekčný lekársky vybavenie na klinikách, nemocniciach, lekárskych a zubných kanceláriách.
 Sterilizované zubné vybavenie. Autor: Daniel Frank. Zdroj: pexels.
Sterilizované zubné vybavenie. Autor: Daniel Frank. Zdroj: pexels. Niektoré zdroje uvádzajú, že ich činnosť proti mikroorganizmom je možné klasifikovať, ako aj: baktérie> Vírus> Spóry baktérií> protozoanové cysty. To znamená, že je účinnejší proti baktériám a menej účinný proti cystom protozoanu.
V štúdiách vykonaných na baktericídnom pôsobení PAA a iných dezinfekčných prostriedkov na vysokej úrovni proti Stafylococcus aureus a Pseudomonas aeruginosa V zariadení pre endoskopiu sa PAA ukázala ako najrýchlejší vo svojom mikrobicídnom účinku.
On Stafylococcus aureus Môže produkovať infekcie v mäkkých tkanivách, v koži, pneumónii a infekcii srdcových tkanív. Ten Pseudomonas aeruginosa Môže produkovať zápal pľúc.
Baktérie tvoria biofilmy, ktoré ich chránia pred vonkajšími stimulmi alebo stresmi, cez hrubú vrstvu extracelulárnych proteínov, polysacharidov a nukleových kyselín.
Tieto biofilmy sú vysoko rezistentné na bežné antibiotiká a dezinfekčné prostriedky. V tímoch, ako sú endoskopy.
PAA útočí na tieto biofilmy pravdepodobne oxidáciou najcitlivejších molekulárnych väzieb proteínov, enzýmov a iných metabolitov. To vedie k prasknutiu bunkových múrov baktérií, ich spór a cýst.
Okrem toho, pri preniknutí do bunky môže PAA oxidovať esenciálne enzýmy, poškodiť transport molekúl a životne dôležité biochemické procesy.
Časy dezinfekcie boli stanovené už niekoľko rokov, ale počas určitých štúdií sa zistilo, že ošetrenie PAA spôsobilo zmeny v tvare buniek už po 5 minútach, s tvorbou vrecka alebo hrčami v bunkovej stene baktérií a kolapsom celulárneho Štruktúry mikroorganizmov po 30 minútach.
Aj keď PAA vynikala za svoju rýchlosť, vedci odporučili prehodnotenie časov stanovených v protokoloch čistenia a dezinfekcie, čím sa zvýšili pre väčšinu antiseptík s vysokou úrovňou, aby sa zabezpečila úplná účinnosť týchto účinkov týchto.
Jedným z negatívnych aspektov PAA je to, že existujú patogény, ku ktorým nie je príliš efektívny, napríklad cysty Giardia Lamblia a Kryptosporidium parvum (parazity, ktoré môžu produkovať hnačku alebo iné črevné podmienky).
Pri čistení odpadových vôd
Dezinfekčný účinok PAA na mestskú odpadovú vodu alebo priemyselné odvetvia bol vyšetrovaný už viac ako 30 rokov.
Môže vám slúžiť: hydrid draselný: štruktúra, formovanie, vlastnosti Čistiaci prostriedok na zvyškovú vodu. Autor: Michal Jarmoluk. Zdroj: Pixabay.
Čistiaci prostriedok na zvyškovú vodu. Autor: Michal Jarmoluk. Zdroj: Pixabay. Medzi jej výhody patrí široké spektrum jej germidskej aktivity aj v prítomnosti organických látok, ako aj skutočnosť, že pre životné prostredie sa nevytvárajú žiadne škodlivé sekundárne výrobky.
Zdá sa, že účinnosť jeho pôsobenia závisí medzi inými faktormi množstva organických látok prítomných v odpadu, od typu a množstva mikroorganizmov, ktoré sa majú odstrániť, na koncentrácii PAA vo vode, ktorá sa má ošetrovať, pH a trvanie liečby.
V niektorých prípadoch sa PAA ukázala lepšie ako chlórnan sodný na dezinfekciu odpadovej vody v tropickom podnebí a bola účinná proti vírusu cholery, medzi mnohými ďalšími patogénmi.
Jedným z negatívnych bodov je však to, že v dôsledku zostávajúcej kyseliny octovej po dezinfekcii je vodný odpad naplnený organickými látkami, čo zvyšuje riziko nového rastu mikroorganizmov.
Na druhej strane je to drahý produkt, takže v dôsledku tohto aspektu nie je veľmi konkurencieschopný napríklad s chlórnanom sodným.
V potravinárskom priemysle
Byť silným oxidačným činidlom je veľmi účinný proti mikroorganizmom pri nízkych teplotách, čo viedlo k svojmu širokému využívaniu ako baktericídny a fungicíd pri spracovaní potravín a nápojov.
To zahŕňa rastliny na spracovanie mäsa a kuracie mäso, mliečne výrobky, pivovary, vinári alebo vinárske vinárstvo a nealkoholické nápoje. Na všetkých týchto miestach sa PAA vzťahuje na to, že je ideálny na čistenie In situ (na mieste).
Enzýmy nájdené v niektorých potravinách, ako je peroxidáza a kataláza, ktoré deaktivujú peroxid vodíka H2Ani2, Nevykazujú škodlivý účinok na kyselinu v permy. Proteínový odpad to tiež nepoškodzuje.
Vzhľadom na to, že v potravinách sa PAA rozkladá v kyseline octovej a vodíkového vodíka, jeho použitie sa považuje za bezpečné v aplikáciách, v ktorých nie je jedlo opláchnuté.
Slúži ako dezinfekčný prostriedok a sterilizácia pre nehrdzavejúce oceľové a sklenené nádrže, potrubia a nákladné autá, ktoré slúžia na prepravu a skladovanie nápojov.
 Nádrže z nehrdzavejúcej ocele na skladovanie piva. Autor: Roberta Keiko Kitahara Santana. Zdroj: UNSPASH.
Nádrže z nehrdzavejúcej ocele na skladovanie piva. Autor: Roberta Keiko Kitahara Santana. Zdroj: UNSPASH. Jeho charakteristika vytvárania ne -toxických výrobkov a to, že pri vysokom riedení nevyrába príchute ani zápach, predstavujú pre tieto odvetvia čas a úspory peňazí.
V priemysle buničiny a papiera
Kyselina perracetová je dôležitým činidlom bez chlóru v technológii bielenia v priemysle výroby papierovej buničiny.
Niektorí autori považujú kyselinu peracetovú za aktivovaný derivát H2Ani2, Kde bol jeden z jeho hydrogénov nahradený skupinou ACILO C3C (= o)-.
V dôsledku toho kyselina Perture reaguje s organickými substrátmi vo väčšej miere ako h2Ani2 a to sa môže použiť v oxidačných reakciách za miernych podmienok ako s h2Ani2.
Za neutrálnych alebo mierne alkalických podmienok ión peracetát CH3C (= o) oo- na to, aby bol silný nukleofil (priťahuje sa atómami deficitu elektrónov), selektívne premiešajte chromofory alebo farebné zlúčeniny prítomné v papierovej buničine.
To umožňuje týmto odvetviam mať veľmi efektívne bielenie a ktorého odpad neznečisťuje ich vodné odpadové vody.
Môže vám slúžiť: čo je Erristeneo?Pri výrobe iných chemických zlúčenín
Kyselina perracetová slúži ako oxidant na prípravu epoxidových zlúčenín ako katalyzátor na výrobu polyesterových živíc a získanie kaprolaktamu a glycerolu.
Pri regenerácii polymérov na recykláciu
Niektorým vedcom sa podarilo obnoviť užitočné materiály pri ošetrení určitého polymérneho odpadu pomocou riešení PAA.
Tento proces sa vykonáva oxidáciou určitého odpadu polymérov vystužených uhlíkovými vláknami z leteckých aktivít, s roztokmi ľadovcovej kyseliny octovej a peroxidom vodíka.
Týmto spôsobom sa generuje kyselina Perture In situ, ktorá rozdeľuje epoxidovú živicu o 97%, takže uhlíkové vlákna sú neporušené.
Potom sa získava viac ako 90% kyseliny octovej, čo vedie k ďalšiemu rozkladu polyméru, ktorý generuje regenerovateľné alifatické a fenolové zlúčeniny.
Uhlíkové vlákna sa získava čisté a udržuje jej odolnosť voči dĺžke a trakcii porovnateľná s vodnými vláknami.
 Uhlíkové vlákno. CJP24 [verejná doména]. Zdroj: Wikipedia Commons.
Uhlíkové vlákno. CJP24 [verejná doména]. Zdroj: Wikipedia Commons. Tento proces sa vykonáva za mäkkých podmienok, bez plynných emisií, čo ho robí šetrným k životnému prostrediu.
Práčovňa
Kvôli svojej oxidačnej sile farebných zlúčenín sa kyselina peracetová používa pri bielení bielizne. V týchto prípadoch sa používa zmes tetra-atyl-etylendiamín s H s H2Ani2 V alkalickom médiu na jeho získanie na mieste.
Jeho interval aplikácie je veľmi široký, pretože sa dá použiť v tvrdých vodách alebo ktoré obsahujú vysoký podiel vápnikových a horčíkových solí, pri pH medzi 3,0 a 7,5 a teplotami od 0 do 40 ° C.
Riziká
Kyselina perracetová alebo PAA môžu byť vysoko korozívne. Je to silne dráždi pokožku a oči.
Ak sa ich roztoky požičia, spôsobia koróziu slizníc úst, hrdla, pažeráka a gastrointestinálneho traktu, čo spôsobuje bolesť a ťažkosti s prehĺtaním.
Ak sú ich výpary vdýchnuté.
Riešenia obsahujú. Môžu rozkladať výbušne. Ak koncentrácia PAA v roztoku presahuje 56%, môže sa spustiť v dôsledku odparovania kyseliny kyseliny octovej.
Trusu by sa malo vyhnúť tepla. Považuje sa za horľavú tekutinu. Jeho rozklad je násilný s výbuchom pri 110 ° C. Musí sa skladovať na čerstvých miestach, najlepšie pod ochladením alebo na veľmi dobre vetraných miestach.
Je preto silne oxidačný, preto v kontakte s organickými materiálmi. Pri skladovaní musí byť izolovaný z iných zlúčenín, najmä organických, palivových, horľavých alebo oxiditeľných zlúčenín. Musí byť oddelený od kyselín, alkalis a ťažkých kovov.
Keď sa zahrieva na rozklad emituje akry a dráždi pár, ktoré dráždia oči, nos a krk.
Ak sa vyliaje, nemalo by sa nechať prúdiť do odtokov, pretože v týchto nebezpečenstvách ohňa alebo výbuchu sa vytvorí.
Ako preventívne opatrenia na manipuláciu, gumové rukavice a ochranné odevy, ochrana tváre alebo ochrana očí (okuliare alebo bezpečnostné okuliare), ochrana dýchacích ciest a nejedenie, pitie alebo fajčenie sa odporúča počas práce s ich roztokmi.
Odkazy
- Alebo.Siež. Lekárska knižnica. (2019). Kyselina peracetová. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Das, m. a kol. (2018). Účinná metóda opätovného systému CFRP pomocou kyseliny peracetovej. Udržateľná chémia a inžinierstvo ACS. Získané z krčiem.ACS.orgán.
- Čínština. a kol. (2017). Morfologické baktericídne rýchlo pôsobiace účinky kyseliny peracetovej, dezinfekčný prostriedok na vysokej úrovni, proti Stafylococcus aureus a Aeruginózne pseudomcas Biofilmy v hadičkách. Antimikrob odoláva infiku riadeniu. 2017: 6: 122. NCBI sa zotavila.NLM.NIH.Vláda.
- Chlieb, G.X. a kol. (1999). Reaktivita kyseliny ferulovej a jej odvodená smerom k póze vodíka a kyseliny peraciovej. J. Poľnohospodárstvo. Potravinárska chémia. 1999, 47, 3325-3331. Získané z krčiem.ACS.orgán.
- Kitis, Mehmet. (2004). Dissinfekcia odpadovej vody s kyselinou peracetovou: prehľad. Environment International 30 (2004) 47-55. Zotavené z vedeckých pracovníkov.com.
- « Štruktúra kyseliny fenylátovej, vlastnosti, použitie, účinky
- Charakteristiky vertikálneho myslenia, metóda a príklady »

