Charakteristiky a účinky karboxyhemoglobínu
- 720
- 199
- MUDr. Žigmund Boška
Ten karboxyhemoglobín Je to hemoglobín pripojený k oxidu uhoľnatého (CO). Hemoglobín je proteín, ktorý transportuje kyslík krvou na ľudí a v mnohých ďalších stavovcoch.
Na prepravu kyslíka sa k tomu musí pridať hemoglobín. Max Perutz, chemik a Nobelova cena, ktorá sa narodila vo Viedni v roku 1914 a zabila v Cam-Bridge v roku 2002, nazývaná „správanie sa pre kyslík hemoglobínu“.
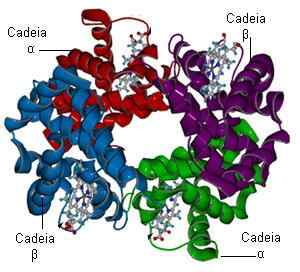
 Štruktúra hemoglobínu (zdroj: Bielabio prostredníctvom Wikimedia Commons)
Štruktúra hemoglobínu (zdroj: Bielabio prostredníctvom Wikimedia Commons) Predstavte si dve molekuly hemoglobínu schopné spojiť každú do štyroch molekúl kyslíka. Jeden už má tri molekuly kyslíka a druhý. Ak sa javí iná molekula kyslíka, otázka je nasledovná: Viaže sa na „bohatú“, ktorá už má tri alebo „chudobné“, ktoré nemá? Pravdepodobnosť je 100 až 1, že bohatá molekula je nasmerovaná.
Predstavte si teraz ďalšie dve molekuly hemoglobínu. Jeden má 4 molekuly kyslíka (je nasýtený) a druhý má iba jeden. Ktorá z molekúl je najpravdepodobnejšia, že dá tkanivá kyslík, bohatých alebo chudobných? Najchudobnejší ľahšie dodá kyslík ako bohatý.
Distribúciu kyslíka v molekule hemoglobínu možno považovať za biblické podobenstvo: „... kto má, bude to dané a kto nemá, dokonca to, čo má, bude odstránené ...“ (Mt, 13:12 ). Z fyziologického hľadiska je toto „nemorálne“ správanie molekuly hemoglobínu plné významu, poloha prispieva k prínosu kyslíka k tkanivám.
Oxid uhoľnatý však bez ohľadu na počet atómov kyslíka spojený s molekulami hemoglobínu, „zametanie“ so všetkými. To znamená, že v prítomnosti hojného CO je všetok kyslík pripojený k hemoglobínu nahradený CO.
[TOC]
Štrukturálne charakteristiky
Ak chcete hovoriť o karboxyhemoglobíne, ktorý nie je ničím iným ako stavom hemoglobínu spojeného s oxidom uhoľnatého, je potrebné najprv odkazovať na hemoglobín vo všeobecnosti.
Hemoglobín je proteín zložený zo štyroch podjednotiek vytvorených polypeptidovým reťazcom známym ako globín a non -proteínová prírodná skupina (protetická skupina) nazývaná HEMO.
Môže vám slúžiť: Bioestadistika: História, oblasť štúdia a aplikácieKaždá skupina Hemo obsahuje atóm železa v železnom štáte (viera2+). Toto sú atómy schopné spájať kyslík bez oxidácie.
Hemoglobín tetramér je tvorený dvoma podjednotkami alfa globínu, každá 141 aminokyselín a dve podjednotky beta globínu, každá 146 aminokyselín.
Hemoglobín formy alebo štruktúry
Ak hemoglobín nie je spojený s atómom kyslíka, štruktúra hemoglobínu je tuhá alebo napätá, čo je produkt tvorby slaných mostíkov vo vnútri.
Kvartérna štruktúra hemoglobínu bez kyslíka (deoxigenada) je známa ako „T“ alebo napätá štruktúra a okysličený hemoglobín (oxyhemoglobín) je známa ako „R“ alebo uvoľnená štruktúra.
Prechod zo štruktúry T na štruktúru R dochádza prostredníctvom spojenia kyslíka na atóm železa (viera2+) skupiny Hemo pripojenej ku každému reťazcu globínu.
Kooperatívne správanie
Podjednotky, ktoré tvoria štruktúru hemoglobínu, vykazujú kooperatívne správanie, ktoré možno vysvetliť nasledujúcim príkladom.
Môžete si predstaviť deoxygenovanú molekulu hemoglobínu (v štruktúre T) ako vlnená škrupina s veľmi skrytými väzbovými miestami kyslíka (skupiny HEM).
Keď sa táto napätá štruktúra spojí s molekulou kyslíka, rýchlosť únie je veľmi pomalá, ale táto únia je dostatočná na to, aby sa lopta trochu uvoľnila a priniesla nasledujúcu skupinu Hemo na povrch, čím sa rýchlosť, s akou viaže nasledujúci kyslík opakovanie procesu a zvýšenie príbuznosti s každou úniou.
Účinky oxidu uhoľnatého
Aby sme študovali účinky oxidu uhoľnatého na prepravu plynov v krvi, je to najskôr potrebné.
Môže vám slúžiť: briológia: čo je, história, aké štúdieKrivka oxihemoglobínu má sigmoid alebo „s“ tvar, ktorý sa líši v závislosti od čiastočného tlaku kyslíka. Krivka je zrejmá z analýz vyrobených na vzorky krvi, ktoré sa používajú na jeho vybudovanie.
Najkreslenejšia oblasť krivky sa získava tlakmi pod 60 mmHg a pri väčších tlakoch ako je táto krivka tendenciu sploštiť, akoby dosiahla náhornú plošinu.
Keď je v prítomnosti určitých látok, krivka môže vykazovať významné odchýlky. Tieto odchýlky vykazujú zmeny, ktoré sa vyskytujú v afinite hemoglobínu v dôsledku kyslíka k rovnakému PO2.
Na kvantifikáciu tohto javu sa zaviedla miera afinity hemoglobínu kyslíkom, známa ako hodnota ppäťdesiat, čo je čiastočná hodnota tlaku kyslíka, na ktorú je hemoglobín 50% nasýtený; to znamená, že keď je polovica ich hemo skupín zjednotená s kyslíkovou molekulou.
V štandardných podmienkach, ktoré sa musia chápať ako pH 7.4, čiastočne 40 mmHg kyslíka a teplota 37 ° C, P, Ppäťdesiat Pod dospelým mužom je 27 mm Hg alebo 3,6 kPa.
Aké faktory môžu ovplyvniť afinita hemoglobínu kyslíkom?
Afinita k kyslíku hemoglobínu obsiahnutého v erytrocytoch sa môže znížiť v prítomnosti 2,3 defoglycelera (2-3DPG), oxidu uhličitého (CO (CO2) vysokých koncentrácií protónov alebo zvýšenou teplotou; A to isté platí pre oxid uhoľnatý (CO).
Funkčné dôsledky
Oxid uhoľnatý je schopný interferovať s funkciou transportu kyslíka v arteriálnej krvi. Táto molekula je schopná spojiť hemoglobín a tvoriť karboxyhemoglobín. Je to preto, že má afinitu k hemoglobínu asi 250 krát väčší ako O2, Takže je schopný to pohnúť, aj keď je s ňou spojený.
Môže vám slúžiť: Czapek Agar: Nadácia, príprava, použitie a obmedzeniaTelo produkuje natrvalo oxid uhoľnatý, hoci v malých množstvách. Tento plyn, bezfarebný a toaletný, pripojí sa k skupine Hemo rovnakým spôsobom ako alebo2, A zvyčajne existuje asi 1% krvného hemoglobínu, ako je karboxyhemoglobín.
Pretože neúplné spaľovanie organických látok produkuje CO, podiel karboxyhemoglobínu u fajčiarov je oveľa vyšší, je schopný dosiahnuť hodnoty medzi 5 a 15% z celkového hemoglobínu. Chronické zvýšenie koncentrácie karboxyhemoglobínu je škodlivé pre zdravie.
Zvýšenie množstva CO, ktorá je vdychovaná, ktorá generuje viac ako 40% karboxyhemoglobínu ohrozuje život. Keď je miesto viazania železa v väzbe zaberá CO, nemôžete zasiahnuť O2.
Únia CO spôsobuje prechod z hemoglobínu na štruktúru R, takže hemoglobín ďalej znižuje schopnosť dodať alebo2 V krvných kapilároch.
Carboxyhemoglobin má svetlo červenú farbu. Pacienti otrávení CO si preto osvojujú ružovú farbu, dokonca aj v stave paralýzy kómy a respiračného paralýzy. Najlepšia liečba, ktorá sa snaží zachrániť životnosť týchto pacientov, je urobiť čistý, dokonca aj hyperbarický kyslík, aby sa pokúsil vytlačiť spojenie železa s CO.
Odkazy
- Líška, s. Jo. (2006). Human Physiology 9. vydanie (PP. 501-502). McGraw-Hill Press, New York, USA.
- Murray, r. Klimatizovať., Granner, D. Klimatizovať., Mayes, P. Do., & Rodwell, V. W. (2014). Harperova ilustrovaná biochémia. McGraw-Hill.
- Rawn, J. D. (1998). Biochemistry (1989). Burlington, Severná Karolína: Publishers Neil Patterson (c) n. Lalioti, CP Raptopoulou, a. Terzis, a. Panagiotopoulos, SP perlepes a. Maness-Zouopa, J. Chem. SOC. Dalton Trans, 1327.
- Robert M. Berne, Matthew N. Vyberať. (2001) Fyziológia. (3. ED.) Harcourt Editions, s.Do.
- West, J. B. (1991). Fyziologický základ lekárskej praxe. Williams a Wilkins
- « Kvalitatívne hodnotiace charakteristiky, výhody, príklady
- Teória pozorovacieho učenia, charakteristiky, príklady »

