Štruktúra, štruktúra, vlastnosti a použitie strieborného bromuro (AGBR)
- 1348
- 121
- Tomáš Klapka
On Striebro Je to anorganická soľ, ktorej chemický vzorec je Agbr. Jeho pevná látka pozostáva z ag katiónov+ A br Aniss- v pomere 1: 1, priťahovaný elektrostatickými silami alebo iónovými väzbami. Je to vidieť, akoby kovové striebro dalo jeden z jeho valenčných elektrónov do molekulárnej brómu.
Jeho povaha pripomína jeho „bratia“ chlorid a strieborný Yoduro. Tri soli sú nerozpustné vo vode, majú podobné farby a navyše sú citlivé na svetlo; to znamená, že trpia fotochemickými reakciami. Táto vlastnosť sa použila pri získavaní fotografií, čo je výsledok zníženia iónov AG+ na kovové striebro.
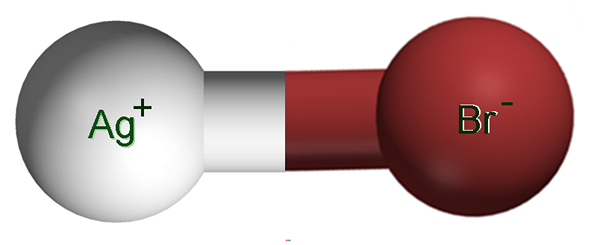
 Ióny strieborného bromidu. Zdroj: Claudio Pistilli [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]
Ióny strieborného bromidu. Zdroj: Claudio Pistilli [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)] Na hornom obrázku je zobrazený ag iónový pár+Br-, v ktorých biele a hnedé gule zodpovedajú iónom AG+ a br-, respektíve. Tu predstavujú iónovú väzbu ako AG-BR, ale je potrebné naznačovať, že neexistuje taká kovalentná väzba medzi oboma iónmi.
Môže sa zdať protichodné, že striebro je ten, kto poskytuje čiernu farbu bezfarebných fotografií. Je to preto, že AGBR reaguje so svetlom a vytvára latentný obraz; čo sa potom zintenzívňuje zvýšením zníženia striebra.
[TOC]
Štruktúra bromidu striebra
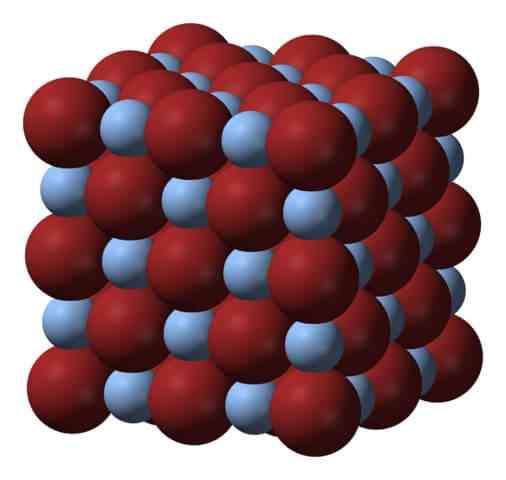 Kryštalická štruktúra strieborného bromidu. Zdroj: Benjah-Bmm27 Via Wikipedia.
Kryštalická štruktúra strieborného bromidu. Zdroj: Benjah-Bmm27 Via Wikipedia. Nad sieťou alebo kryštalickou štruktúrou strieborného bromidu. Tu je uvedené vernejšie znázornenie rozdielu veľkosti medzi iónovými rádiami Ag+ a br-. BR anióny-, Viac objemných, nechajte interstices, kde sa nachádzajú katióny+, ktorý je obklopený šiestimi br- (a naopak).
Táto štruktúra je charakteristická pre kubický kryštalický systém, konkrétne typ soli; To isté napríklad pre chlorid sodný, NaCl. V skutočnosti to obrázok uľahčuje tým, že má dokonalý limit kubického.
Môže vám slúžiť: Referenčná elektróda: Charakteristiky, funkcie, príkladyNa prvý pohľad sa dá poznamenať, že medzi iónmi existuje určitý rozdiel vo veľkosti. Toto a možno aj elektronické charakteristiky AG+ (a možného účinku niektorých nečistôt), vedie k kryštálom AGBR, ktoré prezentujú defekty; To znamená, že stránky, kde je sekvencia objednávok iónov vo vesmíre „zlomená“.
Kryštalické defekty
Tieto defekty pozostávajú z medzier, ktoré zanechali neprítomné alebo vysídlené ióny miesta. Napríklad medzi šiestimi aniónmi BR- Normálne by malo byť krik+; Namiesto toho však môže byť vákuum, pretože striebro sa presunulo do iného interstície (defekt Frenkel).
Aj keď ovplyvňujú kryštalickú sieť, uprednostňujú strieborné reakcie svetlom; A čím väčšie kryštály alebo ich klaster (veľkosť zŕn), tým väčší počet defektov, a preto bude citlivejší na svetlo. Podobne nečistoty ovplyvňujú štruktúru a túto vlastnosť, najmä tie, ktoré sa dajú znížiť elektrónmi.
V dôsledku toho posledne uvedené veľké kryštály AGBR vyžadujú zníženie nižšej expozície svetlu; to znamená, že sú viac žiaduce na fotografické účely.
Syntéza
V laboratóriu môžete syntetizovať strieborný bromid miešanie vodného roztoku dusičnanu striebra, Agno3, So soľou bromidu sodného, nabab. Prvá soľ prináša striebro a druhý bromid. Nasleduje dvojitá reakcia na posunutie alebo metatézu, ktorá môže byť znázornená s chemickou rovnicou nižšie:
Agno3(aq) + nabab (s) => nano3(aq) + agbr (s)
Môže vám slúžiť: bromid sodný (NABR)Všimnite si, že soľ dusičnan solí, nano3, Je rozpustný vo vode, zatiaľ čo AgBr sa vyzráža ako pevná látka so slabou žltou farbou. Následne sa tuhá látka premyje a podstúpi vákuum. Okrem Nabla, KBR by sa mohol použiť aj ako zdroj bromuróznych aniónov.
Na druhej strane, AGBR je možné získať prostredníctvom svojho minerálu Bromirita a procesov čistenia splatnosti.
Vlastnosti
Vzhľad
Hlinená žltá pevná látka podobná hlinke.
Molekulárna hmotnosť
187,77 g/mol.
Hustota
6 473 g/ml.
Bod topenia
432 ° C.
Bod varu
1502 ° C.
Rozpustnosť
0,140 g/ml pri 20 ° C.
Index lomu
2,253.
Tepelná kapacita
270 j/kg · k.
Citlivosť na svetlo
V predchádzajúcej časti sa uviedlo, že v kryštáloch AGBR sú defekty, ktoré podporujú citlivosť tejto soli vo svetle, pretože zachytia vytvorené elektróny; A teoreticky im bránia v reagovaní s inými druhmi v strede, ako je kyslík vzduchu.
Elektrón sa uvoľňuje z reakcie BR- S fotón:
Br- + HV => 1/2br2 + a-
Všimnite si, že existuje2, ktoré zafarbia pevnú červenú, ak sa neodstráni. Oslobodené elektróny znižujú katióny+, Vo svojich medzisteniach, kovové striebro (niekedy predstavované ako AG0):
Zápis+ + a- => Ag
Potom mať čistú rovnicu:
Agbr => ag + 1/2br2
Keď sa vytvoria „prvé vrstvy“ kovového striebra na povrchu, hovorí sa, že existuje latentný obraz, stále neviditeľný pre ľudské oko. Tento obraz sa stáva miliónmi krát viac viditeľnejším, ak vo vývojovom procese) vo vývojovom procese) zvyšuje redukciu kryštálov AGBR na kovové striebro redukciu kryštálov AGBR na kovové striebro (
Môže vám slúžiť: Carbon 12: jadrová notácia, história, komentáreŽiadosti
 Čiernobiele vreckové hodiny. Zdroj: pexels.
Čiernobiele vreckové hodiny. Zdroj: pexels. Strieborný bromid je najpoužívanejší zo všetkých svojich halogenidov v oblasti odhalenia fotografických filmov. Agbr sa aplikuje na tieto filmy, vyrobené z acetátu celulózy, suspendované v želé (fotografická emulzia) a v prítomnosti 4- (metylačného) fenolsulfátu (metol) alebo fenidónu a hydrochinónón.
So všetkými týmito činidlami sa môže život dať latentnému obrazu; Dokončiť a urýchliť transformáciu iónového na kovové striebro. Ale ak nepostupujete s určitou starostlivosťou a zážitkami, všetko povrchové striebro sa oxiduje a kontrast medzi čiernou a bielym farbám sa skončí.
Preto sú životne dôležité v kúpeľniach nezamestnanosti, fixácie a umývania fotografických filmov.
Existujú umelci, ktorí s týmito procesmi hrajú takým spôsobom, že vytvárajú sivé nuansy, ktoré obohacujú krásu obrazu a ich vlastný odkaz; A to všetko, niekedy, niekedy bez podozrenia, vďaka chemickým reakciám, ktorých teoretický základ sa môže stať trochu zložitý a ľahký AGBR citlivý a ktorý označuje východiskový bod.
Odkazy
- Wikipedia. (2019). Striebro. Zdroj: In.Wikipedia.orgán
- Michael W. Davidson . (13. novembra 2015). Galéria digitálneho obrázka polarizovaného svetla: Silver Bromid. Olympus. Obnovené z: Micro.Magnet.Fsu.Edu
- Crystran Ltd. (2012). Strieborný bromid (AGBR). Získané z: Crystran.co.Uk
- Lothar Duenkel, Juergen Eichler, Gerhard Ackermann a Claudia Schneeweiss. (29. júna 2004). Samostatne vyrobené emulzie založené na strieborných bromidoch pre používateľov v holografii: Výroba, spracovanie a aplikácia, Proc. SPIE 5290, Praktická holografia XVIII: Materiály a aplikácie; Doi: 10.1117/12.525035; https: // doi.org/10.1117/12.525035
- Alan G. Forma. (1993). Anorganická chémia. (Druhé vydanie.). Redaktor sa vrátil.
- Carlos Güido a Ma Eugenia Bautista. (2018). Úvod do fotografickej chémie. Získané z: Fotografie.Ceduc.com.mx
- Garcia d. Krásny. (9. januára 2014). Chémia, fotografia a chema madoz. Získané z: dimetylsulfuro.je
- « Ako vzdelávať dieťa primerane 13 praktických rád
- Cyklobutánska štruktúra, vlastnosti, použitie a syntéza »

