Atómový objem
- 4278
- 658
- Alfréd Blaho
Čo je to atómový objem?
On Atómový objem Je to relatívna hodnota, ktorá označuje vzťah medzi molárnou hmotnosťou prvku a jeho hustotou. Potom tento objem závisí od hustoty prvku a hustota závisí od fázy a od toho, ako sú atómy usporiadané v tomto.
Takže atómový objem pre prvok Z nie je rovnaký v inej inej fáze, ako vykazuje pri teplote miestnosti (kvapalina, tuhá látka alebo plyn) alebo keď je súčasťou určitých zlúčenín. Atómový objem Z v ZB zlúčenine sa teda líši od Z v zlúčenine ZB.
Pretože? Aby som to pochopil, je potrebné porovnať atómy napríklad s niektorými guličkami. Mranice majú svoju materiálnu hranicu veľmi dobre definovanú, čo je pozorované vďaka ich brilantnému povrchu. Na druhej strane, hranica atómov je rozptýlená, hoci ich možno považovať za diaľkovo sférické.

To, čo určuje bod za atómovou hranicou, je pravdepodobnosť nájdenia elektrónu a tento bod môže byť ďalej alebo bližšie k jadru v závislosti od toho, koľko susedných atómov interaguje okolo atómu, ktorý sa blíži.
Atómový objem a rádio
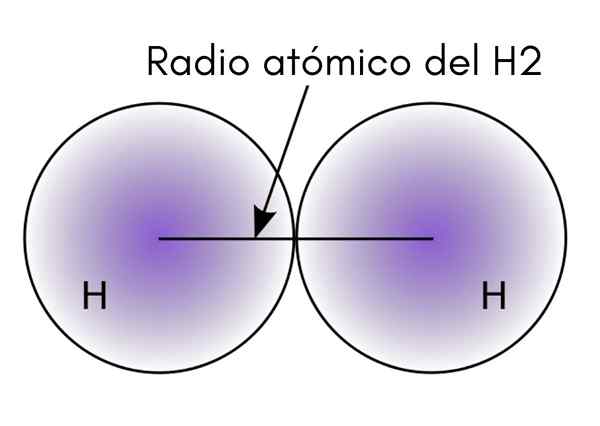
Pri interakcii dvoch atómov H v molekule H2, Polohy ich jadier sú definované, ako aj vzdialenosti medzi nimi (internukleárne vzdialenosti). Ak sú oba atómy sférické, polomer je vzdialenosť medzi jadrom a difúznym okrajom:

Na vynikajúcom obraze je vidieť, ako sa pravdepodobnosť nájdenia elektrónu znižuje, keď sa pohybuje od jadra. Rozdelenie dvoma internukleárnou vzdialenosťou sa získa atómový polomer. Potom, za predpokladu sférickej geometrie pre atómy, sa vzorec používa na výpočet objemu gule:
V = (4/3) (pi) r3
Môže vám slúžiť: horľavostiV tejto expresii R je atómový polomer stanovený pre molekulu H2. Hodnota V vypočítaná touto malú presnú metódu sa môže zmeniť, ak sa napríklad hôc H uvažuje2 v kvapalinovom alebo kovovom stave. Táto metóda je však veľmi nepresná, pretože formy atómov sú veľmi ďaleko od ideálnej sféry v ich interakciách.
Na stanovenie atómových objemov v tuhých látkach sa berie do úvahy veľa premenných týkajúcich sa usporiadania a ktoré sa získavajú pomocou X -Bray Difraction Studies.
Dodatočný vzorec
Molárna hmota exprimuje množstvo hmoty, ktorá má mól atómov chemického prvku.
Jeho jednotky sú g/mol. Na druhej strane, hustotou je objem, ktorý zaberá gram prvku: G/ml. Pretože jednotky atómového objemu sú ML/mol, musíte hrať s premennými, aby ste dosiahli požadované jednotky:
- (g/mol) (ml/g) = ml/mol
Alebo čo je to isté:
- (Molárna hmotnosť) (1/d) = v
- (Molárna hmotnosť/d) = v
Objem móla atómov prvku sa teda môže ľahko vypočítať; Zatiaľ čo s vzorcom sférického objemu sa vypočíta objem jednotlivého atómu.
Na dosiahnutie tejto hodnoty od prvej hodnoty je potrebná konverzia prostredníctvom čísla Avogadro (6,02,10-23).
Ako sa mení atómový objem v periodickej tabuľke?
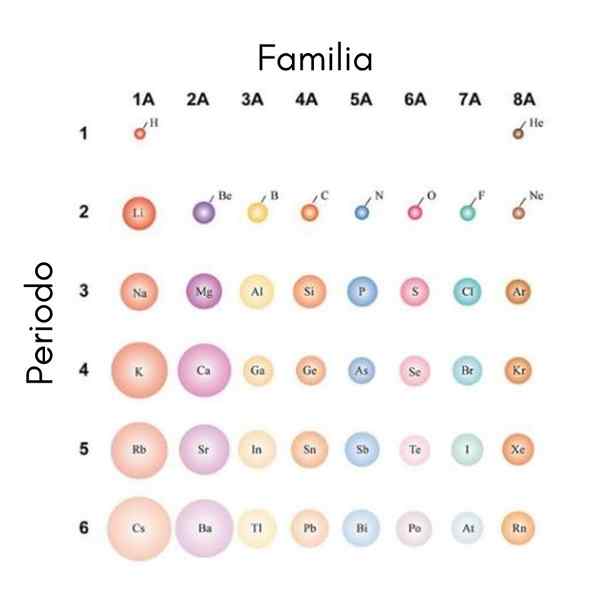
Ak sa atómy považujú za sférické, potom ich variácia bude rovnaká, čo sa pozoruje v atómových rádiách. V nadradenom obrázku, ktorý zobrazuje reprezentatívne prvky, je znázornené, že sprava doľava atómov trpaslí; Na druhej strane, zhora nadol sa stávajú objemnejšími.
Je to preto, že v rovnakom období jadro zahŕňa protóny, ktoré sa pohybuje doprava. Tieto protóny vyvíjajú príťažlivú silu na vonkajšie elektróny, ktoré cítia účinné jadrové zaťaženie zEf, Menšie ako skutočné jadrové zaťaženie z.
Môže vám slúžiť: Disposio: Štruktúra, vlastnosti, získanie, použitieElektróny vnútorných vrstiev odpudzujú vrstvy vonkajšej vrstvy, čím sa znižujú účinok jadra na ne; Toto je známe ako efekt obrazovky. V rovnakom období účinok obrazovky nedokáže pôsobiť proti zvýšeniu počtu protónov, takže elektróny vnútornej vrstvy nezabránia kontrakcii atómov.
Keď však v skupine zostupuje, sú povolené nové úrovne energie, ktoré umožňujú elektrónom obiehať jadro. Podobne sa zvyšuje počet elektrónov vo vnútornej vrstve, ktorých tieniace účinky sa začnú znižovať, ak jadro opäť pridá protóny.
Z týchto dôvodov sa oceňuje, že skupina 1A má najjemnejšie atómy, na rozdiel od malých atómov skupiny 8a (alebo 18), atm.
Atómové objemy prechodných kovov
Atómy prechodných kovov obsahujú elektróny do vnútorných orbitálov d. Toto zvýšenie efektu obrazovky a, ako aj skutočné jadrové zaťaženie Z, sú takmer rovnako zrušené, takže ich atómy si zachovávajú podobnú veľkosť v rovnakom období.
Inými slovami: v období, prechodné kovy vykazujú podobné atómové objemy. Tieto malé rozdiely sú však pri definovaní kovových kryštálov nesmierne významné (akoby to boli kovové mranice).
Príklady atómového objemu
Na výpočet atómového objemu jedného prvku sú k dispozícii dva matematické vzorce, každý so zodpovedajúcimi príkladmi.
Príklad 1
Vzhľadom na atómový rádiogén -37 pm (1 pikometra = 10-12m)-a cézium-265 pm-, vypočítajte svoje atómové objemy.
Môže vám slúžiť: benzaldehydPomocou vzorca sférického objemu máte:
VložkaH= (4/3) (3.14) (37 hod.)3= 212,07 PM3
VložkaCs= (4/3) (3.14) (265 hod.)3= 77912297,67 PM3
Tieto objemy vyjadrené v pikometre sú však prehnané, takže sa transformujú na jednotky Angstroms, čím sa vynásobia konverzným faktorom (1å/100pm)3:
(212,07 hod3) (1å/100pm)3= 2,1207 × 10-4 Do3
(77912297,67 PM3) (1å/100pm)3= 77 912 Á3
Rozdiely vo veľkosti medzi malým atómom H a objemným atómom CS sú teda číselne preukázané. Je potrebné vziať do úvahy, že tieto výpočty nie sú ničím iným ako aproximáciám podľa vyhlásenia, že atóm je úplne sférický, čo divá realitu.
Príklad 2

Hustota čistého zlata je 19,32 g/ml a jeho molárna hmota je 196,97 g/mol. Pri výpočte objemu móla atómov zlata sa použije nasledujúcim vzorcom:
VložkaAu= (196,97 g/mol)/(19,32 g/ml) = 10,19 ml/mol
To znamená, že 1 mol atómov zlata zaberá 10,19 ml, ale aký objem je špecificky zaberaný atóm zlata? A ako ho vyjadriť v jednotkách PM3? Za týmto účelom použite nasledujúce konverzné faktory:
(10,19 ml/mol) · (mol/6,02,10-23 atómy) · (1 m/100 cm)3· (13:00/10-12m)3= 16,92 · 106 popoludnie3
Na druhej strane, atómový polomer zlata je 166 hod. Ak sa porovnávajú oba zväzky - ten, ktorý sa získa predchádzajúcou metódou a ktorý sa vypočíta s vzorcom sférického objemu - zistí sa, že nemajú rovnakú hodnotu:
VložkaAu= (4/3) (3.14) (166 hod.)3= 19,15 · 106 popoludnie3
Ktorá z nich je bližšie k akceptovanej hodnote? Ten, ktorý je najbližšie k experimentálnym výsledkom získaným x -brehom difrakcie kryštalickej štruktúry zlata.

