Serínové charakteristiky, funkcie, metabolizmus, jedlo
- 1959
- 112
- Václav Višňovský
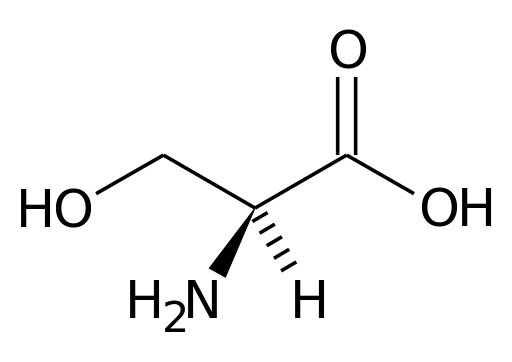
Ten Serín Je to jedna z 22 základných aminokyselín, hoci to nie je klasifikované ako základná aminokyselina pre človeka a iné zvieratá, pretože je syntetizovaná ľudským telom.
Podľa nomenklatúry s tromi lístkami je serín v literatúre opísaný ako (S v jedinom písmenovom kóde). Táto aminokyselina sa podieľa na veľkom počte metabolických trás a má polárne charakteristiky, ale nemá zaťaženie neutrálneho pH.
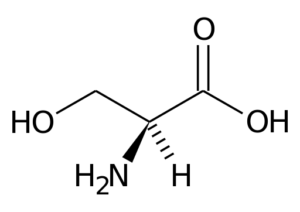 Reprezentácia série serínovej aminokyseliny (zdroj: PageZero na ňu.Wikipedia [verejná doména] cez Wikimedia Commons)
Reprezentácia série serínovej aminokyseliny (zdroj: PageZero na ňu.Wikipedia [verejná doména] cez Wikimedia Commons) Mnoho dôležitých enzýmov pre bunky má veľa.
Serín, medzi mnohými jeho funkciami, sa zúčastňuje ako predchodca a molekula lešenia v biosyntéze iných aminokyselín, ako je glycín a cysteín a je súčasťou štruktúry sfingolipidov prítomných v bunkových membránach v bunkových membránach.
Miera syntézy serínu sa líši v každom orgáne a okrem toho sa mení podľa štádia vývoja, v ktorom je jednotlivec.
Vedci navrhli, že koncentrácie L-serínu v mozgovom tkanive sa zvyšujú s vekom, pretože permeabilita bariéry krvných buniek klesá v mozgu dospelých, čo je schopné spôsobiť vážne poruchy mozgu.
Je známe, že L-serín je životne dôležitý pre biosyntézu neurotransmiterov, fosfolipidov a iných komplexných makromolekúl, pretože poskytuje prekurzory pre tieto viacnásobné metabolické dráhy.
Rôzne štúdie ukázali, že dodávka doplnkov alebo koncentrátov L-serín do určitých typov pacientov zlepšuje homeostázu glukózy, mitochondriálne funkcie a znižuje neuronálnu smrť.
[TOC]
Vlastnosti
Všetky aminokyseliny majú ako základnú štruktúru karboxylovú skupinu a aminoskupinu pripojenú k rovnakému atómu uhlíka; Tieto sa však líšia navzájom svojimi bočnými reťazcami, známymi ako skupiny R, ktoré sa môžu líšiť v ich veľkosti, štruktúre a dokonca aj v ich elektrickom náboji
Serín obsahuje tri atómy uhlíka: United Central Carbon na jednej strane do karboxylovej skupiny (COOH) a na druhej strane aminoskupina (NH3+). Ďalšie dve centrálne uhlíkové väzby sú obsadené atómom vodíka a skupinou CH2OH (skupina R), charakteristická pre serín.
Centrálny uhlík, do ktorého sú amino a karboxylové skupiny aminokyselín známe ako a uhlíkom. Ostatné atómy uhlíka skupín R sú označené písmenami gréckej abecedy.
Napríklad v prípade serínu je jediný atóm uhlíka vo svojej skupine R, ktorý je spojený so skupinou OH, známy ako uhlík y.
Môže vám slúžiť: fosfatidilserín: štruktúra, syntéza, funkcie, umiestnenieKlasifikácia
Serín je klasifikovaný v skupine polárnych aminokyselín bez zaťaženia. Členovia tejto skupiny sú veľmi rozpustné aminokyseliny vo vode, to znamená, že sú to hydrofilné zlúčeniny. V seríne a treoníne je hydrofilita spôsobená jeho schopnosťou tvoriť vodíkové mosty s vodou cez jej hydroxylové skupiny (OH).
V skupine polárnych aminokyselín bez záťaže sa cysteín, asparagín a glutamín tiež zoskupujú. Všetky z nich majú vo svojom reťazci R polárnu skupinu, táto skupina však nie je ionizovateľná a pH blízko neutrality zrušia svoje poplatky, ktoré vytvárajú zlúčeninu vo forme “Zwitteria„.
Stereochémia
Všeobecná asymetria aminokyselín robí stereochémiu týchto zlúčenín životne dôležitý v metabolických trasách, na ktorých sa zúčastňujú. V prípade serínu to možno nájsť ako d-o l-serín, ktorý je syntetizovaný výlučne bunkami nervového systému známych ako astrocyty.
A uhlíky aminokyselín sú chirálne uhlíky, pretože majú štyri rôzne United Substituents, ktoré generujú, že pre každú aminokyselinu existujú najmenej dva rozlišovacie stereoizoméry.
Stereoizomér je zrkadlový obraz molekuly, to znamená, že nemôžete prekrývať jednu na druhej. Roztoky týchto aminokyselín otáčajú polarizovanú svetelnú rovinu v opačných smeroch v opačných smeroch sú označené písmenom D o, ktoré experimentálne.
L-serín, ktorý je syntetizovaný v bunkách nervového systému. D-serín je jedným z najdôležitejších prvkov výmeny vezikúl medzi neurónmi, takže niektorí autori navrhujú, že obe izoformy serínov sú v skutočnosti esenciálnymi aminokyselinami pre neuróny pre neuróny.
Funkcia
Skupina OH serínu vo svojom reťazci R je z neho dobrý nukleofil, takže je kľúčom k aktivite mnohých enzýmov so serínom v jeho aktívnych miestach. Serín je jedným z potrebných substrátov pre syntézu NADPH a glutationic nukleotidov.
Séria L je nevyhnutná pre vývoj a správne fungovanie centrálneho nervového systému. Štúdie ukázali, že exogénny dodávka L-serínu v nízkych dávkach do hippocampusových neurónov a purkinjských buniek In vitro, Zlepšuje vaše prežitie.
Niekoľko štúdií rakovinových buniek a lymfocytov zistilo, že uhlíkové jednotky závislé od serínu sú potrebné pre nadmernú produkciu nukleotidov, ako aj pre následnú proliferáciu rakovinových buniek.
Môže vám slúžiť: Microbiota: Zloženie, funkcie a kde jeSelenocysteín je súčasťou 22 základných aminokyselín a získava sa iba ako derivát serínu. Táto aminokyselina bola pozorovaná iba u niektorých proteínov, obsahuje selén namiesto síry pripojenej k cysteínu a je syntetizovaný na základe sterifikovaného serínu.
Biosyntéza
Serín je neosenciálna aminokyselina, pretože je syntetizovaná ľudským telom. Môže sa to však asimilovať z stravy rôznych zdrojov, ako sú bielkoviny a fosfolipidy, hlavne.
Serín je syntetizovaný vo svojej forme konverziou glycínovej molekuly, reakciou sprostredkovanej hydroxymetyl-transferázovým enzýmom.
Je známe, že hlavné miesto syntézy L-serínu je v astrocytoch a nie v neurónoch. Sú to tieto bunky, syntéza sa vyskytuje fosforylačnou cestou, na ktorej sa 3-fosfoglycerát zúčastňuje, glykolytický sprostredkovateľ.
Na túto cestu pôsobia tri enzýmy: 3-fosfoglycerát dehydrogenáza, fosfoserín-transferáza a fosfoserín-fosfatáza.
Ďalšími dôležitými orgánmi, pokiaľ ide o syntézu serínu, sú pečeň, obličky, semenníky a slezina. Enzýmy, ktoré syntetizujú serín.
Jednou z prvých syntéznych trás serínu, ktorý bol známy, bola katabolická dráha zapojená do glukoneogenézy, kde L-serín sa získa ako sekundárny metabolit. Príspevok tejto trasy k výrobe telového serínu je však nízky.
Metabolizmus
V súčasnosti je známe, že serín sa dá získať z metabolizmu uhľohydrátov v pečeni, kde sa produkuje kyselina D-Glycerová, 3-fosfoglycerová kyselina a 3-fosfohydroxipirúvová kyselina. Vďaka transaminačnému procesu medzi kyselinou 3-hydroxi pyruvovou a alanín sa vyrába serín.
Pokusy s potkanmi rádioaktívne označujúce uhlík 4 glukózy, dospeli k záveru, že tento uhlík je účinne začlenený do uhlíkových kostrov serínu, čo naznačuje, že aminokyselina má prekurzor troch uhlíkov pravdepodobne z pyruvátu.
V baktériách je enzým L-serín-desamináza hlavným enzýmom, ktorý je zodpovedný za metabolizáciu serínu: prevádza L-serín na pyruvát. Je známe, že tento enzým je prítomný a aktívny v plodinách A. coli Udelenie minimálnych médií s glukózou.
Nie je známe s istotou, aká je skutočná funkcia L-serín-desaminázy v týchto mikroorganizmoch, pretože jej expresia je indukovaná mutačnými efektormi, ktoré poškodzujú DNA ultrafialovým žiarením v dôsledku prítomnosti Nalidinexico, mytomicínu a ďalších, mytomicínu a mytomicínu a iným. iní, takže z toho vyplýva, že musí mať dôležité fyziologické dôsledky.
Môže vám slúžiť: DryOpitHecus: Discovery, Charakteristika, lebka, jedloBohaté potraviny
Všetky potraviny s vysokými koncentráciami bielkovín sú bohaté na serín, hlavne vajcia, mäso a ryby. Ide však o neosentičnú aminokyselinu, takže nie je potrebné ju striktne požívať, vzhľadom na skutočnosť, že telo je schopné ju syntetizovať samo o sebe.
Niektorí ľudia trpia nezvyčajnou poruchou, pretože majú fenotyp nedostatku vzhľadom na mechanizmy syntézy serínu a glycínu, preto musia požičať koncentrované potravinové doplnky pre obe aminokyseliny.
Okrem toho komerčné značky špecializované na predaj doplnkov vitamínov (Lamberts, teraz Sport a Holomega) ponúkajú koncentráty fosfatidylserínu a L-serínu na zvýšenie výroby svalovej hmoty u vysoko konkurenčných športovcov a vzpieračov.
Súvisiace choroby
Porucha enzýmov zapojených do biosyntézy serínu môže spôsobiť vážne patológie. Znížením koncentrácie serínu v krvnej plazme a mozgovomiechovom moku môže spôsobiť hypertoniu, psychomotorické oneskorenie, mikrocefália, epilepsiu a komplexné poruchy centrálneho nervového systému.
V súčasnosti sa zistilo, že nedostatok serínu sa podieľa na vývoji diabetes mellitus, pretože L-serín je potrebný na syntézu inzulínu a jeho receptorov.
Deti, ktoré predstavujú defekty v serínovej biosyntéze, sú neurologicky abnormálne pri narodení, majú oneskorenia v vnútromaternicovom raste, vrodené mikrocefália, katarakty, záchvaty a závažné oneskorenie neurologického rozvoja.
Odkazy
- Elsila, J. A., Dworkin, J. P., Bernstein, m. P., Martin, m. P., & Sandford, s. Do. (2007). Mechanizmy tvorby aminokyselín v medzihviezdnych analógoch ľadu. The Astrophysical Journal, 660 (1), 911.
- Ichord, r. N., & Bearden, D. R. (2017). Perinatálne metabolické encefalopatie. V pediatrickej neurológii Swaiman (s. 171-177). Elsevier.
- Mothet, J. P., Rodič a. Tón., Wolosker, h., Brady, r. Ani., Linden, D. J., Ferris, C. D.,… & Snyder, s. H. (2000). D-serín je endogénny ligand pre glycínové miesto prijímača N-metyl-D-apartátu. Zborník Národnej akadémie vied, 97 (9), 4926-4931
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger princípy biochémie. Macmillan.
- Rodríguez, a. A., Ducker, G. Siež., Billingham, L. Klimatizovať., Martinez, C. Do., Mainolfi, n., Suri, v.,… & Chandel, n. Siež. (2019). Metabolizmus serínu podporuje produkciu makrofágov IL-lp. Bunkový metabolizmus, 29 (4), 1003-1011.
- Tabatabaie, l., Klomp, L. W., Berger, r., & Koning, T. J. (2010). Syntéza L-Serín v centrálnom nervovom systéme: prehľad porúch nedostatku serínu. Molekulárna genetika a metabolizmus, 99 (3), 256-262.
- « Štruktúra glyceraldehydu, charakteristiky, funkcie
- História zinku, vlastnosti, štruktúra, riziká, použitie »

