Štruktúra putresciny, vlastnosti, syntéza, použitie
- 3085
- 610
- Mgr. Pravoslav Mokroš
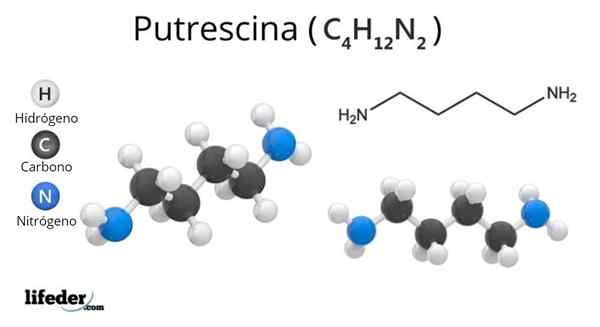
Ten Putrescina Je to organická zlúčenina, ktorej štrukturálny vzorec je NH2(Ch2)4NH2. Skladá sa z najjednoduchšieho polyamínu a je známy ako chemický názov 1.4-butanodiamín. Tento diamín udržuje úzky vzťah s mŕtvolom, 1,5-pintanodiamín.
Putrescina spolu s mŕtvolou. Odtiaľ dlhuješ svoje meno. V roku 1885 boli oba diamíny prvýkrát charakterizované nemeckým doktorom Ludwigom Briegerom.
Putrescina zasahuje priamo do syntézy spermie, iného polyamínu, keď reaguje s S-adenosylmedeínu. Spermie tiež reaguje so S-adenosylmeínom, aby sa vytvoril polyamínový spermín.
Existujú dôkazy o tom, že polyamíny, vrátane putresciny, sú potrebnými rastovými faktormi pre delenie buniek. Konštantná prívod polyamínov je predchádzajúca požiadavka na to, aby sa vyskytla proliferácia buniek.
Putrescina plní špecifickú funkciu v kožnej fyziológii a neuroprotekcii. Je syntetizovaný črevným bakteriálnym účinkom, ktorý odlišuje aminínovú aminokyselinu a produkuje ornitín. Táto aminokyselina pôsobením ornitínovej dekarboxylázy konečne pochádza z putrescínu.
[TOC]
Štruktúra Putrescina
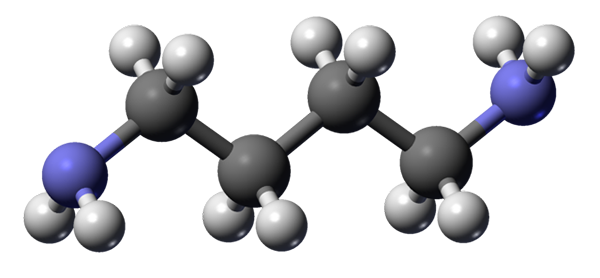
 Molekula putresciny predstavovaná modelom sfér a tyčí. Zdroj: Karlhahn / verejná doména
Molekula putresciny predstavovaná modelom sfér a tyčí. Zdroj: Karlhahn / verejná doména Horný obrázok ukazuje molekulárnu štruktúru putrescínu. Keďže je jej jednoduchá štruktúra, je ironické, že sme schopní ju rozpoznať pre svoju zápach. Sivé gule tvoria svoju uhlíkovú kostru n-bután, zatiaľ čo modrá zodpovedá atómom dusíka skupín NH2.
Tieto skupiny NH2 Môžu protonovať, čo bude pochádzať z toho, že molekula putresciny získava dve pozitívne náboje, h3N+Chvály2Chvály2Chvály2Chvály2NH3+. Preto sa stáva polycytion.
Môže vám slúžiť: 15 najdôležitejších príkladov alkoholovPutrescina je polárna molekula, ktorej intermolekulárne interakcie sú založené na dipólových depoloch a na disperzných silách v Londýne. To je dôvod, prečo je to pevný amín pri izbovej teplote a má vysoký bod varu v porovnaní s bodom iných amínov.
Putrescina vlastnosti
Molekulárna receptúra
C4H12N2
Molekulová hmotnosť
88,15 g/mol
Vzhľad
Bezfarebné kryštály, ktoré sa topia do bezfarebného oleja.
Vôňa
Silný, podobný piperidínu.
Hustota
Alebo 877 g/ml
Bod topenia
27,5 ° C
Bod varu
158,6 ° C
Koeficient priečneho októbra/vody
Log p = - 0,7
Tlak vodnej pary
2,33 mmHg pri 25 ° C
Index lom (ND)
1 455
Rozpustnosť
Veľmi rozpustný.
Pka
10,8 až 20 ° C
Rozklad
Keď sa zahrieva na rozklad, Putrescina emituje toxické plyny oxidov dusíka.
Stabilita
Nezlučiteľné so silnými oxidačnými činidlami.
Reaktivita
Vo vodnom roztoku má silné základné správanie kvôli svojim dvom skupinám aming. Putrescina reaguje s S-adenosylmedeínom za vzniku spermidínového polyamínu a nepriamo putrescín pochádza z polyamínovej spermie.
Syntéza
Putrescín sa vyrába priemyselne hydrogenáciou sukinonitrilovej chemickej zlúčeniny, ktorá je produkovaná reakciou kyanidu vodíka s acrilonitrilom.
Putrescina sa pomocou biotechnológie syntetizuje v prostriedkoch kultivácie určitých kmeňov baktérií a. coli.
Gram negatívne baktérie môžu syntetizovať putrescinu tromi spôsobmi:
-Ornitine sa generuje z arginínovej aminokyseliny. Potom ornitín v dôsledku pôsobenia enzýmu ornitín Discarboxylázy syntetizuje putrescinu
-Arginín pôsobením arginínu Discarboxylázy syntetizuje agmantín. Následne amantín pochádza z putresciny
-Tretím spôsobom sa Agmatina priamo transformuje na putrescinu a močovinu pôsobením enzýmu agmatinosa.
Môže vám slúžiť: Granataria Rovnováha: Charakteristiky, časti a ako ich používaťGram pozitívne baktérie používajú iné cesty na syntézu putrescínu.
Putrescina používa
Priemyselný
Americká spoločnosť DuPont pôvodne komercializovala nylon 6.6. Toto sa vyznačovalo 6 -karbonovým diamínom a 6 -karbónmi, ktoré boli rozptýlené v polymérnej štruktúre. V roku 1990 holandská spoločnosť predstavila na trhu Nylon 4.6.
Nylon 4.6 bol uvedený na trh s názvom Stanyl, ktorý používa putrescinu, ktorá pozostáva zo 4 atómov uhlíka ako diamín, čím sa zachovávalo rovnaké deaccid ako v nylone 6,6.
Stanyl sa používa v sprievodcoch motorov a prevodových vlakov, predstavuje dobrú odolnosť proti opotrebeniu a trecie pôsobenie, najmä pri vysokých teplotách.
Produkcia drog
Dekarboxylácia putrescínu je počiatočný krok sekvencie biochemických udalostí, ktoré vedú k syntéze skopolamínu: vysoko toxický liek, ktorého vysoké dávky môžu spôsobiť smrť. Scopolamín (Burrundanga) sa často používa pri trestných činoch.
Escopolamín sa používa vo veľmi nízkych dávkach pri liečbe vozidlach, nevoľnosti, zvracania a kolitídy.
Enzým Putrescina-N-metyltransferáza (PMT) pôsobí na putrescín v biochemickom procese sprostredkovanom S-adeenosylmedeínu, ktorý vedie k syntéze nikotínu, tropanu a v Nortropan alkaloid.
Nikotín je toxický liek, ktorý sa používa ako poľnohospodársky insekticíd, zatiaľ čo u veterinárnych lekárov sa používa ako vonkajší antiparazitický.
Biologické pôsobenie
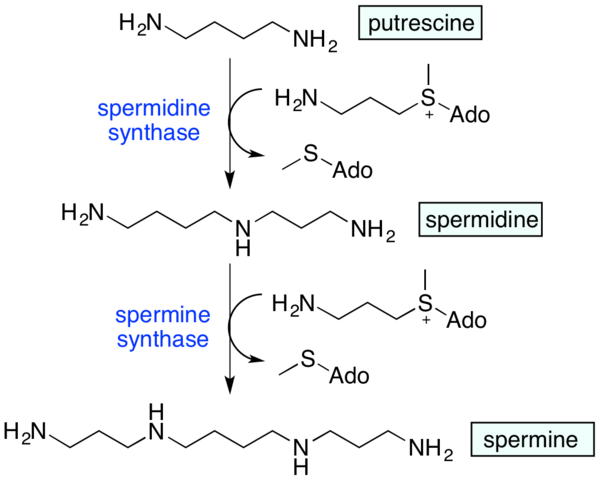 Biosyntéza spermií a spermií z Putresciny. ADO = 5'-adenyl. Zdroj: Andrew Murkin/CC By-S (https: // creativeCommons.Org/licencie/By-SA/4.0)
Biosyntéza spermií a spermií z Putresciny. ADO = 5'-adenyl. Zdroj: Andrew Murkin/CC By-S (https: // creativeCommons.Org/licencie/By-SA/4.0) Putrescina, rovnako ako iné polyamíny, ako je korporeín, spermie a spermie, sú polycytické molekuly v dôsledku prítomnosti amingových skupín. Preto môžu s elektrostaticky interagovať s nukleovými kyselinami, fosfolipidmi a proteínmi s negatívnym zaťažením.
Môže vám slúžiť: pycnometerTáto interakcia umožňuje pôsobenie polyamínov v mnohých biochemických udalostiach, napríklad:
-Regulácia DNA a syntéza proteínov
-Eliminácia reaktívnych druhov kyslíka
-Aktivácia proliferácie buniek
-Diferenciácia a vývoj tkanív
Medzi bunkové funkcie, v ktorých zasahujú polyamíny, patrí dozrievanie črevnej sliznice a migrácie buniek. Putrescina hrá špecifickú úlohu pri kožnej fyziológii a neuroprotekcii.
Aj keď početné biologické funkcie súvisia aj s tvorbou rakoviny s polyamínmi. Enzým ornitín dekarboxyláza, enzým, ktorý katalyzuje konverziu ornitínu na putrescín, je prítomný v rôznych typoch ľudskej rakoviny a hlodavcov.
Zvýšenie koncentrácie polyamínov priamo súvisí so súborom bunkových procesov súvisiacich s inváziou nádoru a metastázami. Okrem toho sa zdôrazňuje, že putrescina môže byť predchodcom N-nitrosamínu, karcinogénneho činidla.
Toxicita
Putrescín má nízku toxicitu, ale je schopný pôsobiť podporovaním toxického účinku histamínu, ktorý sa vytvára pri rozkladu mäsa, ako aj účinnosť tiramínu generovaného v syre.
Odkazy
- Morrison, r. Tón. a Boyd, R, N. (1987). Organická chémia. 5. vydanie. Redakčný Addison-Wesley Inter-American.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. (10. vydanie.). Wiley Plus.
- Národné centrum pre biotechnologické informácie. (2020). Húžecňa. Databáza pubchem. CID = 1045. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Wikipedia. (2020). Húžecňa. Zdroj: In.Wikipedia.orgán
- Elsevier B.Vložka. (2020). Húžecňa. Vedecký. Zdroj: ScienceDirect.com
- Phillip Broadwith. (15. februára 2011). Húžecňa. Chémia vo svojich prvkoch. Získané z: Chemistryworld.com
- Drogová banka.Ac. (13. júna 2005). Húžecňa. Získané z: drogankank.Ac

