Trojitý bod
- 3975
- 1226
- MUDr. Miloslav Habšuda
Čo je trojitý bod?
On Trojitý bod Je to termín v oblasti termodynamiky, ktorý sa týka teploty a tlaku, v ktorom sú súčasne tri fázy látky v termodynamickom rovnovážnom stave. Tento bod existuje pre všetky látky, hoci podmienky, v ktorých sa dosahujú.
Triple Point môže zahŕňať aj viac ako jednu fázu toho istého typu pre špecifickú látku; to znamená, že sú pozorované dve rôzne pevné, tekuté alebo plynové fázy. Hélium, najmä jeho izotop Helio-4, je dobrým príkladom trojitého bodu zahŕňajúceho dve individuálne fázy tekutín: normálna a zbytočná tekutina.
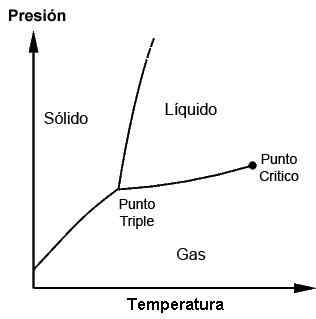
 Fázový diagram ukazujúci trojitý bod a kritický bod
Fázový diagram ukazujúci trojitý bod a kritický bod Na čo je to a kedy sa použije trojitý bod?
Trojitý bod vody sa používa na definovanie Kelvinu, termodynamickej teplotnej základnej jednotky v medzinárodnom systéme jednotiek (SI). Táto hodnota je nastavená podľa definície namiesto miery.
Triple body každej látky sa dajú pozorovať pomocou fázových diagramov, ktoré sú vynesené grafy, ktoré umožňujú demonštrovať obmedzujúce podmienky tuhých, kvapalných, plynných fáz (a ďalšie v osobitných prípadoch) teplota, tlak a/alebo rozpustnosť.
Látka sa nachádza v jeho bode topenia, v ktorom tuhá látka spĺňa tekutinu; Nachádza sa tiež v jeho bode varu, v ktorom tekutina spĺňa plyn. Je to však v trojnásobnom bode, kde sa dosiahnu tri fázy. Tieto diagramy sa budú líšiť pre každú látku, ako bude vidieť neskôr.
Môže vám slúžiť: API Gravity: Stupnica a klasifikácia surovejTriple Point sa môže efektívne použiť pri kalibrácii teplomerov pomocou trojitých bodových buniek.
Toto sú vzorky látok v izolovaných podmienkach (v rámci „buniek“ skla), ktoré sú na svojom trojnásobnom bode so známymi podmienkami teploty a tlaku, a tak uľahčujú štúdium presnosti meraní teplomerov.
Štúdium tohto konceptu pri skúmaní planéty Mars sa tiež použilo, v ktorej sa pokus o hladinu mora počas misií, ktoré sa uskutočnili v 70. rokoch 20. storočia.
Trojitá voda
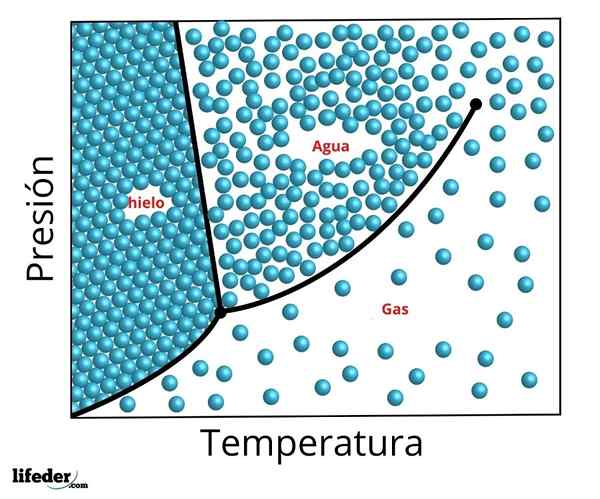 Fázový diagram trojitého bodu vody. Triple Bod je dolný bod a kritik horný bod
Fázový diagram trojitého bodu vody. Triple Bod je dolný bod a kritik horný bod Presné podmienky tlaku a teploty, pri ktorej voda koexistuje vo svojich troch fázach v rovnovážnej - kvapalnej vode, ľade a para - sa vyskytujú pri teplote presne 273,16 K (0,01 ° C) a čiastočný tlak pary pary 611 656 Pascalov (0,00603659 atm. ).
V tomto bode je možné premeniť látku na ktorúkoľvek z troch fáz s minimálnymi zmenami jej teploty alebo tlaku. Aj keď by celkový tlak systému mohol byť umiestnený nad tlakom potrebným pre trojnásobný bod, ak je čiastočný tlak pary na 611 656 Pa, systém dosiahne trojitý bod rovnakým spôsobom.
Na predchádzajúcom obrázku je možné pozorovať reprezentáciu trojitého bodu (alebo Trojitý bod, v angličtine) látky, ktorej diagram je podobný ako pri vode, podľa teploty a tlaku potrebného na dosiahnutie tejto hodnoty.
V prípade vody tento bod zodpovedá minimálnemu tlaku, pri ktorom môže existovať kvapalná voda. Na tlak na tento trojitý bod (napríklad vo vákuu) a keď sa používa konštantné tlakové zahrievanie, pevný ľad sa prevedie priamo na vodnú paru bez toho, aby prešiel kvapalinou; Toto je proces nazývaný sublimácia.
Môže vám slúžiť: Teória veľkého tresku: Charakteristiky, fázy, dôkazy, problémyNad tento minimálny tlak (PTp), ľad sa najprv roztopí, aby vytvoril tekutú vodu, a iba tam sa odparí alebo sa vrie na vytvorenie pary.
Pre mnoho látok je teplotná hodnota v trojnásobnom bode minimálna teplota, pri ktorej môže existovať kvapalná fáza, ale v prípade vody sa to nedeje. Pre vodu sa tak nestane, pretože bod topenia ľadu klesá na základe tlaku, ako je znázornené na zelenej bodkovanej čiare predchádzajúceho obrázku.
Vo fázach s vysokým tlakom má voda pomerne komplexný fázový diagram, ktorý vykazuje pätnásť známych fáz ľadu (pri rôznych teplotách a tlakoch), okrem desiatich rôznych trojitých bodov, ktoré sú zobrazené na nasledujúcom obrázku:
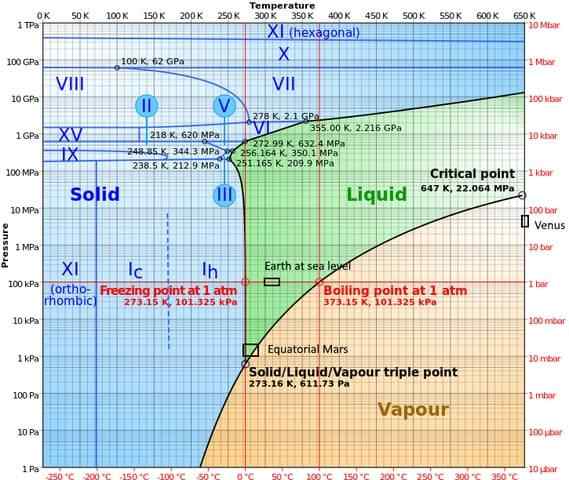
Je možné poznamenať, že v podmienkach vysokého tlaku môže ľad existovať v rovnováhe s kvapalinou; Diagram ukazuje, že body zlúčenia sa zvyšujú tlakom. Pri nízkych konštantných teplotách a zvyšujúcom sa tlaku sa para môže transformovať priamo na ľad bez toho, aby prešla kvapalnou fázou.
Rôzne podmienky, ktoré sa vyskytujú na planétach, kde sú v tomto diagrame znázornené aj trojitý bod (pozemok na mori a v rovníkovej oblasti Mars)).
Diagram objasňuje, že trojitý bod sa líši v závislosti od miesta z dôvodu tlaku a atmosférickej teploty, a to nielen intervenčným zásahom experimentátora.
Trojitý bod cyklohexánu
Cyklohexan je cyklokanom, ktorý má molekulárny vzorec C6H12. Táto látka má zvláštnosť, že má trojnásobné podmienky, ktoré sa dajú ľahko reprodukovať, ako v prípade vody, pretože tento bod sa nachádza pri teplote 279,47 K a tlaku 5 388 kPa.
Môže vám slúžiť: Live Poplatky: Koncept, charakteristiky, príkladyZa týchto podmienok bola pozorovaná hirarová zlúčenina, tuhosť a topenie s minimálnymi zmenami teploty a tlaku.
Trojitý benzén
V prípade podobného cyklohexanu, benzénu (organická zlúčenina s chemickým vzorcom C6H6) má ľahko reprodukovateľné trojité podmienky v laboratóriu.
Jeho hodnoty sú 278,5 K a 4,83 kPa, takže experimentovanie s touto úrovňou začiatočníkov je tiež bežné.
Odkazy
- Wikipedia. (s.F.). Wikipedia. Získané z in.Wikipedia.orgán
- Britannica, e. (1998). Encyclopedia Britannica. Získané od Britannica.com
- Sila n. (s.F.). Jadrový. Získané z jadrovej energie.slepo
- Wagner, w., Saul, a., & Prub,. (1992). Medzinárodné rovnice tlaku pozdĺž topenia a pozdĺž sublimačnej krivky bežnej vody. Buchtán.
- Penoncello, s. G., Jacobsen, R. Tón., & Goodwin, a. R. (Devätnásť deväťdesiatpäť). Do formulácie termodynamickej vlastnosti pre cyklohexán.

