Štruktúra dusičnanu sodného (Nano3), vlastnosti, použitie, riziká

- 1203
- 315
- Tomáš Mydlo
On dusičnan sodný Je to kryštalická anorganická tuhá látka tvorená sodíkovým iónom+ a dusičnanový ión nie3-. Jeho chemický vzorec je nano3. V prírode sa nachádza ako minerál nitratíny alebo nitratitu, ktorý je v Atacama v Čile hojný.
Dusičnan sodný je nekompromisná tuhá látka, ale môže urýchliť oxidáciu alebo spaľovanie horľavých materiálov. Z tohto dôvodu má široké využitie v ohňostrojoch, výbušninách, v zápasoch, v uhoľných tehlách a niektorých druhoch pesticídov, aby sa eliminovali hlodavce a iné malé cicavce.
 Nitratína alebo nitratita, minerál dusičnan s sodným3. John Sobolewski (JSS) [CC po 3.0 (https: // creativeCommons.Org/licencie/o/3.0)]. Zdroj: Wikimedia Commons.
Nitratína alebo nitratita, minerál dusičnan s sodným3. John Sobolewski (JSS) [CC po 3.0 (https: // creativeCommons.Org/licencie/o/3.0)]. Zdroj: Wikimedia Commons. Schopnosť uprednostňovať spaľovanie alebo zapaľovanie iných materiálov znamená, že s ním musí byť manipulovaná s veľkou opatrnosťou. Ak je vystavený plameňom alebo požiarom, môže sa využiť. Napriek tomu nano3 Používa sa v potravinárskom priemysle, pretože má konzervačné vlastnosti, najmä mäso a niektoré druhy syrov.
Ich nadmerné požitie však môže spôsobiť zdravotné problémy, najmä u tehotných žien, detí a detí. Pri transformácii na nitrity v tráviacom systéme môže spôsobiť určité choroby.
[TOC]
Chemická štruktúra
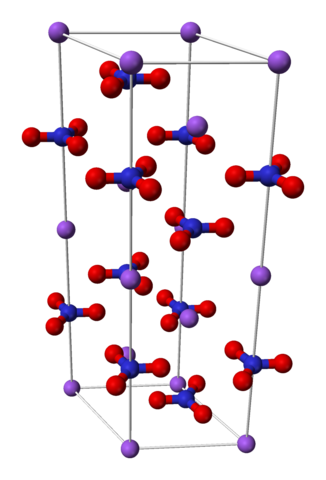 Nano3 Romboédrica Unitary Cell. Zdroj: Benjah-Bmm27 [verejná doména]
Nano3 Romboédrica Unitary Cell. Zdroj: Benjah-Bmm27 [verejná doména] Dusičnan sodný sa skladá z katiónu sodného+ a nitrátový anión č3-.
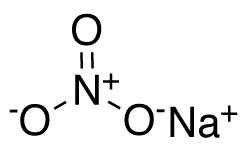 Dusičnan sodný3. Ccroberts [verejná doména]. Zdroj: Wikimedia Commons.
Dusičnan sodný3. Ccroberts [verejná doména]. Zdroj: Wikimedia Commons. V dusičnanom aninii č3- Dusík N má valenciu +5 a kyslíkom a valenciou -2. Z tohto dôvodu má dusičnanový anión negatívne zaťaženie.
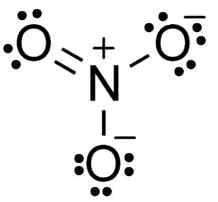 Štruktúra dusičnanu. TEM5PSU [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)]. Zdroj: Wikimedia Commons.
Štruktúra dusičnanu. TEM5PSU [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)]. Zdroj: Wikimedia Commons. Anión nie3- Má plochú a symetrickú štruktúru, v ktorej tri kyslíky distribuujú negatívny alebo jednotný spôsob.
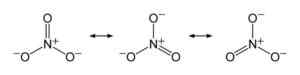 V dusičnanovom ióne je záporné zaťaženie rozdelené rovnako medzi tri atómy kyslíka. Benjah-Bmm27 [verejná doména]. Zdroj: Wikimedia Commons.
V dusičnanovom ióne je záporné zaťaženie rozdelené rovnako medzi tri atómy kyslíka. Benjah-Bmm27 [verejná doména]. Zdroj: Wikimedia Commons. Menovanie
-Dusičnan sodný
-Dusičnan sodný
-Sodný soľný Sodný soľ)
-Nitro sóda (angličtina Sóda)
-Saliter de Chile
-Čílsky dusičnan
-Dusičnan
-Nitratita
-Kalich
Vlastnosti
 Romboédické kryštály dusičnanu sodného získané z jeho presýteného roztoku. Zdroj: Vadim Sedov [CC po 4.0 (https: // creativeCommons.Org/licencie/o/4.0)]
Romboédické kryštály dusičnanu sodného získané z jeho presýteného roztoku. Zdroj: Vadim Sedov [CC po 4.0 (https: // creativeCommons.Org/licencie/o/4.0)] Fyzický stav
Farba bezfarebná až biela, trigonálna alebo rhomboedicínska kryštály.
Molekulová hmotnosť
84,995 g/mol
Bod topenia
308 ° C
Bod varu
380 ° C (rozkladá sa).
Hustota
2,257 g/cm3 pri 20 ° C.
Rozpustnosť
Vodné rozpustné: 91,2 g/100 g vody pri 25 ° C alebo 1 g v 1,1 ml vody. Mierne rozpustný v etanole a metanole.
pH
Roztoky dusičnanu sodného sú neutrálne, to znamená ani kyselina, ani základné, preto je jeho pH 7.
Ďalšie vlastnosti
Je to hygroskopická tuhá látka, to znamená, že absorbuje vodu z prostredia.
 Dusičnan sodný3 tuhý. Ondřej Mangl [verejná doména]. Zdroj: Wikimedia Commons.
Dusičnan sodný3 tuhý. Ondřej Mangl [verejná doména]. Zdroj: Wikimedia Commons. Jeho rozpustenie vody spôsobuje ochladenie roztoku, takže sa hovorí, že tento proces rozpustenia je endotermický, inými slovami, keď rozpustí, absorbuje teplo z prostredia, a preto sa roztok ochladzuje.
Môže vám slúžiť: Primárny uhlík: Charakteristiky, typy a príkladyPri veľmi nízkych teplotách je dusičnan sodný rozpustný v kvapalnom NH amoniaku3, formovanie nano3· 4nh3 Pod -42 ° C.
Nano3 Nie je to palivo, ale jeho prítomnosť urýchľuje spaľovanie materiálov alebo zlúčenín, ktoré sú. Je to preto, že keď je zahrievaný, kyslík alebo2, medzi inými plynmi.
Získanie
Získava sa hlavne extrakciou minerálnych usadenín alebo baní Salitra de Chile (Caliche alebo Nitratita). Na tento účel sa používa soľanka a potom sa vykonáva kryštalizácia a rekryštalizácia na získanie nano kryštálov3 najčistejší.
Tieto bane sú hlavne v Južnej Amerike v severnom Čile v púšti Atacama. Je spojený s dusičnanom draselným Kno3 a rozkladom organických látok.
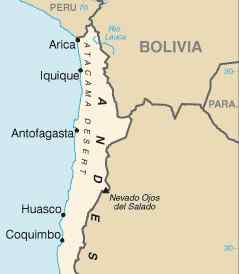 Poloha púšte Atacama v severnom Čile, kde sú dôležité ložiská dusičnanu sodného. CIA [verejná doména]. Zdroj: Wikimedia Commons.
Poloha púšte Atacama v severnom Čile, kde sú dôležité ložiská dusičnanu sodného. CIA [verejná doména]. Zdroj: Wikimedia Commons. Môže sa tiež získať reakciou kyseliny dusičnej s uhličitanom sodným Na2Co3 alebo s hydroxidom sodným NaOH:
2 hno3 + Nat2Co3 → 2 nano3 + Co2↑ + h2Ani
Prítomnosť v ľudskom organizme
Dusičnan sodný môže vstúpiť do ľudského organizmu prostredníctvom potravín a pitia vody, ktorá ho obsahuje.
60-80% požitého dusičnanu pochádza z ovocia a zeleniny. Druhým zdrojom sú vyliečené mäso. Odvetvie mäsa ho používa na zabránenie rastu mikróbov a na udržanie farby.
Vysoký podiel dusičnanu prítomného v ľudskom tele však pochádza z jeho endogénnej syntézy alebo v dôsledku procesov v rámci organizmu.
Žiadosti
V potravinárskom priemysle
Používa sa ako konzervačný stav potravín, ako vytvrdzovacie činidlo pre nakladané mäso a ako farebné retenčné činidlo pre mäso. Potraviny, ktoré ju môžu obsahovať, sú slanina, párky, šunka a niektoré syry.
 Vyliečené mäso, ktoré pravdepodobne obsahuje dusičnan sodný. Autor: Falco. Zdroj: Pixabay.
Vyliečené mäso, ktoré pravdepodobne obsahuje dusičnan sodný. Autor: Falco. Zdroj: Pixabay. V hnojivách
Dusičnan sodný sa používa v zmesiach hnojív, na oplodnenie tabaku, bavlny a rastlinných plodín.
 Traktor oplodnenie plantáže. Autor: Franck Barske. Zdroj: Pixabay.
Traktor oplodnenie plantáže. Autor: Franck Barske. Zdroj: Pixabay. Ako promótor alebo lichotenie spaľovania alebo výbuchu
Nano3 Používa sa ako oxidant v mnohých aplikáciách. Je to solídny kyslík bohatý na kyslík, ktorý uľahčuje proces zapaľovania prostredníctvom výroby alebo2.
Prítomnosť nano3 robí materiály nevyžaduje kyslík z vonkajších zdrojov, aby sa zapálil, pretože to dodáva dostatočné alebo2 Pokiaľ ide o exotermické reakcie s vlastným spôsobom (tepelné generátory), ktoré sa vyskytujú počas zápalu alebo výbuchu.
Používa sa už dlho ako hlavný oxidant v pyrotechnických materiáloch (ohňostroj), ako oxidačná zložka vo výbušninách a detonačných látkach alebo výbuchoch a ako činidlo hnacieho látky.
Môže vám slúžiť: chemická zlúčenina Ohňostroj. Vo svojom zložení je dusičnan nano sodný3. Autor: Woysplaid. Zdroj: Pixabay.
Ohňostroj. Vo svojom zložení je dusičnan nano sodný3. Autor: Woysplaid. Zdroj: Pixabay. Používa sa tiež na zlepšenie spaľovania uhoľných tehál (brikety), na uprednostňovanie zapaľovania v zápasoch a dokonca na zlepšenie horľavých vlastností tabaku.
Na odstránenie hlodavcov a iných cicavcov
Používa sa na špeciálny typ pesticídov. Zloženia, ktoré ho obsahujú.
Z tohto dôvodu sa používa na kontrolu niekoľkých hlodavcov, marmotes, kojotov a kojkov, na otvorených poliach, trávnych porastoch, nekultivovaných oblastiach, céspedes a golfových poliach.
Pri príprave iných zlúčenín
Používa sa v HNO na výrobu kyseliny dusičnej3, Dusitan sodný2, a tiež pôsobí ako katalyzátor pri príprave kyseliny sírovej H2SW4.
Používa sa vo výrobe oxidu dusného2O a ako oxidačné činidlo pri výrobe farmaceutických zlúčenín.
Pri extrakcii kovov elektronického odpadu
Niektorí vedci zistili, že nano3 Uľahčuje nejednotnú extrakciu kovov obsiahnutých v elektronických zariadeniach (mobilné telefóny, tablety, počítače atď.).
Užitočné kovy, ktoré sa môžu extrahovať z komponentov týchto elektronických zariadení, sú Nickel Ni, Cobalt Co, mangán Mn, zinok Zn, Copper Cu a hliník.
Extrakcia sa vykonáva iba pomocou jedného nano roztoku3 a polymér. A dosiahne sa výťažok 60%.
Týmto spôsobom je možné recyklovať elektronický odpad, ktorý prispieva k minimalizácii odpadu a stabilnému zotaveniu zdrojov.
Vo výskume zdravia a cvičenia
Podľa niektorých štúdií požitie doplnkov nano3 alebo potraviny, ktoré ho obsahujú prirodzene, majú pozitívne účinky na zdravie. Niektoré z potravín bohatých na dusičnany sú repa, špenát a rukola.
Medzi účinkami patrí zlepšenie kardiovaskulárneho systému, zníženie krvného tlaku, zlepšenie prietoku krvi a zvýšenie množstva kyslíka v tkanivách, ktoré sa fyzicky cvičia.
To naznačuje, že by sa mohlo zvážiť použitie nano3 Ako lacný liek na prevenciu a liečbu pacientov s problémami s krvným tlakom.
Okrem toho môže slúžiť ako efektívna a prirodzená pomoc pri zvyšovaní svalovej energie u športovcov.
Na niekoľkých použitiach
 Reklamný plagát dvadsiateho storočia, ktorý vyvoláva zaplatenie pôdy dusičnanom Čile. David Perez [verejná doména]. Zdroj: Wikimedia Commons.
Reklamný plagát dvadsiateho storočia, ktorý vyvoláva zaplatenie pôdy dusičnanom Čile. David Perez [verejná doména]. Zdroj: Wikimedia Commons. Používa sa ako oxidačné a zakladateľské činidlo pri výrobe okuliarov a smaltov na keramiku. Používa sa tiež v špeciálnych cementoch.
Slúži ako chemické činidlo pri regenerácii cínu z nezdravého kovu, v latexovej koagulácii, v jadrovom priemysle a pri kontrole korózie vo vodných systémoch.
Môže vám slúžiť: Disposio: Štruktúra, vlastnosti, získanie, použitieRiziká
Nebezpečenstvo jeho manipulácie
Má vlastnosť zrýchlenia spaľovania horľavých materiálov. Ak ste zapojení do požiaru, môže dôjsť k výbuchu.
Pri vystavení tepla alebo požiaru je možné využiť, produkujúce toxické oxidy dusíka.
Problémy súvisiace s vaším požitím s potravinami alebo vodou
Dusičnan pri požití sa môže stať dusitanom v ústach, ako aj v žalúdku a črevách.
Dusičnan pri reakcii s amínmi prítomnými v niektorých potravinách sa môže stať nitrozamínom v kyslom médiu ako v žalúdku. Nitrosamín je karcinogénny.
To sa však nestane, keď sa ovocie a zelenina obsahujú dusičnany prirodzene ingutované.
Podľa niektorých štúdií môže prítomnosť vysokých hladín dusičnanov spôsobiť poruchu krvi, ktorá spôsobí účinné uvoľňovanie kyslíka v tkanivách.
Môže sa to vyskytnúť u detí, ktorých mlieka.
Zistilo sa tiež, že vysoké hladiny dusičnanu môžu spôsobiť problémy s tehotenstvom detí, čo spôsobuje spontánne potraty, predčasné pôrody alebo defekty v nervovej trubici plodu.
Nedávno sa zistilo, že dusičnan sodný môže znamenať riziko rozvoja muskuloskeletálneho systému a u ľudí je ovplyvnená komunikácia s nervami-multi-muscle.
Dusičnan sodný v potravinách
 Dusičnan sodný sa nachádza ako aditívny v slanine a iných mäsových výrobkoch. Zdroj: Cookbookman17 Via Flickr (https: // www.Flickr.com/photos/[e -mail chráni]/6175755733)
Dusičnan sodný sa nachádza ako aditívny v slanine a iných mäsových výrobkoch. Zdroj: Cookbookman17 Via Flickr (https: // www.Flickr.com/photos/[e -mail chráni]/6175755733) Dusičnan sodný je synonymom mäsa, pretože spolu s dusitanom sa k nim pridávajú s cieľom ich zachovať a zlepšiť ich vzhľad a príchute. Pre svoju príčinu, nadmerná spotreba mäsa (perrokalientes, slanina, šunky, údené ryby atď.) bol zapojený do rušivého spojenia rakoviny v celom tráviacom systéme.
Zatiaľ čo vzťah medzi mäsom ošetreným solimi dusičnanom a rakovinou nie je absolútny, odporúča sa zmierniť jeho príjem.
Na druhej strane zelenina (mrkva, repa, reďkovka, šalát, špenát atď.) Sú bohatí na nano3 Pretože ju absorbovali z kultivačných pôd kvôli svojej akcii hnojiva. Príjem tejto zeleniny, v rozpore s výrobkami na mäso, nie je spojený s citovanými chorobami.
Je to z dvoch dôvodov: rozdiel v hladinách bielkovín takýchto potravín a spôsob, akým varí. Mäso pri vyprážaní alebo zahrievaní na plameň podporuje reakciu medzi dusičnanmi-dusičnanmi s určitými skupinami aminokyselín na výrobu nitrosoamínov: skutočné karcinogénne činidlá.
Obsah vitamínu C, vlákniny a polyfenolov v zelenine znižuje tvorbu týchto nitrosoamínov. Preto nano3 Samotné to nie je hrozba pre jedlo.
Odkazy
- Alebo.Siež. Lekárska knižnica. (2019). Dusičnan sodný. Získané z: pubchem.Ncbi.NLM.NIH.Vláda.
- Ullmannova encyklopédia priemyselnej chémie. (1990). Piaty vydanie. VCH Verlagsgellschaft MBH.
- Pouretal, h.R. a Ravanbod, m. (2015). Kinetická štúdia mg/nano3 Pyrotechnic s použitím techniky neoseathermálnej TG/DSC. J Term Anal Calim (2015) 119: 2281-2288. Odkaz obnovený.Prubár.com.
- Jarosz, J. a kol. (2016). Dusičnan sodný znižuje agrín indukovaný receptor acetylcholínu. Farmakológia a toxikológia BMC (2016) 17:20. Zdroj z BMCpharmacoloLoxicol.biomedcentrálny.com.
- Bavlna, f. Albert a Wilkinson, Geoffrey. (1980). Pokročilá anorganická chémia. Štvrté vydanie. John Wiley & Sons.
- Prival, m.J. (2003). Rakovina. Carcinagens v potravinovom reťazci. V encyklopédii potravinových vied a výživy (druhé vydanie). Zotavené z vedeckých pracovníkov.com.
- Zakhodyaeva a.Do. a kol. (2019). Komplexná extrakcia kovov vo vodnom dvojfázovom systéme založenom na poly (etylénoxid) 1500 a dusičnan sodný. Molekuly 2019, 24, 4078. MDPI sa zotavila.com.
- Clements, W.Tón. a kol. (2014). Požitie dusičnanov: prehľad účinkov zdravia a fyzickej výkonnosti. Výživy 2014, 6, 5224-5264. MDPI sa zotavila.com.

