Dusičnan vápenatý (Ca (NO3) 2)

- 4755
- 1094
- Mgr. Pravoslav Mokroš
On dusičnan vápenatý Je to terciárna anorganická soľ, ktorej chemický vzorec je CA (nie3)2. Z jeho vzorca je známe, že jeho pevná látka sa skladá z iónov CA2+ a nie3- V pomere 1: 2. Preto je to zlúčenina čisto iónovej povahy.
Jednou z jeho vlastností je jeho oxidačný charakter, podľa anirácie dusičnanu. Nie je to palivo, to znamená, že nespáli pri vysokých teplotách. Keďže nie je -predstavuje bezpečnú pevnú manipuláciu s ňou bez veľkej starostlivosti; Môže však urýchliť zapálenie horľavých materiálov.
 Dusičnan vápenatko. Zdroj: Ondřej Manggl [verejná doména], z Wikimedia Commons
Dusičnan vápenatko. Zdroj: Ondřej Manggl [verejná doména], z Wikimedia Commons Jeho vzhľad pozostáva z granulovanej pevnej látky, ktorá predstavuje svetlú bielu alebo šedú farbu (vynikajúci obraz). Môže to byť bezvodý alebo tetrahydrát, CA (nie3)24H2Ani. Je veľmi rozpustný vo vode, metanole a acetóne.
Dusičnan vápenatého sa široko používa ako hnojivo, pretože sa ľahko pohybuje vo vlhkej pôde a je rýchlo absorbovaný koreňmi rastlín. Dodáva dva dôležité prvky pre výživu a rast rastlín: dusík a vápnik.
Dusík je jedným z troch základných prvkov pre vývoj rastlín (N, P a K), je nevyhnutný v syntéze proteínov. Medzitým je potrebný vápnik na udržanie štruktúry bunkovej steny rastlín. Z tohto dôvodu CA (nie3)2 Záhrady sú veľmi predurčené.
Na druhej strane táto soľ má toxické účinky, najmä priamym kontaktom s pokožkou a očami, ako aj vdýchnutím jej prachu. Okrem toho sa dá rozpadať otepľovaním.
Štruktúra dusičnanu vápenatého
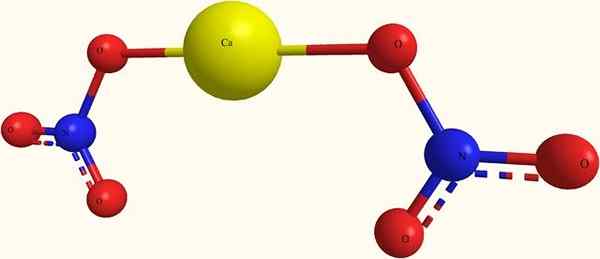 Vápenaté ióny. Zdroj: я.Valcnox na ru.Wikipedia [verejná doména], z Wikimedia Commons
Vápenaté ióny. Zdroj: я.Valcnox na ru.Wikipedia [verejná doména], z Wikimedia Commons Na hornom obrázku štruktúra CA (nie3)2 V modeli guľôčok a tyčí. Tu však existuje defekt: predpokladá sa existencia kovalentných dlhopisov CA-O, čo je v rozpore s jeho iónovým charakterom. Objasňujúc to, interakcie sú skutočne elektrostatického typu.
Katión CA2+ Je obklopený dvoma aniónmi nie3- Podľa jeho rozmerov v skle. Dusík vo forme dusičnanu v kryštalickej štruktúre prevláda.
Ióny sú zoskupené tak, aby stanovili konfiguráciu, ktorej minimálnym výrazom je jednotná bunka; čo je pre bezvodú soľ. To znamená, z kociek obsahujúcich pomer 1: 2 pre tieto ióny sa celé sklo reprodukuje.
Môže vám slúžiť: Tin: Štruktúra, vlastnosti, získanie, použitiaNa druhej strane, tetrahydrátová soľ, CA (nie3)24H2Alebo má pre každú sadu štyri molekuly vody3- Ac2+ Nie3-. Tým sa modifikuje kryštalická štruktúra a deformuje ju v jednotnej monoklinickej bunke.
Preto sú kryštály pre obe soli, bezvodé a tetrahydráty, sú odlišné; Rozdiely, ktoré je možné určiť vo svojich fyzikálnych vlastnostiach, napríklad v bodoch fúzie.
Fyzikálne a chemické vlastnosti
Chemické názvy
-Dusičnan vápenatý
-Vápnikový dinitrát
-Nitrokalcita
-Nórsky sat a limeltpettro.
Molekulárna receptúra
Výtok3)2 alebo môže2Ani6
Molekulová hmotnosť
Anhidro 164 088 g/mol a tetrahydrát 236,15 g/mol. Všimnite si vplyv vody na molekulovú hmotnosť a nemožno ho opovrhovať pri výrobe jej ťažkej.
Fyzický vzhľad
Pevné alebo svetlo šedé granule. Kubické biele kryštály alebo chutné granule; to znamená, že absorbujú vlhkosť do tej miery, že rozpúšťajú produkt svojej vysokej rozpustnosti.
Bod varu
Bezčka sa rozkladá zahrievaním pri teplote, ktorá zabraňuje stanoveniu bodu varu; Zatiaľ čo forma soli tetrahydrátov má bod varu 132 ° C (270 ° F, 405 K).
Bod topenia
-Forma anhydra: 561 ° C až 760 mmHg (1042 ° F, 834 K).
-Tetrahydrátová forma: 42,7 ° C (109 ° F, 316 K).
To ukazuje, ako molekuly vody interferujú s elektrostatickými interakciami medzi CA2+ a nie3- vo vnútri kryštálov; A preto sa tuhá látka topí pri oveľa nižšej teplote.
Rozpustnosť
-Forma anhydra: 1212 g/l pri 20 ° C.
-Tetrahydrátová forma: 1290 g/l pri 20 ° C.
Voda v kryštáloch sotva zvyšuje rozpustnosť soli.
Rozpustnosť v organických rozpúšťadlách
-V etanole, 51,42 g/100 g pri 20 ° C.
-V metanolu, 134 g/100 g pri 10 ° C.
-V acetone, 168 g/100 g pri 20 ° C.
Kyslosť (PKA)
6.0
Hustota
2,5 g/cm3 pri 25 ° C (tetrahydrát).
Rozklad
Keď sa dusičnan vápenatý zahrieva na žiarenie, rozkladá sa na oxid vápenatý, oxid dusíka a kyslík.
Reaktívny profil
Je to silne oxidačné činidlo, ale nie je to palivo. Urýchľuje zapaľovanie horľavých materiálov. Rozdelenie dusičnanu vápenatého do jemných častíc uľahčuje jeho výbuch, keď je zlúčenina vystavená predĺženému požiaru.
Môže vám slúžiť: neoterné zliatiny: štruktúra, vlastnosti, použitia, príkladyZmesi s alkyl estery sa stávajú výbušnými tým, že spôsobujú estery alkyl dusičnanov. Kombinácia dusičnanu vápenatého s fosforom, cínový chlorid (II) alebo iné redukčné činidlo, môže reagovať výbušne.
Žiadosti
poľnohospodárstvo
Používa sa v plodinách ako zdroj dusíka a vápnika. Dusičnan vápenatý je veľmi rozpustný vo vode a ľahko sa absorbuje koreňmi rastlín. Okrem toho neočídá pôdy, pretože ich ióny nemôžu významne hydrolyizovať.
Jeho zmesi by sa malo vyhnúť hnojivom obsahujúcim fosfor alebo síran, aby sa zabránilo tvorbe nerozpustných solí. Po vašej hygroskopicite sa musí uložiť v suchom a čerstvom prostredí.
Jeho použitie má výhodu oproti použitiu dusičnanu amónneho ako hnojiva. Zatiaľ čo táto zlúčenina prináša dusík do rastlín, interferuje s absorpciou vápnika, ktorá by mohla spôsobiť nedostatok vápnika v rastlinách.
Vápnik prispieva k udržiavaniu štruktúry bunkovej steny rastliny. V prítomnosti nedostatku vápnika, tkanivá vo formovaní rastlín, ako sú špičky koreňov, mladé listy a špičky ohniskov, často vykazujú skreslený rast.
Zníženie amória
Dusičnan vápenatý znižuje akumuláciu prchavých mastných kyselín a fenolových fytotoxických zlúčenín, ktoré sa hromadia rozkladom odpadu z sójových plodín.
Okrem toho existuje trend dusičnanu vápenatého na zníženie koncentrácie amonia v pôde, čo zvyšuje kapacitu tlmenia vodíka.
Betón
Dusičnan vápenatého sa používa na skrátenie času nastavenia betónu. Toto je produkované generovaním hydroxidu vápenatého, možno aj dvojitou reakciou na posun.
Okrem toho dusičnan vápenatý indukuje tvorbu zlúčeniny hydroxidu železa, ktorej ochranný pôsobenie betónu znižuje jeho koróziu. To znamená, že prítomné železo môže reagovať so základnými zložkami betónu, ako je napríklad samotný hydroxid vápenatý.
Dusičnan vápenatého znižuje čas nastavenia, ako aj odpor betónu, ku ktorému bol pridaný sopečný popol. Na štúdium účinku agregátu dusičnanu vápenatého na betón sa použili zvyšujúce sa koncentrácie dusičnanu vápenatého medzi 2% a 10%.
Môže vám slúžiť: Molárna frakcia: Ako sa vypočítava, príklady, cvičeniaPozorovalo sa väčšie zníženie času stanovovania, ako aj zvýšenie rezistencie na betón, keď sa koncentrácia dusičnanu vápenatého zvýšila na 10%.
Čistenie odpadu alebo odpadu
Dusičnan vápenatý sa používa na zníženie zápachu odpadových vôd znížením sírovodíka. Okrem toho sa konzumuje organické látky vytvárajúce anaeróbne podmienky, ktoré brzdia prežitie mnohých biologických druhov.
Príprava na studenú kompresiu
Dusičnan vápenatého dusičnanu je endotermická zlúčenina, ktorá má schopnosť absorbovať teplo z prostredia, ktoré ho obklopuje. To vytvára chladenie tiel, ktoré prichádzajú do styku s nádobami, ktoré ich obsahujú.
Kompress zvyšuje ich teplotu a na ich regenerovanie, stačí ich umiestniť do mrazničky
Latexová koagulácia
Dusičnan vápenatý sa používa vo fáze latexovej koagulácie. Je súčasťou ponorného roztoku a keď príde do kontaktu s roztokom, ktorý obsahuje latex, prelomí jeho stabilizáciu a spôsobuje jeho koaguláciu.
Prenos a skladovanie tepla
Binárna zmes roztavených dusičnanov, vrátane vápnika s inými dusičnanmi, sa používa namiesto tepelného oleja v závodoch solárnej energie na prenos a skladovanie tepla.
Formy aplikácie
-Dusičnan vápenatý zmiešaný so zemou sa aplikuje na koncentráciu 1,59 kg pre 30,48 m2, s primeraným zavlažovaním. Dusičnan vápenatý je solubilizovaný vo vode, čo umožňuje jeho absorpciu koreňmi rastliny. V hydroponických plodinách sa rozpúšťa v kultivačnej vode.
-Dusičnan vápenatého dusičnanu sa tiež používa na rozprašovanie listov a kvetov, čo predstavuje účinné ošetrenie pri prevencii hniloby paradajkového kvetu, korkového miesta a horkej diery jablka.
-Pridá sa do zmesi tvoriaceho betón (cement, piesok, kamene a voda) množstvo dusičnanu vápenatého a vplyv jeho pridania na špecifické vlastnosti betónu; napríklad rýchlosť nastavenia a odpor.
-Dusičnan vápenatého sa pridáva k primeranej koncentrácii, aby sa znížilo zápach odpadových vôd alebo zvyškov na úroveň, ktorá je zápach tolerovateľná pre ľudí.
Odkazy
- Špecifikácie dusičnanu vápenatého. Získané z: Direct2farmer.com
- Dusičnan vápenatý. Získané z: pubchem.Ncbi.NLM.NIH.Vláda

