Karnot
- 2647
- 840
- Alfréd Blaho
Čo je Carnot Machine?
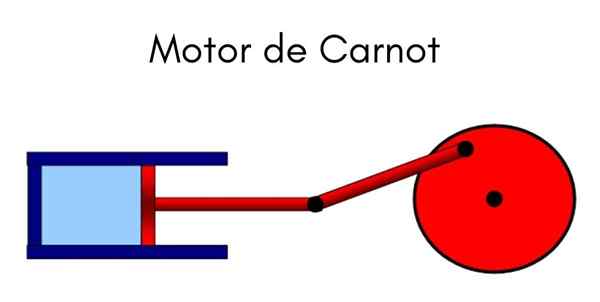
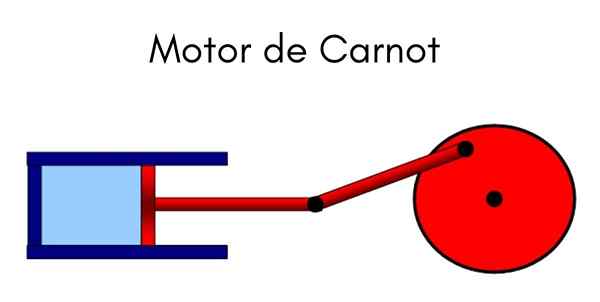
Ten Karnot Je to ideálny cyklický model, v ktorom sa teplo používa na prácu. Systém možno chápať ako piest, ktorý sa pohybuje vo vnútri valca, ktorý komprimuje plyn. Cyklus je cyklus Carnot, ktorý uviedol otec termodynamiky, francúzsky fyzik a inžinier Nicolas Leonard Sadi Carnot.
Carnot uviedol tento cyklus začiatkom devätnásteho storočia. Stroj je vystavený štyrom stavom variácií, striedajúcich sa podmienok, ako je konštantná teplota a tlak, kde sa pri stlačení a rozširovaní plynu preukazuje zmena objemu.
Vzorce
Podľa spoločnosti Carnot, ktorý vystavuje ideálny stroj na zmeny teploty a tlaku, je možné maximalizovať získaný výkon.
Cyklus Carnot sa musí analyzovať osobitne v každej zo svojich štyroch fáz: izotermálna expanzia, adiabatická expanzia, izotermálna kompresia a adiabatická kompresia.
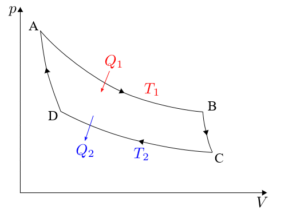
Vzorce spojené s každou z fáz cyklu vyvíjaného na Carnot Machine budú podrobne uvedené nižšie.
Izotermická expanzia (A → B)
Priestory tejto fázy sú nasledujúce:
- Objem plynu: Prechádza z minimálneho objemu na priemerný objem.
- Strojová teplota: Konštantná teplota T1, vysoká hodnota (T1> T2).
- Tlak: Zostup z P1 na p2.
Izotermálny proces naznačuje, že teplota T1 sa počas tejto fázy nemení. Prenos tepla indukuje rozširovanie plynu, ktorá indukuje pohyb na piest a vytvára mechanickú prácu.
Pri rozširovaní plyn predstavuje určitú tendenciu vychladnúť. Avšak absorbuje teplo emitované zdrojom teploty a počas jeho expanzie udržiava konštantnú teplotu.
Môže vám slúžiť: Aká je lineárna rýchlosť? (S vyriešenými cvičeniami)Pretože teplota zostáva počas tohto procesu konštantná, vnútorná energia plynu sa nemení a všetko teplo absorbované plynom sa efektívne transformuje na prácu. Tak:
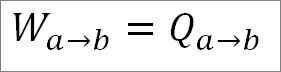
Na druhej strane, na konci tejto fázy cyklu je tiež možné získať tlakovú hodnotu pomocou ideálnej plynovej rovnice pre ňu. Týmto spôsobom máte nasledujúce:
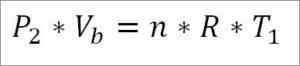
V tomto výraze:
- P2: Tlak na konci fázy.
- Vložkab: Objem v bode B.
- N: Počet mólov plynu.
- Odpoveď: Univerzálna konštanta ideálnych plynov. R = 0,082 (atm*liter)/(móla*k).
- T1: Absolútna počiatočná teplota, stupne Kelvin.
Adiabatická expanzia (B → C)
Počas tejto fázy procesu sa expanzia plynu vykonáva bez potreby vymeniť teplo. Týmto spôsobom sú priestory podrobne uvedené nižšie:
- Objem plynu: Prechádza z priemerného objemu na maximálny objem.
- Strojová teplota: Zostup z T1 na T2.
- Tlak: konštantný tlak P2.
Adiabatický proces znamená, že tlak P2 sa počas tejto fázy nemení. Teplota klesá a plyn sa neustále rozširuje, až kým nedosiahne maximum svojho objemu; to znamená, že piest dosiahne vrchol.
V tomto prípade vykonaná práca pochádza z vnútornej energie plynu a jej hodnota je negatívna, pretože energia sa počas tohto procesu znižuje.
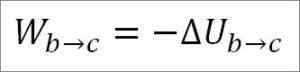
Za predpokladu, že ide o ideálny plyn, sa teória tvrdí, že molekuly plynu majú iba kinetickú energiu. Podľa zásad termodynamiky to možno odvodiť podľa nasledujúceho vzorca:
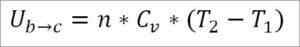
V tomto vzorci:
- ∆UB → C: Vnútorná variácia energetiky ideálneho plynu medzi bodmi B a C.
- N: Počet mólov plynu.
- CV: Molárna tepelná kapacita plynu.
- T1: Absolútna počiatočná teplota, stupne Kelvin.
- T2: Absolútna konečná teplota, stupne Kelvin.
Izotermická kompresia (C → D)
V tejto fáze sa začína kompresia plynu; To znamená, že piest je mobilizovaný do valca, s ktorým plyn stiahne svoj objem.
Podmienky spojené s týmto procesom sú podrobne uvedené nižšie:
- Objem plynu: Prechádza z maximálneho objemu na stredný objem.
- Strojová teplota: konštantná teplota T2, znížená hodnota (T2 < T1).
- Tlak: Zvýšenie z P2 na P1.
Tu sa zvyšuje tlak na plyn, takže sa začína komprimovať. Teplota však zostáva konštantná, a preto je vnútorná variácia energie plynu nula.
Analóg s izotermálnou expanziou, vykonaná práca sa rovná tepla systému. Tak:
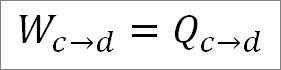
Je tiež možné nájsť tlak v tomto bode pomocou ideálnej plynovej rovnice.
Adiabatická kompresia (D → A)
Toto je posledná fáza procesu, v ktorej sa systém vracia k svojim počiatočným podmienkam. Za týmto účelom sa zvažujú nasledujúce podmienky:
- Objem plynu: Prechádza z prechodného objemu na minimálny objem.
- Strojová teplota: Zvýšenie z T2 na T1.
- Tlak: konštantný tlak P1.
Zdroj tepla začleneného do systému v predchádzajúcej fáze je odstránený, takže ideálny plyn medzitým zvýši svoju teplotu.
Plyn sa vracia na počiatočné teplotné podmienky (T1) a pri objeme (minimum). Vykonaná práca opäť pochádza z vnútornej energie plynu, takže musíte:
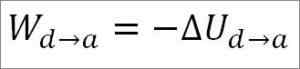
Podobne ako v prípade adiabatickej expanzie je možné získať zmenu energie plynu prostredníctvom nasledujúceho matematického výrazu:
Môže vám slúžiť: fluorid vápenatý (CAF2): Štruktúra, vlastnosti, používa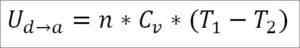
Ako funguje stroj Carnot?
Carnot Machine funguje ako motor, v ktorom sa výkon maximalizuje variáciou izotermických a adiabatických procesov, striedajú sa fázy expanzie a porozumenia ideálneho plynu.
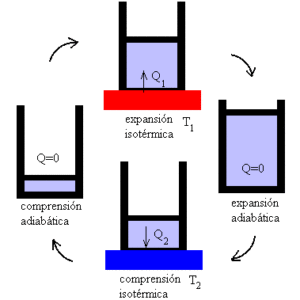
Mechanizmus možno chápať ako ideálne zariadenie, ktoré vykonáva prácu, ktorá je vystavená teplým variáciám, vzhľadom na existenciu dvoch teplotných reflektorov.
V prvom zameraní je systém vystavený teplote T1. Je to vysoká teplota, ktorá podlieha systému na stres a vytvára rozširovanie plynu.
To sa zase premieta do vykonávania mechanického diela, ktoré umožňuje mobilizáciu piestu z valca a ktorého limit je možný iba adiabatickou expanziou.
Potom prichádza druhé zameranie, v ktorom je systém vystavený teplote T2, menej ako T1; To znamená, že mechanizmus je vystavený chladeniu.
To indukuje tepelnú extrakciu a drvenie plynu, ktorá dosahuje jeho počiatočný objem po adiabatickej kompresii.
Žiadosti
Carnot Machine sa široko používa vďaka svojmu príspevku v porozumení najdôležitejších aspektov termodynamiky.
Tento model vám umožňuje jasne porozumieť variáciám ideálnych plynov, ktoré sú predmetom zmien teploty a tlaku, čo je referenčná metóda pri navrhovaní skutočných motorov.