Koncentrácia molarity, jednotky, výpočet, cvičenia
- 1218
- 308
- JUDr. Rudolf Čapkovič
Ten Molárnosť Je to koncentrácia roztoku exprimovaného v móloch z rozpustenej látky na liter roztoku. Je skrátená ako M a vyjadruje vzťah medzi hmotnosťou rozpustenej látky a objemom roztoku (m/v); Aj keď tradičným spôsobom je tento vzťah vyjadrený ako objemová hmotnosť.
Jeden mol je počet atómov alebo molekúl obsiahnutých v atómovej alebo molekulovej hmotnosti; Je vyjadrený v gramoch/mol. Jeden krt je rovnocenný 6,02 · 1023 Atómy alebo molekuly, známe ako číslo Avogadro.
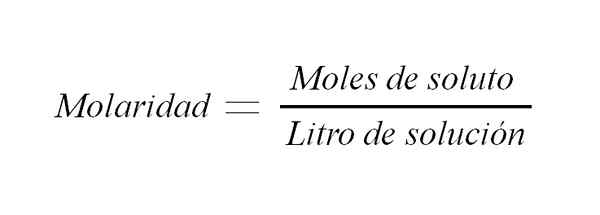 Morálka. Zdroj: Gabriel Bolívar.
Morálka. Zdroj: Gabriel Bolívar. Existujú aj iné spôsoby, ako vyjadriť vzťah medzi hmotnosťou rozpustenej látky a objemom, vrátane: percentuálneho vzťahu medzi hmotnosťou rozpustenej látky a objemom riešenia a normálnosťou. Ten je vyjadrený ako počet ekvivalentov rozpustenej látky na liter roztoku.
Medzitým molealita, ktorá je definovaná ako počet mólov na kilogramy rozpúšťadla, zvyčajne vody, vyjadruje vzťah medzi hmotnosťou rozpustenej látky a hmotnosťou rozpúšťadla (m/m).
Forma expresie koncentrácie roztoku v častiach na milión (ppm) vyjadruje vzťah medzi časťou rozpustenej látky a jedným miliónom častí roztoku, ktorý sa všeobecne používa na expresiu pomeru hmotnostnej MASA (m/m). Ale môžete vyjadriť pomer hmotnosti a objemu (m/v).
Molárna koncentrácia, okrem exprimovania v móloch na liter, sa môže vyjadriť ako milimoles/liter (milimolárny roztok); Mikromoly/ liter (Mikromolárny roztok); atď.
Problémy s molaritou je možné vyriešiť pomocou analytickej metódy a pomocou „pravidla troch“. Výber metódy bude závisieť od schopnosti používať jednu z metód.
[TOC]
Koncentrácia moláru
Sa používa na vyjadrenie koncentrácie rozpustenej látky v určitom roztoku roztoku.
M = N/V (1)
Kde sa m rovná molarite, n je počet krtkov a v objem roztoku. Takže molarita roztoku je počet mólov rozpustenej objemu roztoku exprimovaným v litroch.
Na druhej strane je počet mólov
n = m / pm (2)
Byť m hmotnosť rozpustenej rozpustenej látky a PM jeho molárnej hmoty.
Môže vám slúžiť: aldehydosVýmena (2) v (1):
M = (m / pm) / v
Jednotky
Jednotka v medzinárodnom systéme pre molárnu koncentráciu je mol/m3. To zodpovedá milimolárnemu roztoku, pretože m3 rovnocenné 1.000 litrov. V odvetviach chémie a biológie je molárna koncentrácia zvyčajne exprimovaná ako móly/l. Táto jednotka je vyjadrená s M (kapitál).
Roztok jedného mol/l je ekvivalentný s M; Roztok 10-3 móly/l, rovnocenné s 1 mm (milimolárny); a 10 roztoku-6 móly/l, ekvivalentné 1 um (mikróm).
Ako vypočítať molaritu?
Je vhodné použiť vyššie uvedené výrazy, pretože to zaisťuje, že výsledok použitia vzorca bude uvedený v krtkoch/litroch, čo je definícia molárnej koncentrácie.
Takže na výpočet molárity roztoku je potrebné vyjadriť koncentráciu rozpustenej látky v G / L. Potom zistite molekulovú hmotnosť rozpustenej látky (g / mol) a nájdite kvocient medzi koncentráciou a molekulovou hmotnosťou. Získaný výsledok je molarita exprimovaná v móloch / liter.
Prejdite sa z molarity k molicite
Potrebnou skutočnosťou na prechod z molarity na molealitu je poznať hustotu roztoku. To umožňuje poznať hmotnosť roztoku, čo je nevyhnutná požiadavka na výpočet moliality.
Prvý krok
Najprv musíte ísť z molárnej koncentrácie do gramov/litrov. Na to stačí vynásobiť molaritu roztoku molekulovou hmotnosťou rozpustenej látky.
Gramy/liter rozpustenej látky = molarita (móly/liter) · Molekulová hmotnosť rozpustenej látky (gramy/mol).
To umožňuje získať hmotnosť rozpustenej látky v 1 l roztoku.
Druhý krok
Potom je potrebné vypočítať hmotnosť roztoku. Na tento účel sa používa hustota toho istého. Zvyčajne je hustota vyjadrená v gramoch/kubickom centimetri alebo mililiter.
Hmotnosť roztoku (g) = objem roztoku (ml) · hustota (g/ml)
Tretí krok
Získanie hmotnosti rozpúšťadla. Pretože hmotnosť roztoku sa rovná hmotnosti rozpustenej látky plus hmotnosť rozpúšťadla, na získanie hmotnosti posledného je dostatočné na odpočítanie od hmotnosti roztoku (krok 2) hmotnosti rozpustenej látky (krok 1).
Môže vám slúžiť: oxid z postupe (CL2O7)Štvrtý krok
Nakoniec musíte prejsť hmotnosť rozpustenej látky (G) roztoku do hmotnosti rozpustenej látky, ktorá zodpovedá 1.000 g alebo 1 kg rozpúšťadla. Na to by stačilo urobiť pravidlo troch jednoduchých alebo iných ekvivalentných matematickej operácie.
Piaty krok
Rozdeľte g rozpustenej látky/1 000 g rozpúšťadla medzi molekulovú hmotnosť rozpustenej látky (G/mol), aby ste získali morálku roztoku.
Numerický príklad
3 M glukózový roztok (180 g/mol molekulová hmotnosť) má hustotu 1,15 g/ml. Vypočítajte molealitu tohto roztoku.
Najprv vypočítame gramy glukózy rozpustené v liter roztoku:
g/l = 3 móly/l · 180 g/mol
= 540 g/l
Potom vypočítame hmotnosť roztoku z jeho hustoty:
g roztoku (hmotnosť) = 1.000 ml · 1,15 g/ml
= 1.150 g
Hmotnosť rozpúšťadla je daná rozdielom:
Hmotnosť rozpúšťadla = hmotnosť roztoku - hmotnosť rozpustených látok
= 1.150 g - 540 g
= 610 g
Ale 610 g nie je 1000 g rozpúšťadla, pretože stanovuje definíciu moliality. Preto, koľko gramov glukózy sa musí vypočítať, sa rozpustí v 1000 g rozpúšťadla:
Hmotnosť rozpustenej látky = 540 g rozpustenej látky · (1.000 g rozpúšťadla / 610 g rozpúšťadla)
= 885,25 g
A nakoniec sa molealita vypočíta vrátením gramov do krtkov:
MOLLALITA = (885,25 g rozpusteného / 180 g / mol)
= 4,92 mol Solute / kg rozpúšťadla
= 4,92 m
Problémy vyriešené
Problém 1
Koľko cupric sulfátu bude potrebný na prípravu 500 ml roztoku 0,4 m? Vyjadriť výsledok v gramoch. Molekulová hmotnosť sulfátu podriadeného (CUSO4): 160 g/mol.
Najprv určíme móly, ktoré sa musia rozpustiť v takom roztoku:
M = N/ V
n = m · v
n = (0,4 mol/l) · 0,5 l
= 0,2 mólov
Vedieť potom je počet mólov sulfátu podriadeného, ktorý je možné získať jeho hmotnosť
N = m/pm
M = N · Molekulová hmotnosť
M = 0,2 mol · 160 g/mol
= 32 g Cuso4
To znamená, 32 gramov tejto soli sa musí rozpustiť v 500 ml rozpúšťadla.
Problém 2
Aký objem roztoku je potrebný na rozpustenie 0,4 mólov rozpustenej látky, má koncentráciu 0,25 m?
Objem roztoku sa získa z koncepcie molarity
Môže vám slúžiť: Samario: Charakteristiky, štruktúra, získanie, použitieM = N / V
V = n / m
V = 0,4 mol / (0,25 mol / l)
= 1,6 l
To znamená, že roztok musí mať objem 1,6 litra, aby sa získala takáto koncentrácia 0,25 m.
Problém 3
Hmotnosť 8 g hydroxidu sodného (NaOH) sa rozpustí v 60 g roztoku, ktorý má hustotu 1,6 g/ml. Aká bude molarita roztoku? Molekulová hmotnosť hydroxidu sodného: 40 g/mol.
Naohove móly sa musia vypočítať ako prvé:
N = m / pm
= 8 g hydroxidu sodného / (40 g / mol)
= 0,2 mólov
Teraz sa vypočíta objem riešenia:
M = V · D
V = 60 g /(1,6 g /ml)
V = 37,5 ml
Na získanie molarity musí byť umiestnený objem roztoku v litroch:
V = 37,5 ml · 10-3 L / ml
= 0,0375 l
M = 0,2 mol / 0,0375 l
5,33 mólov / l
5,33 m
Problém 4
Vypočítajte molaritu roztoku kyseliny chlorovodíkovej (HCl) s hustotou 1,25 g/ml a koncentráciou 35%, exprimovanej hmotnosti/hmotnosti. Molekulová hmotnosť kyseliny chlorovodíkovej: 36,5 g/mol.
Stanovuje sa hmotnosť 35% kyseliny chlorovodíkovej
M = V · D
m = 1.000 ml · 1,25 g/ml
= 1.250 g
Ale nie všetko je HCl, ale existuje aj voda:
HCl Mass = 1.250 g · (35 /100)
= 437,5 g
Čo je to isté ako tvrdenie, že v liter 35% roztoku HCL je 437,5 gramov HCL.
Potom sa vypočítajú móly HCL, aby sa stanovila molarita:
N = m / pm
n = (437,5 g/l)/(36,5 g/mol)
= 11,98 mólov/l
Molarita = 11,98 m
Problém 5
Vypočítajte molaritu roztoku obsahujúceho 5 g NaCl v 2 L roztoku. Molekulová hmotnosť chloridu sodného: 58,5 g/mol.
Móly/l NaCl je možné získať v jednom kroku:
Molarita = (5 g NaCl / 2 l roztok) x (1 mol NaCl / 58,5 g NaCl)
= 0,043 mol /l
Molarita = 0,043 m
Ďalším postupom môže byť:
G / l NaCl = 5 g / 2 l
= 2,5 g / l
móly / l = (2,5 g / l) / (58,5 g / mol)
= 0,043 mol / l
= 0,043 m
Odkazy
- Rodríguez, m. (2007). Chémia. Redakčná nadácia Salesiana
- Whitten, Davis, Peck & Stanley. (2008). Chémia. (8. vydanie.). Učenie sa.
- Wikipedia. (2019). Molárnosť. Obnovené z: je.Wikipedia.orgán
- Atarés huerta. (s.F.). Molialita. [PDF]. Získané z: Riunet.UPV.je
- Mäkké školy. (2019). Morálka. Obnovené z: softschools.com
- « Charakteristiky špeciálnych zlúčenín, školenie, použitie
- Ťažkosti s konsolidáciou projektu národa »

