Atómové modely
- 4754
- 1461
- Adrián Fajnor
 Atómové modely sú rôzne grafické reprezentácie, ktoré boli dané atómmi v celej histórii. Rúno
Atómové modely sú rôzne grafické reprezentácie, ktoré boli dané atómmi v celej histórii. Rúno Čo sú to atómové modely?
Ten Atómové modely Sú to grafické znázornenia štruktúry a prevádzky atómu. V histórii bolo veľa modelov.
Dôvodom je, že myšlienka atómu ako základného bloku, ktorého hmota sa vyrába, sa narodila pred tisíckami rokov v starovekom Grécku. V tom čase bol atóm iba produktom filozofických špekulácií.
Keď sa objavili nové vedecké objavy, boli vytvorené nové modely na začlenenie získaných vedomostí. A tak sa to stalo storočie po storočí až do dnešného dňa, keď nám technológia umožnila pozorovať atómy prostredníctvom mikroskopov a určiť správny model.
Čo sú atómy?
Atómy sú submikroskopické štruktúry, z ktorých sa vytvára všetok subjekt, ktorý vnímame, a s ktorými interagujeme každý deň, z nášho tela, jedlo, ktoré jeme, oblečenie, ktoré nosíme, do veľkých mrakodrapov a lietadiel.
Slnko, mesiac, planéty, hviezdy a galaxie sú tvorené atómami.
Sú také malé, že ich nemožno vidieť pri bežných mikroskopách. Iné sú povinné od väčšej sily, nazývané ultramikálne. Atómy však nie sú najmenšími jednotkami prírody.
Atómy sú následne tvorené ešte menšími časticami: protóny, neutróny a elektróny.
Protóny majú kladný elektrický náboj, zatiaľ čo neutróny nemajú elektrický náboj. Tieto dva typy častíc tvoria jadro atómu.
Otáčanie sa okolo jadra, ako sú planéty okolo slnka, sú elektróny, ktoré majú negatívny elektrický náboj.
Atómový model Demokritus

Demokritus z Abdera bol grécky filozof, ktorý žil medzi 460 a 370 pred súčasnou érou. Potvrdil, že všetku hmotu tvorili malé častice, ktoré nazýval atómy, čo v gréčtine znamená nedeliteľné.
Podľa Demokritusa je atóm najmenšou časťou, v ktorej možno túto záležitosť rozdeliť. Existuje nekonečné množstvo, ktoré sú nezničiteľné, neuveriteľné, večné a úplne kompaktné, bez pórov. Existuje niekoľko typov, ktoré sa líšia podľa formy, veľkosti, polohy a spôsobu, akým sú ochotní.
Môže vám slúžiť: katastrofy spôsobené ľudskou bytosťou pri používaní vedy a technikyDemokritusova teória bola odmietnutá Aristotelesom a potom úplne zabudnutá až do výskytu modernej vedy.
Atómový model Dalton

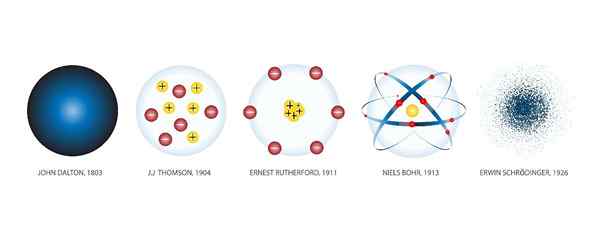
John Dalton (1766-1844) bol anglický meteorológ, ktorý mal záujem vyšetrovať zákony, ktoré riadia správanie plynu. Ovocie svojej práce v tejto oblasti bolo prvým atómovým modelom modernej vedy, ktorú vytvoril v roku 1803.
Keďže existencia protónov a elektrónov ešte nebola objavená, Dalton povedal, rovnako ako Demokritus, že atóm je najmenšou časťou, v ktorej možno rozdeliť hmotnosť, a preto je samo osebe neoddeliteľné.
Podľa Daltona sú atómy pevné a majú sférický tvar, ako baseballová guľa. Dalton ilustroval svoju teóriu rezbárstva v dreve, spolu s jeho asistentmi, desiatky sfér, ktoré predstavujú atómy rôznych chemických prvkov.
Tento model bol v platnosti až do objavenia elektrónu.
Thomson Atomic Model
Anglický fyzik Joseph John Thomson (1865-1940) musel urobiť jeden z najdôležitejších objavov modernej vedy: objavenie elektrónu.
Bolo to v roku 1897 v Cavendish Laboratory na University of Cambridge v Anglicku, kde si tabuľa stále pripomína veľký objav.
Thompson a jeho asistenti projektujú katódové lúče na elektrickom poli. Po kontakte s poľom sa lúče odchýlili s tvorbou širokých uhlov. To potvrdilo, že katódové lúče mali záporný elektrický náboj. Tie negatívne nabité častice ich nazývajú elektróny.
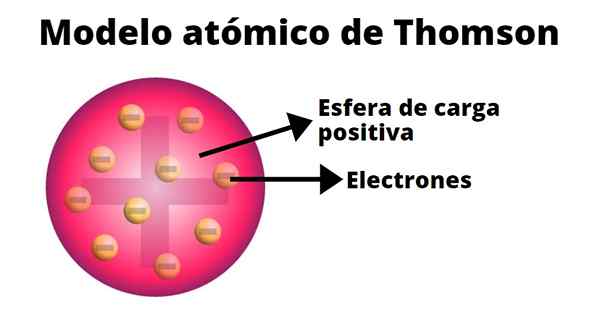
Thomson predpokladal, že elektróny boli zabudované do atómov. Jeho atómový model pochádza z roku 1904.
Puding hrozienok
V Thompsonovom atómovom modeli je atóm pevná guľa s pozitívnym zaťažením (protóny), na ktorých sú náhodne distribuované neutróny (negatívne zaťaženie), pretože raisíny hodené na pudin. Preto bol tento model známy ako „pudin de pasas“.
Podľa Thompsona má atóm polomer 0,00000001 centimetrov a jeho zaťaženie je neutrálne, pretože protóny a elektróny majú rovnaké zaťaženie, ale s opačným znakom.
Model Thompsona nepredstavuje neutróny.
Rutherford Atomic Model
Ernest Rutherford (1871-1937), neozylánsky fyzik, bol jedným z najvýznamnejších Thomsonových študentov.
Môže vám slúžiť: korelačný výskumV roku 1911 a na základe vtedajšieho objavu rádioaktivity Rutherford uskutočnil nasledujúci experiment: Vystrelili alfa rádioaktívne častice s vysokou rýchlosťou a energiou proti plechu zlata.
Keby bol atómový model Thompsona správny, alfa častice by prešli hárkom bez toho, aby sa odchýlili alebo s nevýznamnou odchýlkou. Keď však vypočítali uhol odchýlky od častíc, zistili, že je široký a že niektorí dokonca odrážajú zlatý list.
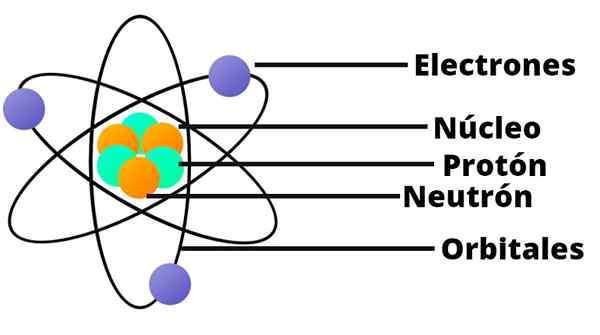
S týmto výsledkom Rutherford pochopil, že atóm by mal mať veľmi malé a vysoko kondenzované jadro. Toto jadro bolo pozitívne nabité.
Malá slnečná sústava
Rutherfordov atómový model je ako miniatúrna slnečná sústava. V strede, na mieste, ktoré by zodpovedalo slnku, je jadro s jeho pozitívne naloženými protónmi. Okolo toho, obieha ako planéty, sú náhodne rozložené elektróny.
Rutherford tiež preukázal, že hmotnosť atómu je rovnocenná so súčtom masy elektrónov a protónov.
Bohr atómový model
Aj keď model Rutherford bol nepopierateľným pokrokom v súvislosti s predchádzajúcimi modelmi, mal dôležité chyby. Napríklad, ak by elektróny účinne orbitáli okolo jadra nakoniec stratili energiu a zrútili sa na jadre. Ale to sa samozrejme nestalo.
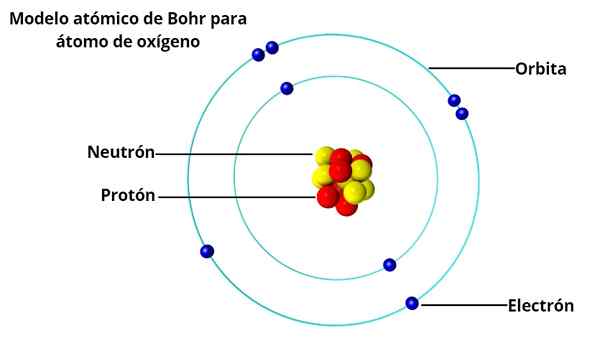
Bol to dánsky fyzik Niels Bohr (1885-1962), študent Rutherfordu na University of Manchester (Anglicko), ktorý v roku 1913 navrhol atómový model, ktorý vyriešil problémy, ktoré predstavuje jeho starý profesor.
Kruhové obežné dráhy
V atómovom modeli Bohr elektróny neobchodujú voľne okolo jadra, ale robia tak v stabilných kruhových dráhach, ktoré sú od seba navzájom oddelené určitou vzdialenosťou, podobne ako sú usporiadané planéty slnečnej sústavy. Každá obežná dráha sa nazýva úroveň energie alebo energie.
Na základe vyšetrovaní Max Plancka a Alberta Einsteina zistil, že každý elektrón na svojej obežnej dráhe má určité množstvo energie.
Zatiaľ čo obiehajú stabilné okolo jadra, hovorí sa, že elektróny sú v stacionárnom stave. Na druhej strane, keď elektrón „skočí“ na obežnú dráhu s nižšou energiou, je tu fotón.
Môže vám slúžiť: metodikaModel Bohr však nebol úspešný na vysvetlenie prevádzky atómov viac ako jedným elektrónom.
Sommerfeld atómový model
Arnold Sommerfeld (1868-1951) bol nemecký fyzik, ktorý venoval svoju prácu rozširovaniu Bohrovho atómového modelu. Tento rozšírený model bol prezentovaný v roku 1916.
Na základe Einsteinovej teórie relativity, Sommerfeld zistil, že niektoré elektróny obiehajú okolo jadra pri rýchlostiach blízko svetla (300.000 kilometrov za sekundu).
Uskutočnil tiež nasledujúce úpravy modelu Bohr:
- Elektróny sa pohybujú okolo jadra v kruhových a eliptických dráhach. Bohr rozpoznáva iba kruhové obežné dráhy.
- V rámci rovnakej úrovne energie existujú čiastkové úrovne s mierne odlišnými energiami.
Kvantový mechanický model (Broglie, Heisenberg a Schrödinger)
Toto je najpresnejší atómový model, ktorý je známy a v súčasnosti je akceptovaný, s niektorými následnými prírastkami. Vyvinuli ho traja vedci: nemecký Werner Heisenberg (1901-1976), rakúsky Erwin Schrödinger (1887-1961) a Francúz Louis de Broglie (1892-1987).
Tento model zlikviduje myšlienku elektrónov, ktoré obiehajú jadro. Namiesto toho máme elektronické oblaky, ktoré sú priestormi okolo jadra, v ktorých je možné nájsť elektrón. Toto sa správa ako stacionárna vlna.
Pravdepodobnosť zistenia, že sa vypočíta s rovnicou stanovenou Schrödingerom.
Toto je kvantový mechanický model atómu, ktorý začal zo Schrödingerovej rovnice. S touto rovnicou ste mohli poznať pravdepodobnosť nájdenia elektrónu v určitom bode atómu.
V tomto modeli sa každý elektrón pohybuje v špecifickom smere, ktorý je určený štyrmi kvantovými číslami, ktoré sú: hlavné kvantové číslo, sekundárne kvantové číslo, magnetické kvantové číslo a kvantové číslo rotácie.
Neexistujú dva elektróny, ktoré majú rovnaké kvantové čísla, ako je uvedené v princípe vylúčenia, ktorý objavil fyzik Wolfgang Pauli.
Odkazy
- (2010). Atóm. Moderná encyklopédia britská.
- (s. F.). Demokritus atómový model, filozofický atomizmus. Prevzaté z energetického.slepo.
- (s. F.). Sommerfeld atómový model, rozšírenie modelu Bohr. Prevzaté z energetického.slepo.
- Bertsch, G. F.; Trefil, James a McGrayne, Sharon Bertsch (2021). Atóm. Encyclopedia Britannica. Prevzaté z Britannice.com.
- Duignan, b. (2021). Demokrit. Encyclopedia Britannica. Prevzaté z Britannice.com.
- Prispievatelia Encyclopedia New World. (2021). Atóm. Prevzaté z Novejclopédie.orgán.
- Zita, Ana. (s. F.). Atómové modely. Prevzaté z Todamateria.com.

