Štruktúra metoxyetánu, vlastnosti, získanie, použitie, riziká
- 2072
- 98
- MUDr. Miloslav Habšuda
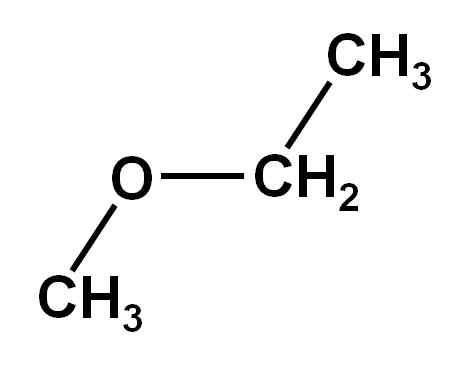
On Metoxyetan Je to organická zlúčenina rodiny éterov alebo alcoxidov. Jeho chemický vzorec je Cho3Okradnúť2Chvály3. Nazýva sa tiež metyl etil éter alebo etylmetyléter. Je to plynná zlúčenina pri teplote miestnosti a jej molekula predstavuje dve metyl -ch skupiny3, jeden pripojený priamo k kyslíku a druhý patriaci k etylu -ch2Chvály3.
Metoxietano je bezfarebný plyn, rozpustný vo vode a miešateľný s éterickým alkoholom a alkoholom. Byť éter je trochu reaktívna zlúčenina, môže však reagovať pri vysokých teplotách s niektorými koncentrovanými kyselinami.
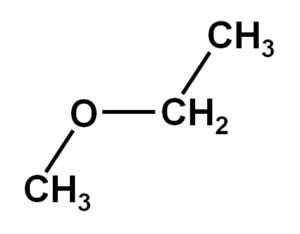 Metoxietano alebo metyléter éter. Autor: Marilú Stea
Metoxietano alebo metyléter éter. Autor: Marilú Stea Všeobecne sa získava So -Called Williamsonov syntéza, ktorá zahŕňa použitie alkoxidu sodného a alkyljodidu. Na druhej strane sa jeho rozklad bol študovaný za niekoľkých podmienok.
Metoxietano sa používa vo výskumných laboratóriách s rôznymi cieľmi, napríklad pri štúdiu polovodičových nanomateriálov alebo pri pozorovaní medzihviezdnej hmoty v konšteláciách a veľkých molekulárnych oblakoch vesmíru vesmíru.
V skutočnosti, vďaka veľmi citlivým teleskopom (interferometre), bol zistený na určitých miestach medzihviezdneho priestoru.
[TOC]
Štruktúra
Metoxyetan zlúčenina má metylovú skupinu -ch3 a etylová skupina -ch2Chvály3 obe pripojené k kyslíku.
Ako je zrejmé, v tejto molekule sú dve metylové skupiny, jedna pripevnená k kyslíkovi Cho3-O a druhý patriaci k etylu -ch2-Chvály3.
V základnom alebo nižšom stave energetiky metylová skupina -ch2-Chvály3 je v polohe previesť Pokiaľ ide o metyl spojený s kyslíkom, to znamená na diametrálne opačnom mieste, ako odkaz na odkaz Cho2-Ani. Preto sa niekedy volá previesť-Etylmetyléter.
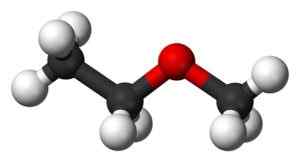 Trans-etylmetyléter štruktúra v 3D. Čierna: uhlík. Biely: vodík. Červená: kyslík. Spojenie medzi kyslíkom a -ch2- sa môže otáčať, v takom prípade dva -ch3 boli by bližšie k sebe. Ben Mills a Jynto [verejná doména]. Zdroj: Wikipedia Commons.
Trans-etylmetyléter štruktúra v 3D. Čierna: uhlík. Biely: vodík. Červená: kyslík. Spojenie medzi kyslíkom a -ch2- sa môže otáčať, v takom prípade dva -ch3 boli by bližšie k sebe. Ben Mills a Jynto [verejná doména]. Zdroj: Wikipedia Commons. Táto molekula môže zažiť torziu v COL Link2-Alebo, čo umiestni metyl do inej priestorovej polohy ako previesť , Metyl -ch3 Sú veľmi blízko k sebe a táto torzia generuje prechod energie detegovateľná citlivými nástrojmi.
Môže vám slúžiť: Coulombimetria: Základy, typy, aplikácieMenovanie
- Metoxyetan.
- Metylový éter.
- previesť-Ethil metyléter (hlavne v anglicky hovoriacich literatúre, anglický preklad previesť-Etylmetyléter).
Fyzikálne vlastnosti
Fyzický stav
Bezfarebný plyn
Molekulová hmotnosť
60 096 g/mol
Bod topenia
-113,0 ° C
Bod varu
7,4 ° C
Bod vzplanutia
1,7 ° C (metóda zatvoreného pohára).
Samostatná teplota
190 ° C
Špecifická váha
0,7251 až 0 ° C/0 ° C (je menej hustá ako voda, ale ťažšia ako vzduch).
Index lomu
1 3420 až 4 ° C
Rozpustnosť
Rozpustné vo vode: 0,83 mólov/l
Rozpustný v acetone. Misilné s etylalkoholom a etyléterom.
Chemické vlastnosti
Metoxietano je éter, takže je relatívne malý reaktívny. Union-oxygón-uhlíka Únia C-O-C je veľmi stabilná pred základňami, oxidačnými činidlami a reduktormi. Vytvára iba svoju degradáciu kyseliny, ale prebieha iba vo intenzívnych podmienkach, to znamená s koncentrovanými kyselinami a vysokými teplotami.
Má však tendenciu oxidovať sa v prítomnosti nestabilných peroxidov tvoriacich vzduchu. Ak sú nádoby, ktoré obsahujú na zahriatie alebo oheň, násilne využívajú nádoby.
Rozklad tepla
Keď je metoxyetan podrobený zahrievaniu medzi 450 a 550 ° C, rozdelí sa na acetaldehyd, etán a metán. Táto reakcia je katalyzovaná prítomnosťou etyljodidu, ktorý je všeobecne prítomný vo vzorkách laboratórneho metoxyetánu, pretože sa používa pri jeho získavaní.
Fotosenzibilizovaný rozklad
Metoxyetán ožarovaný ortuťou parnou lampou (vlnová dĺžka 2537 Á) rozkladom vytvárania širokej škály zlúčenín, medzi ktorými vyniká: vodík, 2,3-dimetoxibtán, 1-etoxy-2-metoxipán a metyl vinyléter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter éter.
Konečné výrobky závisia od doby ožarovania vzorky, pretože pokračovaním ožarovania, ktoré spočiatku tvoria nové zlúčeniny.
Predĺžením doby ožarovania môžu tiež tvoriť: propán, metanol, etanol, acetón, 2-butanón, oxid uhoľnatý, etyl-N-propyléter a metyl-SEC-bititil éter éter.
Získanie
Pretože je to nesymetrický éter, metoxyetán sa môže získať reakciou medzi metoxidom sodným CH3Ona a Yoduro de Etilo ch3Chvály2Jo. Tento typ reakcií sa nazýva Williamsonova syntéza.
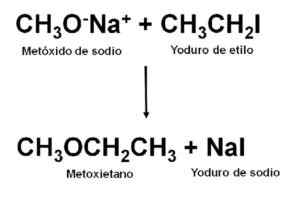 Získanie Metoxietana prostredníctvom Williamsonovej syntézy. Autor: Marilú Stea.
Získanie Metoxietana prostredníctvom Williamsonovej syntézy. Autor: Marilú Stea. Po vykonaní reakcie sa zmes destiluje, aby sa získal éter.
Môže vám slúžiť: ternárne zlúčeniny: Charakteristiky, školenie, príkladyMôže sa tiež získať pomocou choxidu sodného sodného3Chvály2Ona a metylsulfát (ch3)2SW4.
Umiestnenie vo vesmíre
On previesť-Ethil metyléter bol detegovaný v medzihviezdnej polovici v oblastiach, ako je konštelácia Orion KL a v obrovskom molekulárnom oblaku W51E2.
 Orion Constellation, kde sú pozorované molekulárne oblaky. Rogelio Bernal Andreo [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)]. Zdroj: Wikipedia Commons.
Orion Constellation, kde sú pozorované molekulárne oblaky. Rogelio Bernal Andreo [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)]. Zdroj: Wikipedia Commons. Detekcia tejto zlúčeniny v medzihviezdnom priestore spolu s analýzou jej hojnosti je užitočná pre konštrukciu modelov medzihviezdnych chémie.
Použitie metoxyetánu
Metoxietano alebo metyléter éter sa väčšinou používa v laboratórnych skúsenostiach s vedeckým výskumom.
Pre štúdie o medzihviezdnych veciach
Ako organická molekula s vnútornými rotáciami je Metoxietano chemickou zlúčeninou, ktorá je predmetom záujmu štúdie medzihviezdnej hmoty.
Vnútorné rotácie ich metylových skupín spôsobujú energetické prechody v mikrovlnnej oblasti.
Preto ich môžu zistiť vysoko citlivé teleskopy, ako je napríklad veľký milimeter/submylimetrický súbor Atacama alebo duša (skratka pre angličtinu Atacama veľký milimeter/submilimeterový pole).
 Vzhľad časti veľkého astronomického observatóriu almy. ESO/José Francisco Salgado (Josefrancisco.org) [CC po 4.0 (https: // creativeCommons.Org/licencie/o/4.0)]. Zdroj: Wikipedia Commons.
Vzhľad časti veľkého astronomického observatóriu almy. ESO/José Francisco Salgado (Josefrancisco.org) [CC po 4.0 (https: // creativeCommons.Org/licencie/o/4.0)]. Zdroj: Wikipedia Commons. Vďaka svojej vnútornej rotácii a veľkým priestorovým observatóriám previesť-Metylový éter bol nájdený v konštelácii Orion a v obrovskom molekulárnom mraku W51E22.
Odvodiť chemické transformácie v rôznych študijných oblastiach
Niektorí vedci pozorovali tvorbu metoxyetanu alebo metylytyléteru, keď je zmes etylénu CH vyžarovaná elektrónmi2= CH2 A metanol ch3Oh.
Mechanizmus reakcie prechádza tvorbou radikálneho ch3Alebo •, ktorý útočí na dvojité puto bohaté na elektróny Cho2= CH2. Výsledný adukt CH3-Och2-Chvály2• Zachyťte vodík z Cho3OH a tvorí metyl Etil éter Cho3-Och2-Chvály3.
Štúdium tohto typu reakcií na ožarovanie elektrónov je užitočné v oblasti biochémie, pretože sa zistilo, že poškodenie DNA môže spôsobiť alebo v oblasti organometalickej chémie, pretože uprednostňuje tvorbu nanoštruktúr.
Môže vám slúžiť: Zráža saOkrem toho je známe, že veľké množstvo sekundárnych elektrónov sa vyrábajú, keď elektromagnetické alebo časticové žiarenie interaguje s kondenzovanou hmotou vo vesmíre.
Odhaduje sa preto, že tieto elektróny môžu iniciovať chemické transformácie vo veci medzihviezdneho prášku. Preto je dôležitosť štúdia metyl etil éteru v týchto reakciách.
Potenciálne použitie v polovodičoch
Prostredníctvom metód výpočtovej výpočtu niektorí vedci zistili, že metoxyetán alebo metyléter sa dajú adsorbovať grafénom dotknutým galliom (GA) (všimnite si, čo sa adsorpcia líši od absorpcie).
Grafén je nanomateriál tvorený atómami uhlíka, ktoré sú usporiadané a vytvárajú hexagonálny vzor.
 Mikroskopický grafén. Maido Merisalu [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]. Zdroj: Wikipedia Commons.
Mikroskopický grafén. Maido Merisalu [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]. Zdroj: Wikipedia Commons. Adsorpcia metoxyetánu na doprednom graféne dochádza k interakcii medzi kyslíkom éteru a atómom gália, ktorý je na povrchu nanomateriálu. V dôsledku tejto adsorpcie dochádza k čistému prenosu zaťaženia z éteru do gália.
Po adsorpcii metyletyléteru a vďaka prenosu zaťaženia sa grafén dopreduje s gália.
Riziká
Metoxietano je vysoko horľavý.
Zostávajúcou v kontakte so vzduchom má tendenciu tvoriť nestabilné a výbušné peroxidy.
Odkazy
- Alebo.Siež. Lekárska knižnica. (2019). Etylmetyléter. Získané z: pubchem.Ncbi.NLM.NIH.Vláda.
- Irvine w.M. (2019) ethylmetyléter (C2H5Okradnúť3). In: Gargaoud M. a kol. (Eds). Encyklopédia astrobiológie. Springer, Berlín, Heidelberg. Odkaz obnovený.Prubár.com.
- Tretí b. a kol. (2015). Hľadanie trans etylmetyl -etera v Orion KL. Astronómia a astrofyzika. 582, L1 (2015). NCBI sa zotavila.NLM.NIH.Vláda.
- Filseth, s.Vložka. (1969). Ortuť 6 (3P1) Fotosenzitizovaný rozklad metyl ether éteru. Časopis fyzikálnej chémie. Zväzok 73, číslo 4, apríl 1969, 793-797. Získané z krčiem.ACS.orgán.
- Casanova, J.Jr. (1963). Príprava študentov a manipulácia s plynovou metyl ether éter. Journal of Chemical Education. Zväzok 40, číslo 1, január 1963. Získané z krčiem.ACS.orgán.
- Ure, w. a mladý, J.Tón. (1933a). Na mechanizme plynných reinokencií. Jo. Tematický rozklad metyletyléteru. The Journal of Physical Chemistry, zv. Xxxvii, nie.9: 1169-1182. Získané z krčiem.ACS.orgán.
- Ure, w. a mladý, J.Tón. (1933b). Na mechanizme plynných reinokencií. Ii. Homogénna katalýza v rozkladu metódy ether ether. The Journal of Physical Chemistry, 37, 9, 1183-1190. Získané z krčiem.ACS.orgán.
- Shokuhi rad, a. a kol. (2017). Štúdia DFT o adsorpcii dietyl, ethylmetyl a dimetyteteteri na povrchu grafénu dopovaného s gáliami. Aplikovaná povrchová veda. Zväzok 401, 15. apríla 2017, strany 156-161. Zotavené z vedeckých pracovníkov.com.
- Schmidt, f. a kol. (2019). Elektrónovo indukovaná tvorba etylmetyléteru v kondenzovaných zmesiach metanolu a etylénu. J. Fyzický. Chem. A 2019, 123, 1, 37-47. Získané z krčiem.ACS.orgán.

