Metyl alebo metylová skupina

- 780
- 101
- Adrián Fajnor
On Metyl alebo metylová skupina Je to alquilic substituent, ktorého chemický vzorec je cho3. Je to najjednoduchšie zo všetkých sýtených substituentov v organickej chémii, má jeden uhlík a tri vodíny; pochádza z plynu z metánu. Pretože môže byť spojený iba s iným uhlíkom, jeho poloha naznačuje koniec reťazca, jeho ukončenie.
Na obrázku nižšie máte pre túto skupinu jedno z mnohých reprezentácií. Sinuosity po vašej pravici naznačujú, že za odkazom H3C- môže existovať akýkoľvek atóm alebo substituent; Alkyl, R, Aromatic alebo Arilo, AR alebo heteroátomo alebo funkčná skupina, ako je OH alebo CL.
 Metylová skupina je najjednoduchšia z karbonovaných substituentov v organickej chémii. Zdroj: SU-NO-G [verejná doména]
Metylová skupina je najjednoduchšia z karbonovaných substituentov v organickej chémii. Zdroj: SU-NO-G [verejná doména] Keď funkčná skupina spojená s metylom je OH, máme metanolový alkohol, Cho3Oh; A ak je to CL, potom budeme mať metylchlorid, chlo3Cl. V organickej nomenklatúre sa uvádza jednoducho ako „metyl“, ktorému predchádza počet jeho polohy v najdlhšom uhlíkovom reťazci.
Skupina metilo ch3 It is easy to identify during organic structures elucidations, especially thanks to carbon nuclear magnetic resonance spectroscopy 13 (RMN C (RMN C13). Z toho sa po silných oxidáciách získajú skupiny kyselín COOH, ktorá je syntetickou cestou na syntézu karboxylových kyselín.
[TOC]
Zastúpenie
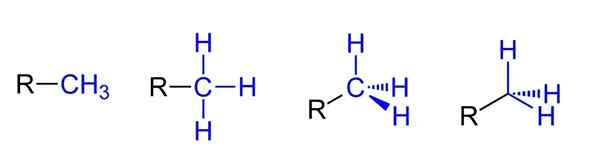 Možné znázornenia pre metylovú skupinu. Zdroj: Jü cez Wikipedia.
Možné znázornenia pre metylovú skupinu. Zdroj: Jü cez Wikipedia. Hore máte štyri možné znázornenie, ktoré predpokladajú, že CHO3 Je spojený s rico substituent r. Všetky sú rovnocenné, ale zatiaľ čo priestorové aspekty molekuly idú zľava doprava.
Napríklad R-CH3 vyvoláva dojem, že je plochý a lineárny. Nasledujúce znázornenie demonštruje tri kovalentné väzby C-H, ktoré umožňujú identifikovať metyl v akejkoľvek Lewisovej štruktúre a vyvolávajú falošný dojem, že je krížom.
Môže vám slúžiť: čo je Erristeneo?Potom, podľa pravice (predposledná), sa pozoruje hybridizácia SP3 V aute Caron3 Kvôli svojej tetraedrálnej geometrii. V poslednej reprezentácii nie je chemický symbol uhlíka ani napísaný, ale tetrahedron je udržiavaný, aby naznačoval, ktoré atómy H sú predné alebo za rovinou.
Aj keď to nie je na obrázku, v čase reprezentácie Cho3 Skladá sa z jednoduchého umiestnenia skriptu (-) „nahý“. To je veľmi užitočné, keď sa nakreslia veľké uhlíkové kostry.
Štruktúra
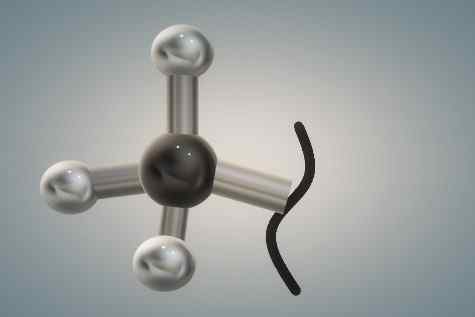 Štruktúra metylovej skupiny predstavovaná sférami a stĺpcovými modelmi. Zdroj: Gabriel Bolívar.
Štruktúra metylovej skupiny predstavovaná sférami a stĺpcovými modelmi. Zdroj: Gabriel Bolívar. Horný obrázok je trojrozmerná reprezentácia prvého. Čierna a lesklá guľa zodpovedá atómu uhlíka, zatiaľ čo biele sú atómy vodíka.
Uhlík má opäť tetraedrický prostredie produktu svojej hybridizácie SP3, A ako taká je to relatívne objemná skupina s rotáciou jej stericky zabráneného spojenia C-R; To znamená, že sa nemôže otáčať, pretože biele gule by zasahovali do elektronických oblakov ich susedných atómov a cítili by ich odporu.
Odkazy C-H však môžu vibrovať, rovnako ako odkaz C-R. Preto CHO3 Je to skupina tetraedrálnej geometrie, ktorú je možné objasniť (určiť, zistiť) infračervenou radiačnou spektroskopiou (IR), rovnako ako všetky funkčné skupiny a uhlíkové väzby s heteroátomosom.
Najdôležitejšou vecou je však jej objasnenie prostredníctvom NMR13. Vďaka tejto technike je stanovené relatívne množstvo metylových skupín, ktoré umožňuje zostavenie molekulárnej štruktúry.
Môže vám slúžiť: hodnotné riešeniaVšeobecne platí, že čím viac skupín ChA3 Mať molekulu, „neohrabanejšie“ alebo neefektívne budú jej intermolekulárne interakcie; To znamená, že maloleté budú jeho topiace sa a varné body. Skupiny Ch3, Kvôli svojim hydrogénom sa „skĺzli“ medzi sebou, keď sa priblížia alebo sa dotýkajú.
Vlastnosti
Metylová skupina sa vyznačuje hydrofóbnou a apolárnou.
Je to preto, že ich väzby C-H nie sú príliš polárne kvôli nízkemu rozdielu medzi elektronickými orgánmi uhlíka a vodíka; A navyše, jej tetraedrálna a symetrická geometria distribuuje svoju elektronickú hustotu takmer homogénne, čo prispieva k opovrhnutiu dipólového momentu.
V neprítomnosti polarity, Cho3 „Voda“ vody, ktorá sa správa ako hydrofóbna. Preto, ak je videný v molekule, bude známe, že tento metylový koniec nebude efektívne interagovať s vodou alebo iným polárnym rozpúšťadlom.
Ďalšia charakteristika CH3 Je to vaša relatívna stabilita. Pokiaľ je atóm, ktorý s ním súvisí s jeho stiahnutím elektronickej hustoty, zostáva prakticky inertná pred veľmi silnými kyslými prostriedkami. Zistí sa však, že sa môže podieľať na chemických reakciách, najmä na jej oxidácii alebo migrácii (metyláciu) na inú molekulu.
Reaktivita
Oxidácia
CH3 nie je oslobodený od oxidácie. To znamená, že je náchylný na formovanie väzieb s kyslíkom, C-O, ak reaguje so silnými oxidačnými činidlami. Keď oxiduje, stáva sa rôznymi funkčnými skupinami.
Napríklad jej prvá oxidácia vedie k skupine Metiol (alebo hydroxymetyl), Cho2Oh, alkohol. Druhý, odvodzuje v skupine Formil, Cho (hc = o), aldehyd. A tretie finále.
Môže vám slúžiť: ionizačná konštantaTáto séria oxidácií sa používa na syntézu kyseliny benzoovej (HOOC-C6H5) Z toluénu (h3Dc6H5).
Ión
CH3 Počas mechanizmu niektorých reakcií môžete vyhrať okamžité elektrické zaťaženie. Napríklad, keď sa metanol zahrieva vo veľmi silnom kyslom médiu, v teoretickej neprítomnosti nukleofilov (pozitívne vyhľadávacie nástroje), tvorí sa metililný katión3+, Pretože odkaz CHO je zlomený3-Ach, vyjde s dvojicou elektrónov väzieb.
Druh ch3+ Je tak reaktívny, že bol schopný určiť iba v plynnej fáze, pretože reaguje alebo zmizne na najmenšiu prítomnosť nukleofilu.
Na druhej strane, Cho3 Je možné získať aj anión: Metanuro, ch3-, Najjednoduchší karbanion zo všetkých. Avšak, ako Cho3+, Jeho prítomnosť je neobvyklá a uskutočňuje sa iba v extrémnych podmienkach.
Metylačná reakcia
Pri metylačnej reakcii sa prenesie CH3 do molekuly bez elektrických nábojov (CHO3+ ani ch3-) v procese. Napríklad metyljodid, Cho3I, je dobré metyntské činidlo a môže nahradiť O-H spojenie niekoľkých molekúl jedným O-CH3.
Pri organickej syntéze to neznamená žiadnu tragédiu; Ale keď to, čo je nadmerne metyl, sú dusíkové bázy DNA.
Odkazy
- Morrison, r. Tón. a Boyd, R, N. (1987). Organická chémia. 5. vydanie. Redakčný Addison-Wesley Inter-American.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. Amín. (10. vydanie.). Wiley Plus.
- Rahul Gladwin. (23. novembra 2018). Metylácia. Encyclopædia Britannica. Získané z: Britannica.com
- Danielle Reid. (2019). Metyl skupina: Štruktúra a receptúra. Štúdium. Získané z: štúdie.com
- Wikipedia. (2019). Metylová skupina. Zdroj: In.Wikipedia.orgán
- « ENEGON VLASTNOSTI, Ako vyrobiť engon, príklady
- Koncept a vzorec molárneho objemu, výpočet a príklady »

