Štruktúra izopentano, vlastnosti, použitie, získanie
- 3266
- 434
- JUDr. Rudolf Čapkovič
On Izopentano Je to organická zlúčenina, ktorej kondenzovaný vzorec je (ch3)2Štiepka2Chvály3. Je to alkan, konkrétne rozvetvený izomér Pentanu, ktorý sa vyznačuje, že je vysoko prchavou tekutinou a používa ako šumivú činnosť. V súčasnosti je jeho najodporúčanejším menom IUPAC 2-metylbután.
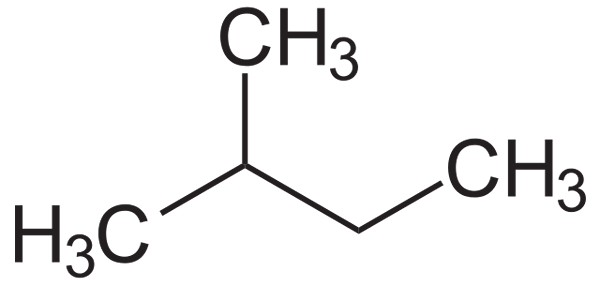
Na spodnom obrázku je vidieť jeho štrukturálny vzorec. Všimnite si, že skupina ch3 účinne je spojený s uhlíkom 2 butylového reťazca. Z izopentana sa získa izopentil alebo izopentilový radikál, ktorý je jedným z najjemnejších alquilitických substituentov, ktoré môžu byť.
 Štrukturálny vzorec izopentanu. Zdroj: Neurotoger / verejná doména
Štrukturálny vzorec izopentanu. Zdroj: Neurotoger / verejná doména Izopentano je apolárna, hydrofóbna a horľavá zlúčenina. Jeho vôňa je podobná ako pri benzíne a je súčasťou jeho zloženia, pretože zvyšuje svoje oktánové alebo oktánové číslo. Získa sa z izomerizačnej reakcie n-Pentano, hoci sa prirodzene dosahuje v niekoľkých množstvách v rezervách zemného plynu.
Izopentano, ktorý ponecháva svoj vysoko horľavý charakter. Človek ho môže prehltnúť a cítiť s mierou skôr, ako predstavuje nežiaduce príznaky, ako je túžba zvracať a závraty. Izopentano sa nachádza v krémoch a kondicionéroch vlasov.
[TOC]
Izopentano štruktúra
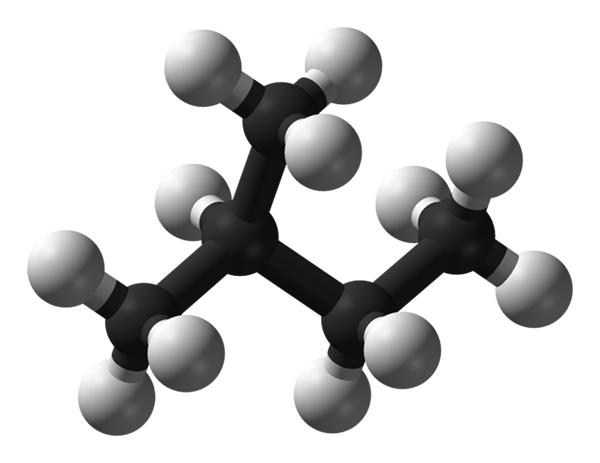 Izopentano molekulárna štruktúra. Zdroj: Benjah-Bmm27 Via Wikipedia.
Izopentano molekulárna štruktúra. Zdroj: Benjah-Bmm27 Via Wikipedia. Na vynikajúcom obraze máme molekulárnu štruktúru izopentanu, reprezentovanú modelom guľôčok a tyčí. Čierne gule zodpovedajú atómom uhlíka, zatiaľ čo biele gule na atóm vodíka. Z jej sýtenej kostry možno povedať, že je robustný, rozvetvený a objemný.
Môže vám slúžiť: reakcia na posunKonce molekuly Isopentano sú chápané skupinami CH3, ktoré sú neefektívne, pokiaľ ide o posilňovanie intermolekulárnych interakcií. Molekuly Isopentano závisia od disperzných síl v Londýne a ich hmotnosti, aby boli schopné zostať súdržné, a tak definovať kvapalinu v normálnych teplotách a tlakových podmienkach.
Jeho geometria a skupiny však3 Sú zodpovední za to, že tekutina Isopentano je vysoko prchavá a privaje pri teplote 28.2 ° C. Napríklad lineárny izomér n-Pentano varí okolo 36 ° C, čo je odrazom svojich najlepších intermolekulárnych interakcií.
Napriek svojej zjavnej robustnosti je molekula Isopentano schopná prijať niekoľko konfigurácií priestoru, čo je kľúčovým faktorom pri stanovovaní jeho skla pri teplote -160 ° C.
Vlastnosti
Fyzický vzhľad
Tekutý alebo bezfarebný plyn s vodným vzhľadom, ktorý tiež dáva vôňu podobnú benzínu. Je to vysoko prchavá látka.
Bod topenia
Izopentano kryštalizuje teplotný interval medzi -161 a -159 ° C.
Bod varu
Izopentano sa vrie v teplotnom intervale medzi 27.8 a 28.2 ° C. Preto je sotva exponovaný mimo vášho nádob.
Tlak vodnej pary
76.9 kPa pri 20 ° C (asi 0.76 ATM)
Hustota
0.6201 g/ml pri 20 ° C. Pary izopentano sú 2.48 hustejšie ako vzduch.
Rozpustnosť
Izopentano za to, že je apolárnou látkou, je nerozpustný a nemiešateľný s vodou a niektorými alkoholmi. Je rozpustný a miešateľný v parafínových rozpúšťadlách, éteroch, tetrachloridu uhlíka a tiež v aromatických tekutinách, ako je toluén.
Môže vám slúžiť: kvartérne zlúčeniny: Charakteristiky, školenie, príkladyIndex lomu
1.354
Povrchové napätie
15 dyn/cm pri 20 ° C
Hrebeň
0.214 CP pri 20 ° C
Bod vzplanutia
-51 ° C. Táto teplota robí izopentano.
Teplota
420 ° C
Žiadosti
 Krémy náklonnosti obsahujú malé množstvá izopentano, ktoré pôsobia ako pohonná látka a dávajú textúru produktu. Zdroj: Pixabay.
Krémy náklonnosti obsahujú malé množstvá izopentano, ktoré pôsobia ako pohonná látka a dávajú textúru produktu. Zdroj: Pixabay. Izopentano je organické rozpúšťadlo, ktoré slúži ako prostriedok reakcie na určitú organickú syntézu a tiež predstavuje surovinu na výrobu iných zlúčenín.
Pridáva sa do benzínu, aby sa zvýšila jeho oktán a do niekoľkých kozmetických výrobkov, aby sa zlepšila jeho textúra, ako sú krémy na holenie, raz sa rýchlo vyparia a opustí bublajúcu hmotu.
Podobne sa v Isopentane zvlhčí polystyrén, takže pri odparovaní sa plast rozširuje a vytvára druh peny, s ktorou plavidlá, modely, platne, podnosy atď.
Na druhej strane sa izopentano používa v kryogénnosti spolu so suchým ľadom a tekutým dusíkom na zmrazenie biologických tkanív a vzoriek.
Získanie
Izopentano je možné získať z nádrží zemného plynu, hoci iba 1% jeho obsahu.
Ďalšia trasa, najpoužívanejšia na priemyselnej úrovni, je založená na n-Destilát Pentán procesov rafinácie oleja. Potom on n-Pentano prechádza špeciálnou reakciou s názvom izomerizácia.
Účel izomerizácie n-Pentano má získať svoje najviac rozvetvené izoméry. Medzi výrobkami teda máme nielen izopentano, ale aj Neopentano. Táto reakcia je možná použitím veľmi špecifických kovových katalyzátorov, ktoré kontrolujú, akú teplotu a aké tlaky sú potrebné.
Môže vám slúžiť: Vlastnosti kovalentných zlúčenín (s príkladmi)Riziká
Izopentano sa považuje za nettoxickú látku. Je to čiastočne kvôli jeho nízkej reaktivite, pretože jej prepojenia C-C alebo C-H nie je ľahké prelomiť, takže v žiadnom metabolickom procese nezasahujú ako také. V skutočnosti je človek schopný vdýchnuť vysoké množstvá svojich výparov pred dusením, bez toho, aby zjavne utrpel poškodenie kolaterálu.
Jeho príjem spôsobuje nevoľnosť a zvracanie a končí jeho kontakt s pokožkou. Na druhej strane lekárske štúdie neboli schopné špecifikovať, či je izopentano karcinogénnou látkou. Považuje sa však za nebezpečnú znečisťujúcu látku pre morské ekosystémy a ich faunu.
Najväčšie nebezpečenstvo okolo Isopentana nie je ani tak jeho reaktivita, ale jeho horľavosť: horí s kyslíkom vzduchu. A pretože jej tekutina je vysoko prchavá, najmenší únik sa oddelí mnohými z jeho výparov smerom k životnému prostrediu, čo zapáli najmenšiu blízkosť plameňa alebo akéhokoľvek iného zdroja tepla.
Preto musia byť výrobky obsahujúce Isopentano uložené v bezpečnom a čerstvom prostredí.
Odkazy
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. (10th Vydanie.). Wiley Plus.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Morrison a Boyd. (1987). Organická chémia. (Piate vydanie). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Izopentán. Zdroj: In.Wikipedia.orgán
- Národné centrum pre biotechnologické informácie. (2020). Izopentán. Databáza pubchem. CID = 6556. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Elsevier B.Vložka. (2020). Izopentán. Vedecký. Zdroj: ScienceDirect.com
- Jennifer B. Galvin a Fred Marashi. (2010). 2-metylbután (izopentán). Journal of Toxikológia a zdravie životného prostredia, súčasť súčasných problémov. Zväzok 58, 1999 -vydanie 1-2. doi.org/10.1080/009841099157403
- « Charakteristiky lipidov, štruktúra, funkcie, príklady
- Charakteristiky profesionálnej etiky, dôležitosť, kód, príklady »

