Chemická zotrvačnosť

- 1157
- 38
- Adrián Fajnor
Čo je chemická zotrvačnosť?
Chemická zotrvačnosť je vlastnosť, ktorá má látku alebo materiál, ktorá odoláva degradácii spôsobenej vonkajšími látkami. V tomto zmysle zostávajú jeho fyzikálne vlastnosti a najmä chemikálie nezmenené. Neexistujú žiadne prestávky na odkazy alebo formovanie nových.
Teraz je chemická zotrvačnosť relatívna. Niektoré látky alebo materiály sú inertnejšie ako iné, čo je spôsobené povahou a silou ich interakcií. Ako v zásade, v zásade kontrastovať s javmi zmeny, nevyhnutné, aby sa hmota vyvíjala v rôznych výrobkoch.
 Zlato nahliadnuť. Zlato je korózia odolnejší kov
Zlato nahliadnuť. Zlato je korózia odolnejší kov Preto, akokoľvek inerte, že ide o látku alebo materiál, vždy bude existovať stav, za ktorého sa stane reaktívny. Napríklad zlato je najušľachtilejší z kovov a považuje sa za inertné. Je však napadnutý a rozpustený Royal Water, riešenie, na ktoré je veľmi reaktívny.
Možno a doteraz jediným chemickým prvkom, ktorý preukázal absolútnu chemickú zotrvačnosť, je neón. Nie je známa žiadna zlúčenina, dokonca ani za ultrapressurových podmienok, ako sú napríklad v jadrách planét alebo mesiacov.
Charakteristiky chemickej zotrvačnosti
Nedostatok oxidácie
Aby bol materiál alebo látka inertné, v zásade by nemalo reagovať s okolitým vzduchom. To znamená, že nemá tendenciu tvoriť väzby s molekulami kyslíka alebo dusíka, ktoré obklopujú jeho povrch. Inými slovami: neoxidujte vystavenie vzduchu.
Jedlo a všetky príslušné organické látky majú tendenciu oxidovať. Preto sa hovorí, že nie sú inertné.
Nedostatok oxidácie v chemickej zotrvačnosti by sa mal udržiavať pri teplotách vyšších ako 100 ° C. Čím vyššia je teplota, látky alebo materiály sa začnú oxidovať rýchlejšie a reagujú s kyslíkom alebo dusíkom vzduchu za vzniku oxidov alebo dusičnanov.
Rezistencia na kyselinu alebo alkalis
Ďalším znakom prítomným v chemickej zotrvačnosti je rezistencia na kyseliny alebo základne. To znamená, že inertná látka alebo materiál by mali odolávať útoku kyselín, bez tendencie degradovať sa akceptovaním H iónov+ alebo veľmi silné elektrofily; alebo útok základní, bez toho, aby sa degradoval kvôli OH ión-.
Môže vám slúžiť: Kyselina perbromová (HBRO4): Vlastnosti, riziká a použitiaOpäť je to relatívne, pretože existujú rôzne typy kyselín a základní. Niektoré inertné látky môžu byť veľmi odolné voči kyseline sírovej, ale sú degradované namiesto dolnej kvapky kyseliny fluórovej. To je prípad sklenených fliaš, keď reagujú s HF.
Elektronická stabilita
Vyššie uvedené charakteristiky súvisia s termodynamickou stabilitou odvodenou z povahy intermolekulárnych interakcií, okrem iných faktorov. Na druhej strane, chemická zotrvačnosť sa tiež pozerá do elektronických charakteristík rovnakých atómov.
Čím stabilnejšia je elektronická konfigurácia atómu, tým nižšia je tendencia vyhrať alebo stratiť elektróny. Preto bude vykazovať väčšiu chemickú zotrvačnosť. Toto je prípad šľachetných plynov, ktoré sa objavia v nasledujúcej časti.
Bioinaktivita
V medicíne je látka alebo materiál inertná, ak nemá biologickú aktivitu. To znamená, že sa môže nachádzať vo vnútri organizmu bez toho, aby bol asimilovaný počas jeho metabolizmu. Táto vlastnosť je veľmi žiaduca v kostných protézach alebo v rekonštrukcii tkanív.
Odpor
Nakoniec, inertné látky alebo materiály by mali byť tiež odolné voči žiareniu, ultrafialové alebo jadrové.
Príklady chemickej zotrvačnosti
Pohár
 Sklo je relatívne inertný materiál
Sklo je relatívne inertný materiál Medzi príkladmi materiálov, ktoré vykazujú chemickú zotrvačnosť, máme sklo. Keby neboli inertné, neslúžili by na vypracovanie kontajnerov alebo kontajnerov, pretože by reagovali s ich obsahom. V závislosti od ich zloženia, ako sú borosilikáty, sa môžu stať veľmi odolnými voči korózii a teplote.
Ako je však uvedené na začiatku, sklo nie je imunné voči všetkým látkam: reaguje s HF, dokonca zriedeným, horúce alkalis, ako sú NaOH a H3Po4 Veľmi koncentrované a horúce.
Môže vám slúžiť: pyrolýzaPlasty
 Keby teflónova panvica nebola inertná, pokazilo by to všetky jedlá, ktoré sme v nej uvarili. Zdroj: Mdevicente, CC0, cez Wikimedia Commons
Keby teflónova panvica nebola inertná, pokazilo by to všetky jedlá, ktoré sme v nej uvarili. Zdroj: Mdevicente, CC0, cez Wikimedia Commons Plasty tiež spĺňajú funkcie podobné funkciám skla, ale existuje oveľa viac všestranných (tak ľahko sa nerozbijú). Niektoré plasty, ako je teflón (polytetrafluóretylén), kynar (polyvinylidén fluorid) a telene (polydiccyclopentadién), sú mimoriadne rezistentné na útok kyselín a korózie.
Keramika
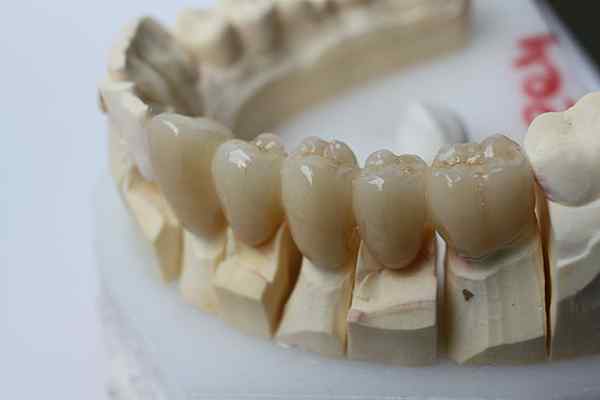 Chemická zotrvačnosť zirkónia umožňuje jeho použitie na zubné protézy. Zdroj: Bin Im Garten cez Wikipedia.
Chemická zotrvačnosť zirkónia umožňuje jeho použitie na zubné protézy. Zdroj: Bin Im Garten cez Wikipedia. Inertná keramika ide o krok ďalej ako plasty. Sú určené pre aplikácie, v ktorých prevažujú vysoké teploty, v automobilovom priemysle a leteckom priemysle; alebo v biochemických systémoch, rovnako ako vo farmaceutickom priemysle a pri implementácii protéz kostí.
Medzi niektorými z týchto keramiky s veľkou chemickou zotrvačnosťou, ktorú máme: hlinit (do2Ani3, Prítomné v Corindone a Sapphire), kremičitany (špecializované sklo), karbid kremíka (sic, tvrdý a húževnatý) a zirkón (Zio2).
Inertné plyny
Necháme inertné materiály stranou, teraz máme inertné látky. Inertné plyny nie sú príliš reaktívne, takže ich prítomnosť vo vzduchu neznamená žiadne riziko reakcie za normálnych podmienok.
Medzi týmito plynmi máme CO2, Co a n2. Dusík je najviac inertný zo všetkých týchto plynov; A napriek tomu je schopný reagovať horúco s niektorými kovmi za vzniku dusičnanov, m3Nn, bytosť n Stav oxidácie kovov alebo kovov.
CO2 Je relatívne inertný; S výnimkou prípadov, keď sa stretáva s alkalickými roztokmi, kde sa transformuje na uhličitany alebo v prítomnosti anhydraických enzýmov uhoľných uhlí.
Pokiaľ ide o svoju časť, CO zostáva inertná pri izbovej teplote; Ale pri vysokých teplotách reaguje s uhlím, vodnou parou, oxidmi kovov, olefínmi, medzi inými zlúčeninami.
Môže vám slúžiť: Chemická rovnováha: Vysvetlenie, faktory, typy, príkladyTakéto reakcie môžu pokračovať v prítomnosti kovových katalyzátorov. Podobne je Co, aj bez porušenia svojich kovalentných väzieb, schopná koordinovať neutrálne atómy kovov.
Ušľachtilé kovy
Ušľachtilé kovy sú najodotívnejšie voči korózii a útoku na kyseliny a alkalis. Každý, pri vysokých teplotách alebo vo formáte prachu, bude reagovať s kyslíkom alebo fluoridom. Preto je chemická zotrvačnosť týchto prvkov pomerne relatívna.
Medzi ušľachtilé kovy, ktoré máme: Gold (Au), Ruthenio (RU), Platinum (PT), Paladio (PD), Osmio (OS) a Iridido (IR). Zo všetkých je zlato najušľachtilejšie, dokonca aj v kovovom stave v zemskej kôre.
Šľachetné plyny
A nakoniec, v najvyššom sedadle chemickej zotrvačnosti máme ušľachtilé plyny: hélium (HE), neón (NE), argón (AR), Crypton (KR), xenón (XE) a Radon (RN). Všetky sú mimoriadne inertné. Mnoho zlúčenín xenónu však bolo syntetizovaných, vrátane solí známych ako Perxenatos, s aniónom XEO64-.
 Neónové svetlá zodpovedajú najrôznejším chemickým prvkom prírody
Neónové svetlá zodpovedajú najrôznejším chemickým prvkom prírody Jeho chemická zotrvačnosť je preto, že ich atómy obsahujú svoju energiu a orbitálne vrstvy úplne plné elektrónov. Z argónu je možné, že pri ultrapresiách budú mať prístup k elektrónom pomocou prázdnych orbitálnych alebo viacerých energetických vrstiev (napríklad 3D a 4S); vec, ktorá je nemožná pre hélium alebo neón.
Noble Plyns Presne hélium a neón sú najviac inertné. Hélium je schopné tvoriť zlúčeniny sodíkom na veľmi vysoké tlaky (Hena).
Medzitým nie je vôbec známa žiadna zlúčenina, ktorá je ešte viac inertná ako samotná hélium kvôli jeho účinnejšiemu jadrovému zaťaženiu, čo silne odpudzuje akýkoľvek atóm, ktorý sa snaží priblížiť k neónovým atómom.
Odkazy
- Whitten, Davis, Peck & Stanley. (2008). Chémia. (8. vydanie.). Učenie sa.
- Triasť a Atkins. (2008). Inorgán chémiaICA. (Štvrté vydanie). MC Graw Hill.
- Wikipedia. (2020). Chemicky inertný. Zdroj: In.Wikipedia.orgán
- DR. Doug Stewart. (2020). Definícia inertného. Získané z: Chemicool.com
- Elsevier B.Vložka. (2020). Chemická inerct. Vedecký. Zdroj: ScienceDirect.com
- Clara Moskowitz. (20. marca 2018). Prekvapenie vznešeného plynu: hélium môže tvoriť podivné zlúčeniny. Zotavené z: vedeckého Američana.com
- Coorstek. (2020). Chemické vlastnosti technickej keramiky. Získané z: Coorstek.com
- Osborne priemysel. (2020). 3 najviac kyslé odolné voči plastom. Získané z: Osborneindustries.com

