Charakteristiky Guaniny, štruktúra, školenie a funkcie
- 5072
- 726
- Tomáš Klapka
Ten Guanina Je to dusíkavá báza, ktorá slúži na biosyntézu 5'-monofosfátového guanilátu. Obe látky sú súčasťou RNA a DNA, ktoré ukladajú genetické informácie o bunkách.
Kyselina ribonukleová (RNA) a kyselina deoxyribonukleová (DNA) sú tvorené nukleotidmi, ktoré sú tvorené dusíkovou bázou pripojenou k cukru a fosfátovej skupine.
 Zdroj: Neurotoger [verejná doména]
Zdroj: Neurotoger [verejná doména] Guanín, okrem toho, že je súčasťou nukleových kyselín, v ich monofosfátovom, difosfátovom a trojfázovom nukleozidoch (GMP, GDP a GTP) sa podieľa na procesoch, ako je energetický metabolizmus, translácia intracelulárneho signálu, fyziológia fotoreceptorov a fúzia vezikulov.
[TOC]
Chemická štruktúra
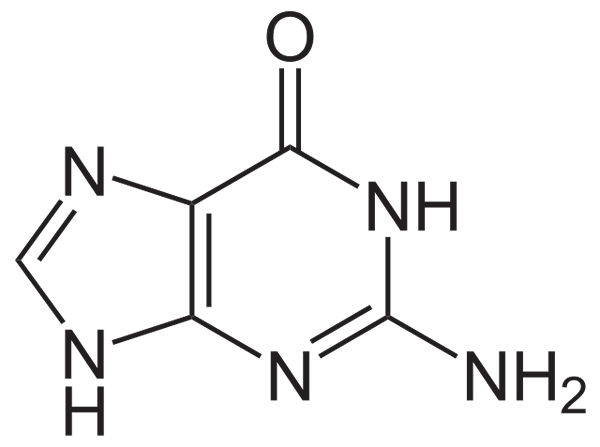
Chemická štruktúra guanínu (2-amino-6-hydroxipurín) je heterocyklický purínový kruh, ktorý pozostáva zo systému s dvoma krúžkami: Jeden kruh je pyrimidín a druhý kruh je imidazole.
Heterocyklický prsteň guanínu je plochý a s niektorými dvojitými konjugovanými odkazmi. Okrem toho má dve tautomérne formy, keto a enolovú formu, medzi skupinami C-1 a N-6.
Charakteristika
Charakteristiky guanínu sú:
- Guaníny je apolárna látka. Je nerozpustný vo vode, ale je rozpustný v koncentrovaných roztokoch kyselín alebo silných báz.
- Môže byť izolovaný ako biela tuhá látka s empirickým vzorec5H5N5Alebo a molekulová hmotnosť 151,3 g/mol.
- Vlastnosť absorbujúceho svetla pri 260 nm DNA je čiastočne spôsobená chemickou štruktúrou guanínu.
- V DNA tvorí guaníny tri vodíkové väzby. Skupina Carbonyl C-6 je akceptorom vodíka, skupina N-1 a aminokry C-2 sú darcovia vodíkových väzieb.
Z tohto dôvodu je potrebných viac energie na prelomenie prepojenia medzi guanínom a cytozínom, ako je adenín s timinom, pretože tento moment je spojený iba dvoma vodíkovými mostmi.
Môže vám slúžiť: elektroforéza: základ, technika, na čo je, príklady- V bunke je vždy súčasťou nukleových kyselín alebo ako GMP, HDP a GTP, nikdy vo svojej voľnej forme.
Biosyntéza
Guanínová molekula, rovnako ako iné puríny, je syntetizovaná novo Z 5-fosforibozyl-1-pyrofosfátu (PRPP), enzýmom katalyzovanými reakciami.
Prvý krok spočíva v pridaní aminoskupiny, od glutamínu, po PRPP a tvorí 5-fosforibosylamín (PRA).
Následne v usporiadanej sekvencii sa vyskytuje pridanie glycínu, aspartátu, glutamínu, formovania a oxidu uhličitého do PRA. Týmto spôsobom sa tvorí medziprodukt metabolit nazývaný Inosina 5'-monofosfát (IMP).
Počas tohto procesu sa používa voľná energia hydrolýzy ATP (adenozín 5'-triffosfát), ktorá produkuje ADP (adenozín 5'-Diaphypho) a PI (anorganický fosfát).
Oxidácia impondy na NAD+ (Nikotínamid a adenín dinukleotid), produkuje xantín 5'-monofosfát (XMP). Následné pridanie aminoskupiny do XMP produkuje molekulu Guanilaato.
Regulácia biosyntézy guanilaato sa vykonáva na začiatku, keď sa vytvorí PRA, a nakoniec, keď dôjde k oxidácii IMPE. Regulácia sa vyskytuje negatívnou spätnou väzbou: Nukleotid GMP inhibuje enzýmy v oboch štádiách.
Počas metabolickej degradácie nukleotidov sa recyklujú dusíky. GMP je tvorený hypoxantín-keepanínovými enzýmom fosforibosyltransferáza, ktorá prenáša fosribozylovú skupinu z PRPP do guanínu.
Funkcia
Pretože guaníny sa nenachádza vo svojej voľnej forme, jeho funkcie sú spojené s GMP, HDP a GTP. Niektoré z nich sú uvedené nižšie:
- Guanozín 5'-triffosfátu (GTP) pôsobí ako rezervoár voľnej energie. Skupina gama fosfátu GTP sa môže preniesť na adenozín 5'-trifosfát (ADP), aby sa vytvorila ATP. Táto reakcia je reverzibilná a je katalyzovaná nukleozidnou difosfátovou kinázou.
Môže vám slúžiť: beta galaktozidáza: charakteristiky, štruktúra, funkcie- GMP je najstabilnejšia forma nukleotidu obsahujúceho guaninu. Prostredníctvom hydrolýzy tvorí GMP cyklický GMP (GMPC), čo je druhý posol počas intracelulárneho značenia, v translačných cestách. Napríklad v bunkách zápachu a chemiorreceptorových buniek zápachu.
- GMPC sa podieľa na relaxácii krvných ciev hladkého svalstva počas biosyntézy oxidu dusnatého v endotelových bunkách.
- Hydrolýza fosfátu GTP gama slúži ako zdroj voľnej energie pre biosyntézu proteínov v ribozómoch.
- Enzýmy helikázy potrebujú voľnú energiu hydrolýzy GTP na oddelenie dvojitého DNA vrtule, počas replikácie a transkripcie DNA.
- V neurónoch hippocampu je pôsobenie sodíkových kanálov závislých od napätia regulované hydrolýzou GTP na HDP.
Súvisiace choroby
Vysoké hladiny kyseliny krvi a moču a moču boli spojené s tromi rôznymi metabolickými defektmi, ktoré uvidíme nižšie.
Syndróm Lesch-Nyhan
Vyznačuje sa nedostatkom HPRT (hypoxantín-guaddibozyltransferáza), dôležitým enzýmom na recykláciu hypoxantínu a guanínu. V tomto prípade zvyšuje hladiny PRPP a nevytvára IMP a GMP, dva dôležité regulátory počiatočného štádia syntézy purínu. To všetko uprednostňuje biosyntézu novo puríny.
Aktivita PRPP rozšírená syntáza
To vedie k zvýšeniu hladín PRPP. Tento metabolit pôsobí ako aktivátor gutamínu PRPP-amidotranferázy, ktorá je zodpovedná za syntézu 5-fosforibosyllamínu, zvyšujúca sa biosyntéza novo purín.
Môže vám slúžiť: Sfingomyeline: Čo je, štruktúra, funkcie, syntézaSyndróm von Gierke
Je to choroba súvisiace s ukladaním glykogénu typu I. Pacienti trpiaci týmto syndrómom majú defektnú 6-fosfatázovú glukózu. To vedie k zvýšeniu hladín 6-fosfátu glukózy, ktorá slúži na syntézu 5-fosfátového ribózy prostredníctvom pentózového fosfátu.
5-fosfátový ribóza je počiatočný metabolit pre biosyntézu PRPP. Podobne ako v predchádzajúcich dvoch prípadoch to vedie k zvýšeniu biosyntézy novo puríny.
Zvýšenie kyseliny močovej v krvi a moči spôsobuje príznaky, ktoré sa bežne nazývajú dna. V prípade syndrómu Lesch Nyhan pacientom úplne chýba aktivita enzýmu HPRP, čo vedie k prejavu ďalších príznakov, ktoré zahŕňajú ochrnutie a mentálnu retardáciu.
Gén HPRP sa nachádza na X chromozóme. Preto mutácie v tomto géne ovplyvňujú mužov. Neexistuje žiadna liečba na liečbu neurologických problémov. Príznaky spojené so zvýšením kyseliny močovej sú liečené alopurinolom.
Odkazy
- Dawson, R. a kol. 1986. Údaje pre biochemický výskum. Clarendon Press, Oxford.
- Horton, R; Moran, L; Scrimgeour, G; Perry, m. A Rawn, D. 2008. Zásady biochémie. 4. vydanie. Pearson Vzdelanie.
- Mathews, Van Holde, Ahern. 2001. Biochémia. 3. vydanie.
- Murray, R; Granner, D; Mayes, P. A Rodwell, v. 2003. Harperova ilustrovaná biochémia. 26. vydanie. Spoločnosti McGraw-Hill.
- Nelson, DL a Cox, M. 1994. Lehninger. Zásady biochémie. 4. vydanie. Ed Omega.
- Sigma-Aldrich. 2019. Chemický list. Word Wide Web Address: Sigmaaldrich.com.

