Rozptýlená fáza
- 654
- 98
- MUDr. Žigmund Boška
 Zdroj: Gabriel Bolívar
Zdroj: Gabriel Bolívar Aká je rozptýlená fáza?
Ten rozptýlená fáza Je to ten, ktorý má menší podiel v disperzii a je zložený z veľmi malých agregátov častíc. Medzitým sa najhojnejšia a nepretržitejšia fáza, v ktorej sa častice ležia, nazývaná disperzovacia fáza. Príkladom je voda s cukrom, kde by dispergovaná fáza bola cukor a dispergová voda.
Disperzie sa klasifikujú podľa veľkosti častíc, ktoré tvoria rozptýlenú fázu a sú schopné rozlíšiť tri typy disperzií: hrubé disperzie, koloidné riešenia a skutočné riešenia.
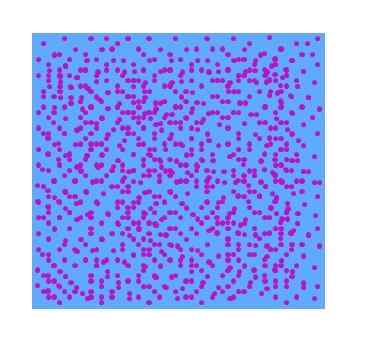
Na vynikajúcom obraze je možné vidieť hypotetickú dispergovanú fázu fialových častíc vo vode. Výsledkom je, že sklo plné tejto disperzie nevykazuje priehľadnosť viditeľného svetla; to znamená, že to bude vyzerať ako fialový tekutý jogurt. Typ disperzií sa líši v závislosti od veľkosti týchto častíc.
Keď sú „skvelé“ (10-7 m) Hovorí sa o hrubých disperziách a môže sedimentovať pôsobením gravitácie; koloidné roztoky, ak sa ich veľkosti pohybujú medzi 10-9 M a 10-6 M, čo ich zviditeľňuje iba ultramikroskopom alebo elektronickým mikroskopom; a skutočné riešenia, ak sú ich veľkosti menšie ako 10-9 M, byť schopný krížiť membrány.
Skutočné riešenia sú preto všetky známe, ako napríklad ocot alebo sladká voda.
Charakteristiky rozptýlenej fázy
Riešenia predstavujú konkrétny prípad disperzií, ktoré sú veľmi zaujímavé pre znalosť fyzioquimice živých bytostí. Väčšina biologických látok, intracelulárnych aj extracelulárnych, sa nachádza vo forme disperzií volania.
Brownov pohyb a Tyndall efekt
Častice dispergovanej fázy koloidných roztokov majú malú veľkosť, ktorá brzdí ich sedimentáciu. Okrem toho sa častice neustále pohybujú v náhodnom pohybe a navzájom sa zrážajú, čo tiež sťažuje sedimentáciu. Tento typ pohybu je známy ako Brownian.
Môže vám slúžiť: fialové skloV dôsledku relatívne veľkej veľkosti častíc dispergovanej fázy majú koloidné roztoky kalný alebo dokonca nepriehľadný vzhľad. Je to preto, že svetlo je rozptýlené, keď koloid kríži, jav známy ako Tyndall Effect.
Heterogenita
Koloidné systémy sú nehomogénne systémy, pretože dispergovaná fáza sa skladá z častíc s priemerom medzi 10-9 M a 10-6 m. Zatiaľ čo častice roztoku majú menšiu veľkosť, zvyčajne menej ako 10-9 m.
Častice dispergovanej fázy koloidných roztokov môžu prechádzať filtračným papierom a hlineným filtrom. Ale nemôžu krížiť dialyzačné membrány, ako je celofán, kapilárny endotel a kolódium.
V niektorých prípadoch sú častice, ktoré tvoria dispergovanú fázu, proteíny. Keď sa nachádzajú vo vodnej fáze, proteíny sa zložia a hydrofilnú časť zanechávajú vonku pre väčšiu interakciu s vodou, cez iónové dipolo sily alebo s tvorbou vodíkových mostov.
Proteíny tvoria retikulárny systém vo vnútri buniek, ktorý je schopný prevziať časť dispergátora. Okrem toho povrch proteínov slúži na spojenie malých molekúl, ktoré pripisujú povrchový elektrický náboj, ktorý obmedzuje interakciu medzi molekulami proteínov, čo im bráni v tvorbe zrazenín, ktoré spôsobujú sedimentáciu.
Stabilita
Koloidy sú klasifikované podľa príťažlivosti medzi dispergovanou fázou a dispergáciou fázy. Ak je dispergácia fáza tekutá, koloidné systémy sa klasifikujú ako slnko. Tieto sú rozdelené do deliphilos a liofóbov.
Môže vám slúžiť: chlorečník draselného (KCLO3)Liofilové koloidy môžu tvoriť skutočné roztoky a sú termodynamicky stabilné. Na druhej strane koloidy Liophobes môžu tvoriť dve fázy, pretože sú nestabilné, aj keď sú stabilné z kinetického hľadiska. To im umožňuje dlho zostať v rozptýlenom stave.
Dispergované príklady fázy
Disperzná fáza aj dispergovaná fáza sa môže vyskytnúť v troch fyzikálnych stavoch veci, to znamená: pevná, kvapalná alebo plynná.
Za normálnych okolností je kontinuálna alebo dispergácia v kvapalnom stave, ale koloidy, ktorých zložky sa nachádzajú v iných stavoch agregácie hmoty.
Možnosti kombinácie dispergovej fázy a rozptýlenej fázy v týchto fyzických štátoch sú deväť.
Každý z nich bude vysvetlený niekoľkými príslušnými príkladmi.
- Solídne riešenia: Keď je dispergácia fáza pevná, môže sa kombinovať s dispergovanou fázou v tuhom stave, čím sa vytvorí So -zavolané tuhé roztoky.
Toto sú príklady týchto interakcií: mnoho oceľových zliatin s inými kovmi, niektoré farebné drahokamy, zosilnenú gumu, porcelán a pigmentované plasty.
- Pevné emulzie: Fáza dispergovania tuhého stavu sa môže kombinovať s fázou dispergovanou kvapalinou, ktorá tvorí So -založené tuhé emulzie. Sú to príklady týchto interakcií: syr, maslo a želé.
- Tuhé peny: Disperzná fáza ako pevná látka sa môže kombinovať s dispergovanou fázou v plynnom stave, ktorá predstavuje So -zavolané tuhé peny. Príkladmi týchto interakcií sú špongia, guma, pemza a gumová pena.
- Podrážky a gély: Disperzná fáza v stave kvapalného stavu je kombinovaná s dispergovanou fázou v tuhom stave, čím sa vytvára slnko a gély. Príkladmi týchto interakcií je magnézia mlieko, maľby, bahno a pudin.
Môže vám slúžiť: Riešenia tlmiča nárazov- Emulzia: Disperzujúca fáza v stave kvapalného stavu je kombinovaná s dispergovanou fázou aj v tekutom stave, ktorý produkuje So -zavolané emulzie. Príkladmi týchto interakcií sú mlieko, krém na tvár, šalátové dresingy a majonéza.
- Peny: Disperzujúca fáza v kvapalnom stave je kombinovaná s dispergovanou fázou v plynnom stave, čím sa vytvára peny. Príkladmi týchto interakcií sú holenie, šľahačka a piva pena.
- Pevné aerosóly: Disperzujúca fáza v plynnom stave je kombinovaná s dispergovanou fázou v tuhom stave, čo spôsobuje So -Called tuhých aerosólov. Príkladmi týchto interakcií sú dym, vírusy, korpuskulárne materiály vo vzduchu, materiály emitované výfukovými rúrkami automobilov.
- Aerosóly: Disperzujúca fáza v plynnom stave sa môže kombinovať s dispergovanou fázou v stave kvapalného stavu, ktorá predstavuje So -zavolané kvapalinové spreje. Príkladmi týchto interakcií sú hmla, hmla a rosa.
- Skutočné riešenia: Disperzná fáza v plynnom stave sa môže kombinovať s plynnou fázou v plynnom stave, čím sa vytvára plynné zmesi, ktoré sú skutočnými roztokmi a nie koloidnými systémami. Príkladmi týchto interakcií sú vzduch a plyn osvetlenia.
Odkazy
- Whitten, Davis, Peck & Stanley. Chémia (8.ª Ed.). Učenie sa.
- Toppr (s.F.). Klasifikácia koloidov. Získané z: Toppr.com
- Jiménez Vargas, J a Macarulla. J. M. (1984). Fyziologická fyzikálna pôsobnosť, šieste vydanie. Inter -American Editorial.
- Madhusha. Rozdiel medzi disperznou fázou a disperznou medom. Získané z: Pediaa.com

