Elektroforéza nadácie, technika, na čo je, príklady

- 3619
- 198
- Václav Višňovský
Ten Elektroforéza Je to technika používaná na oddelenie molekúl v elektrickom poli. Musí urobiť konkrétne s migráciou častíc naložených pod vplyvom elektrického prúdu aplikovaného medzi dvoma pólmi, jeden pozitívny a druhý negatívny.
Elektroforéza je v súčasnosti jedným z najbežnejších postupov, ktoré sa uskutočňujú počas vývoja experimentu, najmä v oblastiach súvisiacich s analytickou chémiou, biochémiou a biologickými a lekárskymi vedami vo všeobecnosti.
 Elektroforéza. Zdroj: Melodygar/CC By-SA (https: // creativeCommons.Org/licencie/By-SA/4.0)
Elektroforéza. Zdroj: Melodygar/CC By-SA (https: // creativeCommons.Org/licencie/By-SA/4.0) Používa sa na oddelenie proteínu, peptidov, DNA, RNA a ďalších podľa ich zaťaženia, veľkosti, hustoty a čistoty.
Rôzne komerčné domy navrhli rôzne formáty s rôznymi aplikáciami a primeranými ziskami na konkrétne účely, všetky postupy si však vyžadujú rovnaké základné prvky:
- Zdroj energie na výrobu elektrického náboja
- Médium podpory pre oddelenie
- Roztok pufra (nárazník) Udržiavať pH konštantné
[TOC]
Základ
Elektroforéza nie je ničím iným ako migrácia (separácia) častíc alebo zaťažených molekúl (prirodzene alebo umelo) v médiu alebo podpora pod vplyvom elektrického poľa.
Táto technika je založená na jednej z hlavných fyzikálnych rovníc elektromagnetizmu, podľa ktorej sa sila rovná elektrickému náboja vynásobené elektrickým poľom aplikovaným v tomto bode (F (sila) = q (elektrický náboj) x e (elektrické pole (elektrické pole) ).
Podľa tejto rovnice sa dve častice s rovnakou hmotnosťou, ale iného zaťaženia, presunú k rôznym rýchlostiam v rovnakom elektrickom poli. Okrem toho rýchlosť pohybu týchto častíc bude závisieť od vzťahu medzi ich zaťažením a hmotnosťou.
Vedci využili tieto vlastnosti a nákladné/masové vzťahy na oddelenie zložiek od biomolekulov v ich najmenších častiach, ako aj na oddelenie rôznych molekúl v zmesi, okrem iného.
Je dôležité si uvedomiť, že biologické molekuly, ako sú aminokyseliny, peptidy, proteíny, niektoré uhľohydráty, nukleotidy a nukleové kyseliny, majú niečo, čo nazývame „ionizovateľné skupiny“, takže môžu existovať ako pozitívne alebo negatívne nabité druhy za určitých podmienok pH pH pH.
Technika
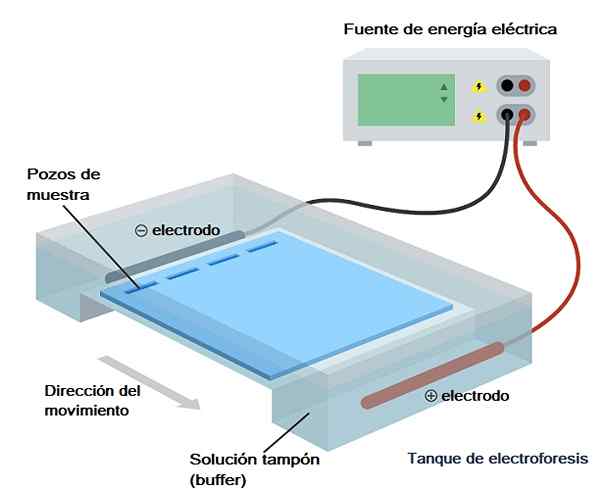
Aj keď existujú rôzne typy elektroforézy, gélová elektroforéza je najpoužívanejšia v biochemickej analýze, molekulárnej biológii a biotechnológii, takže to bude o čom budeme krátko hovoriť z technického hľadiska.
Ako už názov napovedá, gélová elektroforéza znamená použitie tuhého tuhého podporného média, buď na analýzu/separáciu zmesí proteínu alebo nukleových kyselín (DNA a/alebo RNA) pod vplyvom elektrického poľa.
Systém alebo prístroj používaný na vykonanie elektroforetického „behu“ môže byť vodorovná (zvyčajne sa používa na nukleové kyseliny) alebo vertikálne (zvyčajne sa používa na proteín).
- Príklad techniky elektroforézy nukleovej kyseliny
Nukleové kyseliny sa zvyčajne separujú pomocou agarózových gélov (galaktózový polysacharid), ktorý sa pripravuje s primeraným roztokom pufra (Tris/acetát/EDTA alebo Tris/borato/EDTA) a ktorého koncentrácia určí „rozlíšenie“ fragmentov rôznych veľkostí.
Môže vám slúžiť: Zemský potravinový reťazec: Odkazy a príkladpríprava vzorky
Prvým krokom pred vykonaním elektroforetického behu v agarózovom géli je získanie vzorky. Bude to závisieť od experimentálneho konca a vzorky môžu byť produktom enzymatického štiepenia, na polymerázovej reťazovej reakcii (PCR), čistenie nukleových kyselín atď.
 Zmes vzorky s zaťažením buff.Org/licencie/o/4.0) Via Wikimedia Commons)
Zmes vzorky s zaťažením buff.Org/licencie/o/4.0) Via Wikimedia Commons) Po získaní sa to zmieša s farebným roztokom (zaťažovací roztok), ktorý umožňuje rýchle ukladanie vzorky v studni, pretože má glycerol a farbivo, ktoré umožňuje vizuálne beh.
Gélová príprava
Tento krok spočíva v zmiešaní potrebného množstva gelového substrátu (agarózy) s roztokom vyrovnávacej pamäte, jeho roztavení pomocou tepla a jeho tuhosti na podporu, ktorá funguje ako „pleseň“.
Počas gélifikácie sa do gélu zavedú niektoré „hrebene“ umiestnené v „forme“ na vymedzenie „jamiek“, kde sa vzorky zavedú pred behom.
Akonáhle sa gél ochladí a stuhne, „hrebene“ sa odstránia a zavádzajú sa do nádoby známeho ako „vedro“, ktorý je plný bežiaceho roztoku pufra, (TRIS/acetát/EDTA alebo TRIS/Borato/Borato/EDTA).
Táto vedra je zase zahrnutá v tzv. „Elektroforetickej komore“, ktorá nie je ničím iným ako nádobou, cez ktorú prechádza elektrické pole, a ktoré má priestor, kde je zavedený gél, a dve časti, s ktorými sú naplnené Tlmivého roztoku (nárazník spustiť).
Táto kamera má dve elektródy, jednu pozitívnu a jednu negatívnu, z ktorej sa pohyb iónov vyrába po aplikácii elektrického poľa (je pripojený k zdroju energie).
Zaťaženie
Akonáhle sa vzorky zmiešajú s príslušným roztokom zaťaženia, zavedú sa do „jamiek“ predtým vyrobených do gélu.
Pretože nukleové kyseliny majú záporné čisté zaťaženie, migrujú z negatívneho pólu na pozitívny kde boli vzorky naložené.
Čas Corrida je stanovený v prísnej závislosti od výskumného pracovníka zodpovedného za experiment. Napätie sa všeobecne vypočíta v 5 -voltovom pomere za centimeter v géli, ktorý oddeľuje tieto dve elektródy.
Zobrazenie
Keď gél beží (keď vzorky prebehli gél z jedného konca na druhý), je ponorené do roztoku etidného bromidu (ETBR), farbiva, ktoré je rozptýlené medzi nitrogénnymi základňami a že „značka“. Môžu sa vizualizovať v transilumenante pomocou ultrafialového svetla.
Čo je elektroforéza pre?
Elektroforéza sa historicky používala na viacerých účeloch. Dnes však jej užitočnosť do značnej miery závisí od „otázky“, že výskumný pracovník je položený vo vzťahu k javu alebo konkrétnemu systému, ako aj od typu elektroforézy, ktorú chce použiť.
Môže vám slúžiť: topoizomeráza: Čo sú, charakteristiky, funkcie, typyMôžeme však získať niektoré z hlavných funkcií, ktoré táto technika má, počnúc najzriehodnejšími a končiacimi najobľúbenejšími a najčastejšie využívaným vo svete biologických vied. Elektroforéza je užitočná:
- Pre kvantitatívnu analýzu komplexných zmesí makromolekulov a na výpočet potenciálneho „Zeta“ (koloidná vlastnosť častice v kvapalnom médiu pod vplyvom statického elektrického poľa).
- Na analýzu krvných sérov na diagnostické účely.
- Na separáciu glukoproteínov, lipoproteínov a krvného hemoglobínu.
- Na analýzu potravín, farmaceutické výrobky a znečisťujúce látky v oblasti životného prostredia.
Elektroforéza v agarózových géloch
- Na separáciu fragmentov DNA po trávení reštrikčnými enzýmami.
- Na separáciu molekúl nukleových kyselín pred prenosom do membrán pre následné analýzy.
- Na analýzu produktov PCR (polymerázová reťazová reakcia), ktorá overuje, či sa to stalo alebo nie.
- Na odhad veľkosti molekúl v zmesi DNA alebo RNA.
- Pre odhad množstva a/alebo kvality purifikovaných nukleových kyselín.
Elektroforéza v polyakrylamidových géloch za denaturalizujúcich alebo natívnych podmienok
- Na stanovenie veľkosti proteínu.
- Na identifikáciu proteínov.
- Na určenie čistoty vzorky po niekoľkých krokoch čistenia.
- Na identifikáciu prítomnosti intramolekulárnych disulfidových väzieb.
- Na stanovenie interakcie medzi proteínmi.
- Na stanovenie izoelektrického bodu proteínu.
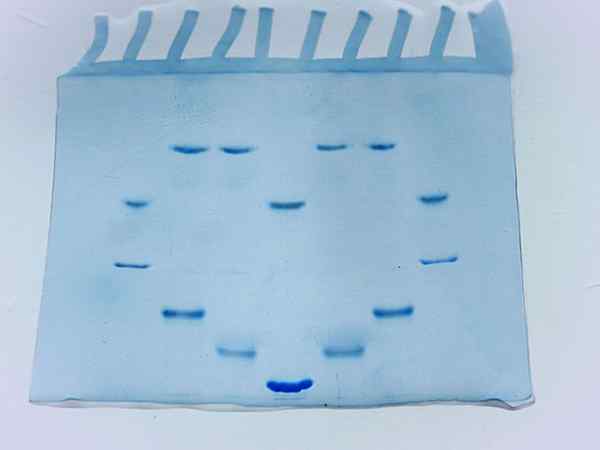 Fotografia akrylamidového gélu po spustení niekoľkých vzoriek proteínov (zdroj: Larionova.Marina/CC BY-SA (https: // creativeCommons.Org/licencie/By-SA/4.0) Via Wikimedia Commons)
Fotografia akrylamidového gélu po spustení niekoľkých vzoriek proteínov (zdroj: Larionova.Marina/CC BY-SA (https: // creativeCommons.Org/licencie/By-SA/4.0) Via Wikimedia Commons) Faktory, ktoré ovplyvňujú elektroforézu
Migrácia častíc v elektrickom poli závisí od rôznych faktorov, medzi ktorými sú:
- Váš elektrický náboj
- Jeho molekulárna veľkosť
- Jeho hydrofóbnosť a jej forma
- Rozsah aplikovaného elektrického poľa
- Teplota systému a iónová sila použitého roztoku pufra
- Povaha prostredia, v ktorom sa nachádza
Vo vzťahu k vzorke
Medzi parametrami súvisiacimi s časticami (vzorkami), ktoré sú vystavené elektrickému poľu.
Čím väčšie je čisté zaťaženie častice, tým väčšia rýchlosť jej migrácie a táto veľkosť bude závisieť od pH. Vzťah s veľkosťou je však nepriamo úmerný, čo znamená, že čím viac „veľká“ molekula, tým pomaly migruje pomaly.
Môže vám slúžiť: Lia Agar (železná lyzín): Čo je, nadácia, príprava, použitiaVo vzťahu k elektrickému poľu
Doteraz sme hovorili o dôležitosti elektrického poľa na dosiahnutie pohybu častice elektroforézou, ale nedefinovali sme, čo to je: elektrická sila na jednotku zaťaženia alebo, v jednoduchšom vyjadrení, oblasť vesmíru, kde existuje elektrická sila.
Parametre týkajúce sa elektrického poľa, ktoré môže ovplyvniť migráciu, sú napätie, prúd a odpor.
Napätie ovplyvňuje „čas letu“ molekúl, ktoré sú po aplikácii elektrického poľa oddelené. Čím vyššie je, tým rýchlejšie sú tieto kroky.
Prúd (kontinuálne a jednotné elektróny, ktoré sú „tlačené“ zdrojom napätia) sa vykonáva medzi elektroforetickými systémovými elektródami vďaka iónom prítomným v roztoku pufra. Priamo súvisí s napätím.
Vo vzťahu k roztoku vyrovnávacej pamäte
Zloženie, iónová sila a pH roztoku pufra sú hlavnými parametrami, ktoré ovplyvňujú elektroforetický „beh“, pretože priamo ovplyvňujú niektoré z vlastností vzoriek, najmä elektrický náboj.
Pretože? Roztok pufra stabilizuje pH podporného média, kde sa vyskytuje elektroforéza. Jeho zloženie môže ovplyvniť posun migrovaných častíc a iónovú koncentráciu, pretože priamo súvisí so prúdom.
Vo vzťahu k podpornému médiu
Rôzne typy a formáty elektroforézy tiež prezentujú rôzne médiá, na ktorých sa migrácia vyskytuje a kde sa môže následne „registrovať“.
Rýchlosť migrácie molekúl vystavených elektroforéze závisí od typu podporného média, ktoré by malo byť zvyčajne inertné.
Jeho absorpčné charakteristiky, elektroendoosmóza je dôležitá (pohybová kapacita kvapaliny cez membránu pod vplyvom elektrického poľa) a jeho kapacita molekulárneho sita.
Príklady použitia elektroforézy
Klasické príklady elektroforetických techník používaných v biológii a biotechnológii zahŕňajú:
- Elektroforéza v agarózových géloch (angličtina Elektroforéza gél)
- Elektroforéza v akrylamidových géloch v denaturalizačných podmienkach (SDS-PAGE, angličtina Dodecylsulfát sodný polyakrylamidový gél elektroforéza)
- Elektroforéza v akrylamidových géloch v natívnych podmienkach (BN-PAGE, angličtina Elektroforéza modrého polyakrylamidového gélu)
- Elektroforéza v dvoch rozmeroch (2D-stran, z angličtiny Dvojrozmerná elektroforéza gélu polyakrylamidového gélu)
- Kapilárna elektroforéza (z angličtiny Elektroforéza)
- Izoleectroenfoque (angličtina Izolektrofokusovanie)
- Pulzná elektroforéza v poli (angličtina Elektroforéza pulzného poľa)
Odkazy
- Beck, Kevin. (2020, 25. mája). Typy elektroforézy. Vedecký.com. Zdroj: z vedy.com
- Eseje, UK. (November 2018). Typy a aplikácie elektroforézy. Zdroj: z Ukessays.com
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger princípy biochémie. Macmillan.
- Parmar, P. (August 2018). Elektroforéza: význam, definícia a klasifikácia (s diagramom). Technológia bio. Zdroj z biotechnológie.com
- Perrett, D. (2010). 200 rokov elektroforézy. Chromatog. Dnes 4-7.
- Righetti, P. G. (2005). Elektroforéza: March of Pennies, March of Dimes. Journal of Chromatography A, 1079 (1-2), 24-40.
- Rilbe, h. (Devätnásť deväťdesiatpäť). Som spomínanie histórie elektroforézy. Elektroforéza, 16 (1), 1354-1359.
- Vesterberg, alebo. (1993). Krátka história elektroforetických metód. Elektroforéza, 14 (1), 1243-1249.
- Vinayagam, m. (Žiadny dátum). Faktory ovplyvňujúce elektroforézu. Akadémia.Edu. Zdroj z akademickej obce.Edu
- « Vysvetlenie chemickej rovnováhy, faktory, typy, príklady
- Toltec Culture Origin, Umiestnenie, charakteristika, organizácia »

