Koprepitácia
- 2967
- 779
- Gabriel Bahna
Čo je koprecipitácia?
Ten Koprepitácia Je to zrážanie tuhej látky, ktorá vťahuje normálne rozpustné látky a vyskytuje.
Týmto spôsobom môžete vytvoriť kontamináciu nerozpustnej látky, ktorá nesie rozpustené rozpustené látky kvapalného média. Slovo „znečistenie“ sa uplatňuje na prípady, keď sú rozpustné rozpustené látky vyzrážané nerozpustnou podporou, ale keď nie sú, je to alternatívna analytická alebo syntetická metóda.
Na druhej strane, nerozpustná podpora je vyzrážaná látka. To môže niesť rozpustnú rozpustenú látku vo vnútri (absorpcia) alebo na jeho povrchu (adsorpcia). Spôsob, akým úplne zmení fyzikálno -chemické vlastnosti výslednej tuhej látky.
Aj keď sa koncepcia koprecipitácie môže zdať trochu mätúca, je bežnejšia, ako sa predpokladá, pretože sa vytvárajú viac ako jednoduché kontaminované tuhé látky, vytvárajú sa solídne riešenia zložitých štruktúr a bohaté na neoceniteľné komponenty. Pôda, z ktorej sa rastliny vyživujú, je príkladom koprecipitácie.
Podobne sú minerály, keramika, íly a nečistoty v ľade tiež produktom tohto javu. Ak nie, pôdy by stratili veľkú časť svojich základných prvkov, minerály by neboli také, aké sú známe, a tiež by neexistovala dôležitá metóda pre syntézu nových materiálov.
Príklad koprecipitácie
Aby sme lepšie porozumeli myšlienke koprecipitácie, je ponúkaný nasledujúci príklad.
 Príklady koprecipitácie. Zdroj: Gabriel Bolívar
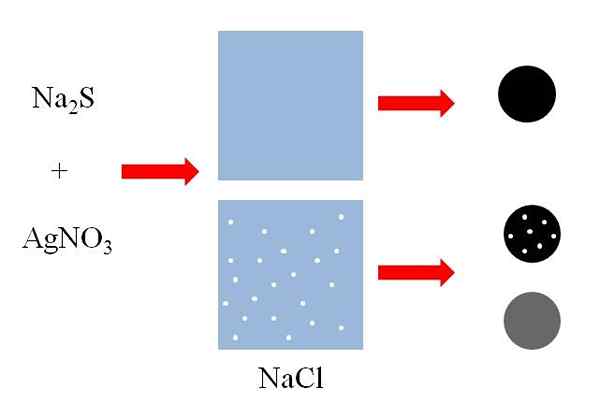
Príklady koprecipitácie. Zdroj: Gabriel Bolívar Vrchol (vynikajúci obrázok) Existujú dva nádoby s vodou, z ktorých jeden obsahuje rozpustený NaCl. NaCl je vysoko rozpustná soľná soľ, ale veľkosť bielych bodov sa zveličuje na vysvetľujúce účely. Každý biely bod sa stane malými agregátmi NaCl v roztoku na okraji nasýtenia.
Môže vám slúžiť: Fermio (FM)Pridané do obidvoch kontajnerov zmes sulfidu sodného, na2S a Silver Dusičnan, agno3, Vyznieva pevnú nerozpustnú sulfur strieborného striebra, AGS:
Nat2S + agno3 => Ags + nano3
Ako je vidieť v prvom nádobe s vodou, čierna tuhá (čierna guľa) sa vyzráža. Táto tuhá látka v rozpustenej nádobe NaCl však nesie častice tejto soli (čierna guľa s bielymi bodmi). NaCl je rozpustný vo vode, ale keď sa AgS vyzráža, adsorbuje sa na čiernom povrchu.
Potom sa hovorí, že NaCl Coprecipited o Ags. Ak sa analyzovala čierna tuhá látka, na povrchu bolo možné pozorovať mikrokristály NaCl.
Tieto kryštály však môžu byť tiež vo vnútri AG, takže tuhá látka by „otočila“ sivú (biela + čierna = sivá).
Typy Koprepitácia
Čierna guľa s bielymi bodmi a šedá guľa ukazuje, že rozpustná rozpustená látka môže koprecipitovať rôznymi spôsobmi.
V prvom, to robí povrchne, adsorbovaný na nerozpustnej podpore (AGS v predchádzajúcom príklade), zatiaľ čo v druhom to robí interne, „mení“ čiernu farbu zrazeniny.
Dajú sa získať ďalšie typy tuhých látok? To znamená gule s čiernymi a čiernymi fázami, to znamená z AGS a NaCl (spolu s nano3 ktoré tiež coprecipita). To je miesto, kde vzniká vynaliezavosť syntézy nových tuhých látok a materiálov.
Vráťte sa však do počiatočného bodu, v podstate rozpustná rozpustná látka solutu, ktorá generuje rôzne typy tuhých látok. Typy koprecipitácie a tuhé látky, ktoré z nich vyplývajú, budú uvedené nižšie.
Môže vám slúžiť: materiály, ktoré majú malý odpor voči priechodu elektrinyZaradenie
Hovorí sa o zahrnutí, keď v kryštalickej sieti môže byť jeden z iónov nahradený niektorými z koprecipitovaných rozpustných látok.
Napríklad, ak NaCl bol koprecipovaný prostredníctvom inklúzie, na ióny+ Obsadili by miesto AG+ V časti kryštalického usporiadania.
Avšak zo všetkých typov koprecipitácie je to najmenej pravdepodobné, pretože na to, aby sa vyskytli, musia byť veľmi podobné iónové rádiá. Po návrate do šedej sféry obrazu by zaradenie predstavovalo jeden z jasnejších šedých tónov.
Ako už bolo uvedené, inklúzia je uvedená v kryštalických tuhých látkach a na ich získanie, doména chémie roztokov a niekoľkých faktorov (T, pH, čas agitácie, molárne vzťahy atď.).
Oklúzia
Pri oklúzii sú ióny zachytené v kryštalickej sieti, ale bez toho, aby sa nahradil akýkoľvek ión usporiadania. Napríklad v rámci AGS môžete tvoriť kryštály Ocluido. Graficky by sa dalo vizualizovať ako biely kryštál obklopený čiernymi kryštálmi.
Tento typ koprecipitácie je jedným z najbežnejších a vďaka tomu je syntéza nových kryštalických tuhých látok. Obluidné častice nemožno eliminovať jednoduchým premytím. Na tento účel by bolo potrebné rekryzovať celú súpravu, to znamená nerozpustnú podporu.
Zahrnutie aj oklúzia sú absorpčné procesy uvedené v kryštalických štruktúrach.
Adsorpcia
Pri adsorpcii leží koprecipitovaná tuhá látka na povrchu nerozpustnej podpory. Veľkosť častíc tejto podpory definuje typ získanej tuhej látky.
Môže vám slúžiť: IsóbarosAk sú malé, získa sa koagulovaná tuhá látka, z ktorej je ľahké eliminovať nečistoty. Ale ak sú veľmi malé, tuhá látka absorbuje množstvo vody a bude želatín.
Vráťte sa do čiernej gule s bielymi bodmi, koprecipitované kryštály NaCl na Ag sa môžu premyť destilovanou vodou. Takže, až kým sa čistí Ags, ktoré sa potom môže zahrievať, aby sa odparil všetku vodu.
Aplikácie Koprepitácia
Niektoré z aplikácií Coprecipitation sú nasledujúce:
- Umožňuje kvantifikovať rozpustné látky, ktoré nie sú ľahko vyzrážané od média. Prostredníctvom nerozpustnej podpory teda vedie napríklad rádioaktívne izotopy, ako je Francio, pre neskoršiu štúdiu a analýzu.
- Ak sa koprecipitujú ióny v želatínových tuhých látkach, kvapalné médium sa čistí. Oklúzia je v týchto prípadoch ešte viac požadovaná, pretože nečistota nebude schopná uniknúť.
- Coprecipitácia umožňuje počas ich tvorby začleniť látky do tuhých látok. Ak je tuhá látka polymér, potom absorbuje rozpustné rozpustené látky, ktoré potom budú koprecipitovať vo vnútri, čím sa dá nové vlastnosti. Ak je to napríklad celulóza, mohol by byť kobalt (alebo iný kov) vyrobený v Coprecipite.
- Okrem toho vyššie uvedeného je koprecipitácia jednou z kľúčových metód syntézy nanočastíc na nerozpustnej podpore. Vďaka tejto.
Odkazy
- Zrážky a korepitácia. NPTEL sa obnovil.Ac.v
- Čo je koprecipitácia. Zotavené z WiseGeek.com

