Štruktúra kyseliny sulfanidovej, vlastnosti, syntéza, použitie
- 3665
- 1075
- Alfréd Blaho
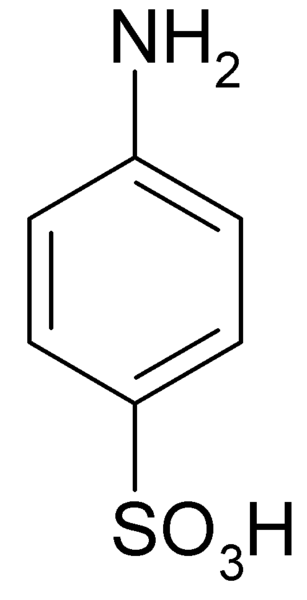
On Kyselina sulfanínová Je to kryštalická zlúčenina, ktorej molekula je tvorená benzénovým kruhom, ku ktorému je základná skupina súčasne zjednotená (-NH2) a kyslou skupinou (-SO3H). Jeho chemický vzorec je NH2C6H4SW3H.
Je tiež známa ako kyselina 4-aminobencensulfónová kyselina. Je pripravený sulfonáciou anilínu v polohe pre. Jeho kryštály sú biele alebo biele drážky. Jeho správanie je viac podobné správaniu soli ako v organickom zlúčenine so skupinami NH2 nosiť3H. Preto je nerozpustný vo väčšine organických rozpúšťadiel.
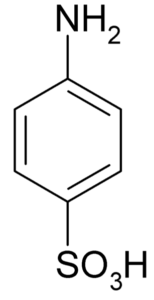 Molekulárny vzorec kyseliny sulfanidovej alebo kyseliny 4-amynobenzeulfónovej. Klaus Hoffmeier [verejná doména]. Zdroj: Wikipedia ako my
Molekulárny vzorec kyseliny sulfanidovej alebo kyseliny 4-amynobenzeulfónovej. Klaus Hoffmeier [verejná doména]. Zdroj: Wikipedia ako my Jedným z jej hlavných použití je syntéza farbív, pretože ľahko tvorí diazokomponovaný, ktorý je surovinou pre túto aplikáciu.
Kyselina sulfanylová aj jej deriváty sa používajú ako antibakteriálne látky. Používa sa v syntéze mukolytických zlúčenín, pretože majú schopnosť redukovať viskozitu hlienu alebo veľmi viskózne biologické tekutiny.
Používa sa tiež v papierovom priemysle a vo vzorcoch pre rytiny alebo litografie. Je súčasťou živíc, ktoré sa používajú v betónových zmesiach alebo maltách, aby im umožnili udržiavať svoju plynulosť po dlhú dobu, bez toho, aby ovplyvnili konečný čas nastavenia.
Je to xenobiotický metabolit, to znamená, že nie je prirodzene produkovaný živými bytosťami. Je to dráždivá pokožka, oči a sliznica. Okrem toho môžete kontaminovať životné prostredie.
[TOC]
Štruktúra
Kyselina sulfanínová má biele kryštály tvorené ortorbickými alebo monoklinickými plachtami. Jeho monohydráty kryštalizuje vo vode vo forme orhorrombických listov. Ak sa kryštalizácia vykonáva veľmi pomaly, kryštalizuje dihydrát. Monohydrát sa stáva bezvodým, keď je asi 100 ° C.
Menovanie
- Kyselina sulfanínová.
- Kyselina p-amynobencensulfónová.
- Kyselina 4-amybonzefónová.
Vlastnosti
Fyzický stav
Biela alebo biela kryštalická pevná látka.
Molekulová hmotnosť
173,19 g/mol.
Bod topenia
Rozpadne sa na asi 288 ° C bez topenia. Uvádza sa tiež na> 320 ° C.
Hustota
1,49 g/cm3
Rozpustnosť
Takmer nerozpustné vo vode: 10,68 g/l pri 20 ° C.
Nerozpustný v etanole, benzéne a éteru. Mierne rozpustný v horúcom metanole.
Rozpustné vo vodných roztokoch. Nerozpustné vo vodných roztokoch minerálnych kyselín. Rozpustný v koncentrovanej kyseline chlorovodíkovej.
Chemické vlastnosti
Jeho vlastnosti sa líšia od vlastností iných amínových alebo sulfonovaných zlúčenín, ktoré sú podobné vlastnostiam soli. Je to preto, že jej štruktúra obsahuje skupiny -NH3+ A tak3-, Čo mu dáva charakteristiky dipólových iónov.
Môže vám slúžiť: presýtené riešenieObsahuje kyslú skupinu a základnú skupinu v opačných póloch tej istej molekuly. Ale vodíkový ión je spojený s dusíkom namiesto kyslíka, pretože skupina -NH2 Je to silnejšia základňa ako skupina3-.
Pretože je to dipólový ión, predstavuje najvyšší bod zlúčenia a nerozpustnosti v organických rozpúšťadlách.
Kyselina sulfanidová je rozpustná v alkalickom roztoku, pretože OH hydroxid ión-, Byť silne základný, začína sa vodíkový ión (h+) slabej základnej skupiny -nh2, Tvorba iónu p-aminobencensulfonátu, ktorý je rozpustný vo vode.
V kyslom roztoku sa štruktúra kyseliny sulfanylovej nemení, preto zostáva nerozpustná.
Ďalšie vlastnosti
Keď sa zahrieva na jeho rozklad emituje toxické výpary dusíka a oxidov síry.
Expozícia kyseliny sulfanylovej môže viesť k príznakom, ako je podráždenie kože, oči a sliznice. Je to korozívna zlúčenina.
Syntéza
Sa pripravuje reagovaním anilínu kyselinou sírovou (H2SW4) pri vysokých teplotách. Spočiatku sa vytvorí soľ sulfátu kyseliny anilínskej kyseliny, ktorá sa pri zahrievaní pri 180-200 ° C reorganizuje, aby sa vytvoril kruh nahradený v polohe, pretože je najstabilnejší produkt.
Na jeho prípravu s vysokým stupňom čistoty sa sulfonácia zmesi anilínu a sulfolano vykonáva s H2SW4 pri 180-190 ° C.
Žiadosti
V priemysle sfarbenia
Kyselina sulfanylová sa používa pri syntéze alebo príprave niekoľkých farbív, ako je metyl oranžová a tartrazín. Z tohto.
Je dôležité zdôrazniť, že tartrazín sa používa ako sfarbenie v potravinách. Ale po požití vytvára určité metabolity v ľudskom organizme vrátane kyseliny sulfanylovej, ktoré sú možné zodpovedné za tvorbu reaktívnych druhov kyslíka. Môžu ovplyvniť obličkové (obličky) alebo pečeňové tkanivá (pečeň).
 Karamely so žltým farbivom. David Adam Kess [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]. Zdroj: Wikipedia Commons
Karamely so žltým farbivom. David Adam Kess [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]. Zdroj: Wikipedia Commons V analytickej chémii
Používa sa ako činidlo pri určovaní niekoľkých chemických zlúčenín vrátane dusičnanov.
V medicíne ako antibakteriálne činidlo
Sulfanylamid, odvodený od kyseliny sulfanylovej, má aplikáciu vo farmaceutickom priemysle, pretože má antibakteriálnu aktivitu.
V ľudskom tele baktérie zmiasť s kyselinou p-aminobenzoovou, ktorá je nevyhnutným metabolitom. Táto substitúcia spôsobuje, že sa baktérie nebudú reprodukovať a nezomrejú.
Môže vám slúžiť: Vodík: História, štruktúra, vlastnosti a použitia Baktéria. Obrázok Raman Oza. Zdroj: Pixabay
Baktéria. Obrázok Raman Oza. Zdroj: Pixabay Ďalší odvodený z kyseliny sulfanylovej, získanej kondenzáciou s inými zlúčeninami, má tiež antibakteriálne vlastnosti, ktoré sú založené na jej schopnosti vytlačiť kyselinu listovú (člen vitamínového komplexu B).
Táto zlúčenina sa môže odobrať orálne, injektované intravenózne alebo externe aplikovať do masti.
V medicíne ako mukolytické činidlo
Použil sa derivát kyseliny sulfanylovej, ktorý má mukolytickú aktivitu. Je to tak, že predstavuje aktivitu hlienu LicueFactiva, rozpustenie hlienu alebo veľmi viskóznych biologických tekutín.
Zlúčenina sa môže použiť na produkciu hlienu produkovaného tkanivom v dôsledku patologických podmienok. Napríklad preťaženie dýchacieho systému alebo medzi iným z vaginálneho traktu.
Pokiaľ ide o skvapalnenie hlienu v respiračnom trakte, produkt sa podáva vdýchnutím, kvapkami v nose, rose, aerosóloch alebo rozprachoch. Je to liečba uplatniteľná na ľudskú bytosť alebo cicavce. Je to silnejšia zlúčenina ako na báze cysteínu.
 Aplikácia nosných kvapiek na chlad. Obrázok Thorsten Frenzel. Zdroj: Pixabay
Aplikácia nosných kvapiek na chlad. Obrázok Thorsten Frenzel. Zdroj: Pixabay Používa sa tiež v laboratóriu, keď je potrebné znížiť viskozitu biologických tekutín, aby sa uľahčili analytické stanovenia.
V laboratóriách bioanalýzy
Diazotizovaná kyselina sulfanylová (derivát, ktorý sa pripravuje reakciou kyseliny sulfanylovej s dusičnanom sodným) sa používa pri stanovení bilirubínu.
Bilirubín je žltý pigment nachádzajúci sa v žlč. Prebytok bilirubínu v krvi je dôsledkom chorôb pečene, hematologických porúch (alebo krvi) alebo porúch v biliárnom trakte.
Na meranie množstva bilirubínu v krvi sa dialýza odvodená od kyseliny sulfanylovej s bilirubínom reaguje na vytvorenie azobilirubínového komplexu, ktorého farba sa merala intenzita pomocou kolorimetra alebo spektrofotometra. Týmto spôsobom je obsah bilirubínu v krvi určený v krvi.
V papierovom priemysle
Kyselina sulfanínová vám umožňuje syntetizovať papierové leštenie, to znamená zlúčeninu, ktorá poskytuje optický jas alebo biely vzhľad, pretože neutralizuje žltú farbu prírodného alebo nekologického papiera.
 Zápisník. Zdroj: pexels
Zápisník. Zdroj: pexels Má výhodu oproti iným zlúčeninám, pretože sa môže použiť v relatívne vysokých koncentráciách na ošetrenie papierovej buničiny za podmienok s nízkym pH bez zvýšenia žltej papiera.
Môže vám slúžiť: síran amónnyVýsledok sa dokazuje, keď sa papier pozoruje s UV svetlom (ultrafialové), pod ktorým fluores a oveľa viac, ako keď sa používajú iné zlúčeniny, a pri viditeľnom svetle sa pozoruje, že stupeň žltosti je veľmi nízka.
Je veľmi rozpustný vo vode, čo jej umožňuje používať v koncentrovanejších roztokoch. Môže sa použiť v akomkoľvek type papiera, vrátane papiera vyrobeného s buničinou z mletého dreva, sulfitou alebo iným procesom.
V dojmoch, rytinách alebo litografiách
Kyselina sulfanidová funguje ako okyslenie v koncentrovaných roztokoch pre litografiu bez toho, aby predstavovala problémy iných kyselín, ako je fosforerácia, je menej toxická a menej znečisťujúca ako táto.
Vo stavebných materiáloch
Vodný melamín-formaldehyd živice roztoky modifikované kyselinou sulfanylovou kyselinou boli testované špecificky (betón), malty alebo cementovej pasty. Účelom bolo znížiť obsah vody a zabrániť zníženiu plynulosti zmesi pri plynutí času, bez toho, aby sa čas nastavenia znížil.
Betón alebo malta pripravená s týmito roztokmi je veľmi účinná v lete, keď pokles plynulosti v priebehu času predstavuje problém.
S týmito roztokmi, ak je malta alebo betón pripravený a z akéhokoľvek dôvodu sa musí nechať odpočívať, zloženie cementu sa dá ľahko vypustiť do foriem alebo podobne, pretože v priebehu času nestratila plynulosť.
 Výtok. Igor obraz ovsynykovov. Zdroj: Pixabay
Výtok. Igor obraz ovsynykovov. Zdroj: Pixabay Odkazy
- Windholz, m. a kol. (redaktori) (1983). Index Merck. Encyklopédia chemikálií, dragov a biologických látok. Desiate vydanie. Merck & Co., Inc.
- Kirk-Othmer (1994). Encyklopédia chemickej technológie. Zväzok 2. Štvrté vydanie. John Wiley & Sons.
- Lekárska knižnica. (2019). Kyselina sulfanínová. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Urist, h. a Martin, G.J. (1950). Deriváty kyseliny sulfanidovej. USA patent nie. 2 504 471. Prideľovatelia Národnej drogovej spoločnosti. 18. apríla 1950.
- Villaume, Frederick G. (1964). Zloženie Brightcar pre papier zadávaný z metanilácie a kyseliny sulfanidovej. USA patent nie. 3 132,106. 5. mája 1964.
- Martin, Tellis a. a jesť, William T. (1979). Derivát kyseliny benzoovej a mukolytický proces kyseliny benzénovej. USA patent nie. 4 132 802. 2. januára 1979.
- Druker, L.J. a Kincaid, r.B. (1979). Koncentrát litografickej fontány. USA patent nie. 4 150,996. 24. apríla 1979.
- Shull, Bruce C. (1983). Bilirubínový test. USA patent nie. 4 404 286. 13. september 1983.
- Uchida, j. a kol. (2001). Proces na prípravu vodného roztoku kyseliny sulfanidovej modifikovanej melamín-formaldehydovej živice a cementovej kompozície. USA patent nie. 6 214 965 B1. 10. apríla 2001.
- Corradini, m.G. (2019). Zväzok 1. V encyklopédii chémie potravín. Zotavené z vedeckých pracovníkov.com.
- « Štruktúra kyseliny galovej, vlastnosti, získanie, použitia
- Čierna podľa pozadia, vývoja, opatrení »

