Kyselina dusičná (HNO3)
- 4475
- 624
- MUDr. Miloslav Habšuda
On kyselina dusičná Je to anorganická zlúčenina, ktorá pozostáva z oxoacidy dusíka. Považuje sa za silnú kyselinu, hoci jej PKA (-1,4) je podobná PKA hydrónskeho iónu (-1,74). Od tohto bodu je to pravdepodobne „najslabší“ z mnohých známych silných kyselín.
Jeho fyzický vzhľad pozostáva z bezfarebnej kvapaliny, ktorá sa zmení na žltkastú farbu v dôsledku tvorby dusíkových plynov. Jeho chemický vzorec je HNO3.
Je nestabilný a zažíva ľahký rozklad na vystavenie slnečnému žiareniu. Okrem toho sa môže úplne rozpadať zahrievaním, čo spôsobuje dusík, vodu a kyslíkový oxid.
Používa sa na výrobu anorganických a organických dusičnanov, ako aj v zlúčeninách dusíkov, ktoré sa používajú pri výrobe hnojív, výbušnín, sprostredkovateľov farbív a rôznych organických chemických zlúčenín.
V atmosfére nie2 Produkovaný ľudskou aktivitou reaguje s vodou oblakov a tvorí HNO3. Potom, počas kyslých dažďov, precipitáty spolu s kvapkami vody, napríklad socha verejných štvorcov.
Kyselina dusičná je veľmi toxická zlúčenina a kontinuálna expozícia jej výparom môže produkovať chronickú bronchitídu a chemická pneumónia.
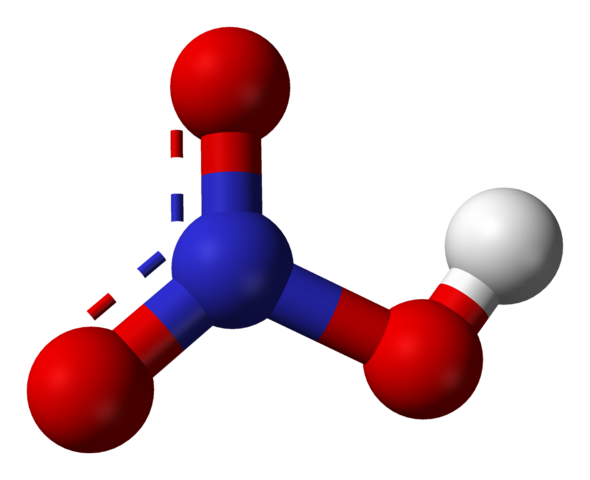
Štruktúra kyseliny dusičnej
 Zdroj: Ben Mills [verejná doména], z Wikimedia Commons
Zdroj: Ben Mills [verejná doména], z Wikimedia Commons Horný obrázok ukazuje štruktúru molekuly HNO3 S sférou a tyčovým modelom. Atóm dusíka, modrá guľa, sa nachádza v strede, obklopená trigonálnou plochou geometriou; Avšak trojuholník je zdeformovaný jedným z najdlhších vrcholov.
Molekuly kyseliny dusičnej sú potom ploché. Odkazy N = O, N-O a N-OH tvoria vrcholy plochého trojuholníka. Ak je podrobne pozorovaný, Link N-OH je predĺženejší ako ostatné dva (kde biela guľa predstavuje atóm H).
Rezonančné štruktúry
Existujú dva odkazy, ktoré majú rovnakú dĺžku: n = o a n-o. Táto skutočnosť je proti teórii odkazov Valencie, kde sa predpokladá, že dvojité odkazy sú kratšie ako jednoduché odkazy. Vysvetlenie v tomto spočíva vo fenoméne rezonancie, ako je pozorované na nižšom obrázku.
 Zdroj: Ben Mills [verejná doména], z Wikimedia Commons
Zdroj: Ben Mills [verejná doména], z Wikimedia Commons Obe odkazy, N = O a N-O, sú preto rovnocenné v rezonančných podmienkach. Toto je graficky znázornené v štruktúrnom modeli pomocou diskontinuálnej čiary medzi dvoma atómami O (pozri štruktúru).
Keď je HNO nechránený3, Stabilný anión dusičnanov je tvorený nie3-. V ňom rezonancia teraz zahŕňa tri atómy O. To je dôvod, prečo HNO3 Má veľkú kyslosť bronsted-liwry (druh donátora hone+).
Môže vám slúžiť: Appette PipateFyzikálne a chemické vlastnosti
Chemické názvy
-Kyselina dusičná
-Kyselina
-Dusičnanový vodík
-Voda.
Molekulová hmotnosť
63,012 g/mol.
Fyzický vzhľad
Bezfarebná tekutina alebo bledožltá farba, ktorá môže byť červenkasto hnedá.
Vôňa
Aker, charakteristické dusenie.
Bod varu
181 ° F pri 760 mmHg (83 ° C).
Bod topenia
-41,6 ° C.
Rozpustnosť
Veľmi rozpustné a miešateľné vodou.
Hustota
1 513 g/cm3 pri 20 ° C.
Relatívna hustota
1,50 (vo vzťahu k vode = 1).
Relatívna hustota pary
2 alebo 3 -krát odhadované (vo vzdušnom vzťahu = 1).
Tlak vodnej pary
63,1 mmHg pri 25 ° C.
Rozklad
Vystavením atmosférickej alebo tepelnej vlhkosti sa môže rozložiť tvorba peroxidu dusíka. Keď sa tento rozklad zahrieva, emituje veľmi toxický dym z oxidu dusíka a dusíka vodíka.
Kyselina dusičná nie je stabilná, je schopná preniknúť do kontaktu s teplom a vystavením slnečnému žiareniu a emiting oxidu dusičného, kyslíka a vody.
Hrebeň
1 092 MPa pri 0 ° C a 0,617 MPa pri 40 ° C.
Korózia
Je schopný zaútočiť na všetky základné kovy, s výnimkou hliníka a chromickej ocele. Zaútočte na niektoré z odrôd plastového materiálu, kaučukov a povlakov. Je to žieravá a korozívna látka, takže sa musí manipulovať s vysokou opatrnosťou.
Molárna entalpia odparovania
39,1 kJ/mol pri 25 ° C.
Štandardná molárna entalpia
-207 kJ/mol (298 ° F).
Štandardná molárna entropia
146 kJ/mol (298 ° F).
Povrchové napätie
-0,04356 N/M A 0 ° C
-0,04115 N/m A 20 ° C
-0,0376 N/m A 40 ° C
Prah
-Nízka vôňa: 0,75 mg/m3
-Vysoký zápach: 250 mg/m3
-Podráždená koncentrácia: 155 mg/m3.
Disociačná konštanta
Pka = -1,38.
Index lom (η/d)
1 393 (16,5 ° C).
Chemické reakcie
Hydratácia
Môže tvoriť tuhé hydráty, napríklad HNO3∙ h2Alebo hno3∙ 3h2O: „Dusičný ľad“.
Disociácia vo vode
Kyselina dusičná je silná kyselina, ktorá sa rýchlo ionizuje vo vode nasledujúcim spôsobom:
Hned3 (L) +h2Alebo (l) => h3Ani+ (ac) +nie3-
Tvorba predaja
Reaguje so základnými oxidmi tvoriacimi dusičnanu a vodnú soľ.
CAO (s) +2 hno3 (l) => CA (nie3)2 (Ac) +h2Alebo (l)
Podobne reaguje so základňami (hydroxidy) a tvorí dusičnanu a vodnú soľ.
NaOH (ac) +hno3 (l) => nano3 (Ac) +h2Alebo (l)
A tiež s uhličitanou a kyslými uhličitanymi (bikarbonáty), ktoré tiež tvoria oxid uhličitý.
Nat2Co3 (Ac)+hno3 (l) => nano3 (Ac)+h2Alebo (l)+co2 g)
Protonácia
Kyselina dusičná sa môže tiež správať ako základňa. Z tohto dôvodu môžete reagovať s kyselinou sírovou.
Hned3 + 2h2SW4 Nie2+ + H3Ani+ + 2HSO4-
Sebaproakovanie
Kyselina dusičná prežíva samonosotolýzu.
2Hno3 Nie2+ + Nie3- + H2Ani
Oxidácia kovu
Pri reakcii s kovmi sa kyselina dusičná nepohoní ako silné kyseliny, ktoré reagujú s kovmi tvoriacimi zodpovedajúcu soľ a uvoľňujúci vodík plynným spôsobom.
Môže vám slúžiť: hydrokoloidHorčík a mangán však reagujú horúce s kyselinou dusičnou, ako to robia zostávajúce silné kyseliny.
Mg (s) +2 hno3 (l) => mg (nie3)2 (Ac) +h2 g)
Ďalší
Kyselina dusičná reaguje s sulfitmi kovu a spôsobuje dusičnanovú soľ, oxid siričitý a vodu.
Nat2SW3 (s) +2 hno3 (L) => 2 nano3 (Ac) +So2 g) +h2Alebo (l)
A tiež reaguje s organickými zlúčeninami a nahradí vodík za nitro skupinu; Teda základný základ pre syntézu výbušných zlúčenín, ako je nitroglycerín a trinitrotoluén (TNT).
Syntéza
Priemyselný
Vyrába sa na priemyselnej úrovni katalytickou oxidáciou amoniak podľa metódy opísanej Oswaldom v roku 1901. Postup pozostáva z troch etáp alebo krokov.
Fáza 1: Oxidácia amónneho oxidu dusnatého
Amónny sa oxiduje kyslíkom prítomným vo vzduchu. Reakcia sa uskutoční pri 800 ° C a 6-7 atm, s použitím platiny ako katalyzátora. Amónny sa zmieša so vzduchom s nasledujúcim pomerom: 1 objem amónia o 8 objemov vzduchu.
4 nh3 g) +5o2 (g) => 4No (g) +6h2Alebo (l)
Pri reakcii oxid dusnatého vzniká, ktorý sa preberá do oxidačnej komory pre ďalšiu fázu.
Fáza 2. Oxidácia oxidu dusnatého pri oxidu dusičného
Oxidácia sa vykonáva kyslíkom prítomným vo vzduchu pri teplote pod 100 ° C.
2No (g) +alebo2 (g) => 2No2 g)
Stage 3. Rozpustenie oxidu dusičnanom vo vode
V tomto štádiu dochádza k tvorbe kyseliny dusičnej.
42 + 2h2Alebo +o2 => 4Hno3
Existuje niekoľko metód absorpcie oxidu dusičného (nie2) Vo vode.
Medzi iné metódy: Nie2 je dimmerizovaný na n2Ani4 Pri nízkych teplotách a vysokom tlaku, aby sa zvýšila rozpustnosť vody a produkovala kyselinu dusičnú.
3n2Ani4 + 2h2O => 4Hno3 + 2
Kyselina dusičná produkovaná oxidáciou amónneho má koncentráciu medzi 50-70%, čo sa môže dosiahnuť na 98% pomocou kyseliny sírovej koncentrovanej ako dehydratácia, čo umožňuje zvýšiť koncentráciu kyseliny dusičnej.
V laboratóriu
Tepelný rozklad dusičnanov medi (II), ktorý produkuje plyny dusíka a oxidu kyslíka, ktoré prechádzajú vodou za vzniku kyseliny dusičnej; Rovnako ako v metóde Oswald, predtým opísaná.
2CU (nie3)2 => 2CUO +4NO2 + Ani2
Reakcia dusičnanovej soli s H2SW4 koncentrovaný. Tvarovaná kyselina dusičná je oddelená od H2SW4 destiláciou pri 83 ° C (bod varu kyseliny dusičnej).
Môže vám slúžiť: Absolvenovaná pipetka: Charakteristiky a použitiaPokaziť sa3 + H2SW4 => Hno3 + Khso4
Žiadosti
- 60% produkcie kyseliny dusičnej sa používa pri výrobe hnojív, najmä dusičnanu amónneho.
- 15 % výroby kyseliny dusičnej sa používa vo výrobe syntetických vlákien.
- Používa sa na vypracovanie dusičných a nitroderivovaných kyslých esterov; ako je nitrocelulóza, akrylové obrazy, nitrobenzén, nitrotoluén, acrilonitrilos atď.
- Do organických zlúčenín môžete pridať nitro skupiny, ktoré môžete využívať na výrobu výbušnín, ako je nitroglycerín a trinitrotoluén (TNT).
- Vďaka svojej oxidačnej kapacite je veľmi užitočná pri čistení kovov prítomných v mineráloch. Používa sa tiež pri získavaní prvkov, ako je urán, mangán, niobium, zirkón a acidifikácia fosforických hornín, aby sa získala kyselina fosforečná kyselina.
- Zmieša sa s koncentrovanou kyselinou chlorovodíkovou, aby sa vytvoril „kráľovská voda“. Tento roztok je schopný rozpustiť zlato a platinu, čo umožňuje jeho použitie pri čistení týchto kovov.
- Používa sa na získanie účinku seniority na nábytok vyrobený z borovicového dreva. Ošetrenie 10% roztokom kyseliny dusičnej vytvára farbu sivej zlatej farby v nábytkovom dreve.
- Zmes vodných roztokov 5-30% kyseliny dusičnej a kyseliny fosforečnej 15-40% sa používa pri čistení zariadenia používaného v dojenia.
- Je užitočný pri čistení skleneného materiálu používaného v laboratóriu.
- Vďaka svojej kapacite rozpúšťadla sa používa pri analýze rôznych kovov prostredníctvom techník absorpčnej spektrofotometrie atómového plameňa a spektrofotometrie indukčnej spojovacej hmoty.
- Kombinácia kyseliny dusičnej a kyseliny sírovej sa použila na spoločnú konverziu bavlny na dusičnan celulózy (dusnatková bavlna).
- Kyselina červená fajčiarska dusičná a biela kyselina fajčiarska dusičná sa používajú ako oxidanty pre raketové kvapalné palivá, najmä v rakete Bomarc.
Toxicita
- V kontakte s kožou môže spôsobiť popáleniny kože, intenzívnu bolesť a dermatitídu.
- V kontakte s očami môže spôsobiť intenzívne, roztrhnutie a v ťažkých prípadoch poškodenie rohovky a slepoty.
- Vdýchnutie výparov môže spôsobiť kašeľ, respiračné ťažkosti, spôsobovať intenzívne alebo chronické výstavy, krvácanie z nosa, lingingitída, chronická bronchitída, pneumónia a pľúcny edém.
- Kvôli jeho požitiu sa vyskytujú zranenia v ústach, slinenie, intenzívny smäd, prehltnutie bolesti, intenzívna bolesť v celom tráviacom trakte a riziko vŕtania steny.
Odkazy
- Kyselina dusičná. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Kyselina dusičná. Encyclopædia Britannica. Získané z: Britannica.com
- Kyselina dusičná. Obnovené z: Chemicalbook.com
- « Myšlienky, ktoré konfrontujú teologické myslenie s evolučnou teóriou
- Aké boli voľby, keď nebol autonómny a spoľahlivý volebný systém? »

