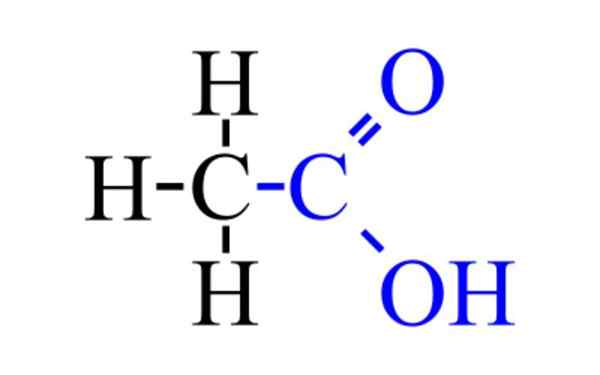
Kyselina octová (CH3COOH)
- 2066
- 278
- Alfréd Blaho
 Kyselina octová je zodpovedná za charakteristickú chuť a vôňu octu
Kyselina octová je zodpovedná za charakteristickú chuť a vôňu octu Čo je kyselina octová?
On octová kyselina, o Kyselina estano, je to bezfarebná organická kvapalina, ktorej chemický vzorec je Cho3Kohútik. Je prítomný v octe, ktorý dáva jeho charakteristickú vôňu a chuť. Ocot je vodný roztok kyseliny octovej s 5%koncentráciou, približne.
Ako už názov napovedá, je to kyslá zlúčenina, a preto má ocot hodnoty pH menšie ako 7. V prítomnosti jeho acetátovej soli predstavuje účinný systém tlmenia v regulácii pH medzi 2,76 a 6,76, to znamená, že udržiava pH v tomto intervale proti miernym pridaním bázy alebo kyseliny.
Po kyseline mravčej, HCOOH, je jednou z najjednoduchších organických kyselín, čo tiež predstavuje konečný bod mnohých fermentačných procesov. Bežne sa používa na obliekanie potravín a tiež na odstránenie nečistôt a mikroorganizmov zo zeleniny.
História
Človek použil kvasenie početných ovocia, strukovín, obilnín atď., Na získanie alkoholických nápojov, produkt transformácie cukrov, ako je glukóza, v etanole, ch3Chvály2Oh.
Pravdepodobne preto, že počiatočná metóda výroby alkoholu a octu je fermentácia, možno sa snaží vyrábať alkohol v neurčitovanom okamihu, pred mnohými storočiami, ocot sa získal omylom.
Už v treťom storočí.C., Grécky filozof Theophastus opísal pôsobenie octu na výrobu pigmentov, napríklad olovo biela.
1800
V roku 1823 bolo v Nemecku navrhnuté zariadenie na tvare veže na aeróbne fermentáciu rôznych výrobkov, aby sa získala kyselina octová vo forme octu.
V roku 1846 Herman Foelbe prvýkrát dosiahol syntézu kyseliny octovej pomocou anorganických zlúčenín. Syntéza sa začala chloráciou disulfidu uhlíka a po dvoch reakciách sa uzavrela elektrolytickou redukciou na kyselinu octovú.
Na konci 19. a začiatkom dvadsiateho storočia, kvôli J J. Weizmann začal používať baktérie Clostridium acetobutylicum Na produkciu kyseliny octovej, prostredníctvom anaeróbnej fermentácie.
Môže vám slúžiť: Vzťah chémie a technológie s človekom, zdravím a životným prostredím1900
Na začiatku 20. storočia bola dominantnou technológiou produkcia kyseliny octovej oxidáciou acetaldehydu.
V roku 1925 Henry Dreyfus z britskej spoločnosti Celanese navrhol pilotný závod na karbonilamáciu metanolu. Následne v roku 1963 nemecká spoločnosť BASF zaviedla použitie kobaltu ako katalyzátora.
Otto Hromatka a Heinrich Ebner (1949), navrhli nádrž s agitáciou a dodávky vzduchu na aeróbne fermentáciu určené na výrobu octu. Táto implementácia s niektorými úpravami zostáva v používaní.
V roku 1970 severoamerická spoločnosť Monsanto použila systém katalyzátorov založených na ródiu na karbonilamáciu metanolu.
Následne spoločnosť BP v roku 1990 zavádza postup Cativa s použitím katalyzátora Iridium na rovnaký účel. Ukázalo sa, že táto metóda je účinnejšia a menej agresívna ako metóda Monsanto.
Štruktúra kyseliny octovej
 Štruktúra chemickej kyseliny octovej
Štruktúra chemickej kyseliny octovej Horný obrázok ukazuje štruktúru kyseliny octovej reprezentovanú s modelom guľôčok a tyčí. Červené gule zodpovedajú atómom kyslíka, ktoré zase patria karboxylovej skupine, -cooh. Preto je to karboxylová kyselina. Na pravej strane štruktúry máte metylovú skupinu, -ch3.
Ako je vidieť, je to veľmi malá a jednoduchá molekula. Má trvalý dipólový moment v dôsledku skupiny -COOH, ktorá tiež umožňuje kyselinu octovú tvoriť dva po sebe.
Práve tieto mosty priestorovo vedú molekuly ch3COOH za vzniku odmeny v kvapalnom stave (a plyne).
 Dva vodíkové mosty
Dva vodíkové mosty Na obrázku sa pozoruje, ako sú tieto dve molekuly usporiadané tak, aby tvorili dva vodíkové mosty: O-H-O a O-H-O.
Na odparovanie kyseliny octovej sa musí dodať dostatok energie na prelomenie týchto interakcií, a preto ide o kvapalinu s bodom varu väčšieho ako voda (približne 118 ° C).
Fyzikálne a chemické vlastnosti kyseliny octovej
Chemické názvy
Kyselina:
Môže vám slúžiť: hliníkový bromid- Octový
- Etanoický
- Etyl
Molekulárna receptúra
C2H4Ani2 alebo CH3Kohútik.
Fyzický vzhľad
Bezfarebná tekutina.
Vôňa
Charakteristický aker.
Príchuť
Popáliť.
Bod varu
244 ° F pri 760 mmHg (117,9 ° C).
Bod topenia
61,9 ° F (16,6 ° C).
zapaľovač
112 ° F (otvorené sklo) 104 ° F (zatvorené sklo).
Rozpustnosť
106 mg/ml pri 25 ° C (je miešateľný vo všetkých rozmeroch).
Rozpustnosť v organických rozpúšťadlách
Je rozpustný v etanole, etyléter, acetóne a benzéne. Je tiež rozpustný v uhlíkovom tetrachloridu.
Hustota
1 051 g/cm3 pri 68 ° F (1 044 g/cm3 pri 25 ° C).
Hustota pary
2,07 (s vzťahom vzduchu = 1).
Tlak vodnej pary
15,7 mmHg pri 25 ° C.
Rozklad
Keď sa zahrieva na viac ako 440 ° C, rozdeľuje sa, aby sa vytvoril oxid uhličitý a metán.
Hrebeň
1 056 MPASCAL pri 25 ° C.
Kričanie
Kyselina ľadová octová je vysoko korozívna a jej požitie môže u ľudí spôsobiť závažné lézie pažeráka a pylorusu.
Spaľovacie teplo
874,2 kJ/mol.
Odparovanie
23,70 kJ/mol pri 117,9 ° C.
23,36 kJ/mol pri 25,0 ° C.
pH
- Koncentračný roztok 1 m má pH 2,4.
- Pre roztok 0,1 m je jeho pH 2,9.
- A 3.4, ak je roztok 0,01 m.
Povrchové napätie
27,10 Mn/m A 25 ° C.
Pka
4,76 až 25 ° C.
Chemické reakcie
Kyselina octová je pre mnoho kovov korozívna, uvoľňuje plyn h2 a formovanie kovových soli nazývaných acetáty. S výnimkou octanu chrómu (II) sú acetáty rozpustné vo vode.
Jeho reakcia s horčíkom je predstavovaná nasledujúcou chemickou rovnicou:
Mg (s) +2 Cho3CoOH (ag) => (ch3Coo)2Mg (ag) +h2 g)
Redukciou tvorí kyselina octová etanol. Môžete tiež tvoriť anhydrid actickej straty vody z dvoch molekúl vody.
Kyselina octová používa
Priemyselný pracovník
- Kyselina octová reaguje s etylénom v prítomnosti kyslíka za vzniku monoméru vinylacetátu, s použitím paladium ako katalyzátora pre reakciu. Polymeriza vinylacetát v polyvinylacetáte, ktorý sa používa ako súčasť obrazov a adhezívneho materiálu.
- Reaguje s rôznymi alkoholmi na výrobu esterov vrátane etylacetátu a propylacetátu. Acetátové estery sa používajú ako atramentové rozpúšťadlá, nitrocelulóza, povlaky, laky a akrylové lakas.
Môže ti slúžiť: zliatiny- Kondenzáciou dvoch molekúl kyseliny octovej sa vytvorí anhydrid octovej, ch3Ko-koch3. Táto zlúčenina zasahuje do syntézy octanu celulózy, polyméru, ktorý predstavuje syntetickú tkaninu a používa sa pri vypracovaní fotografických filmov.
Ako rozpúšťadlo
- Je to polárne rozpúšťadlo schopné rozpúšťať polárne zlúčeniny, ako sú anorganické soli a cukry, ale tiež rozpúšťa nepolárne zlúčeniny, ako sú oleje a tuky. Kyselina octová je navyše miešateľná s polárnymi a nepolárnymi rozpúšťadlami.
- Misabilita kyseliny octovej v alkánoch závisí od rozšírenia ich reťazca: keďže sa zvyšuje dĺžka šnúry alkánov, jeho miešateľnosť s kyselinou octovou klesá.
Lekári
- Zriedená kyselina octová sa používa ako antiseptikum, aplikovaná topicky so schopnosťou napadnúť baktérie, ako sú streptokoky, stafylokoky a pseudomonas. V dôsledku tohto pôsobenia sa používa pri liečbe kožných infekcií.
- Používa sa v endoskopii Barrett Ezofagus, čo je stav, v ktorom je modifikovaný povlak pažeráka, ktorý sa stáva podobnou štrbine tenkého čreva.
- Zdá sa, že 3% gél kyseliny octovej je účinným adjuvans na liečbu vaginálnym liekom na misoprostol, ktorý v strednej štvrtine vyvoláva lekárske potraty, najmä u žien s vaginálnym pH 5 alebo viac.
- Používa sa ako náhrada za chemickú exfoliáciu. Komplikácie s týmto použitím sa však objavili, pretože bolo hlásené, prinajmenšom prípad popálení, ktoré utrpel pacient.
- Používa sa ako farbivo na detekciu ľudského papilomavírusu (HPV).
Jedlo
Ocot sa používa ako korenie a ochutenie potravín po stáročia, takže je to najznámejšia aplikácia kyseliny octovej.
Odkazy
- Čo je kyselina etanovú? Uzdravený z Byjusa.com
- OCTOVÁ KYSELINA. Obnovený z pubchem.Ncbi.NLM.NIH.Vláda
- Ľadovec kyseliny octovej. Obnovené z chemickej knihy.com

