Štruktúra benzoátu sodného, vlastnosti, použitia a riziká
- 651
- 152
- JUDr. Rudolf Čapkovič
On Benzoát sodný Je to organická soľ, ktorej chemický vzorec je C6H5Cesta. Vyskytuje sa alebo vytvára neutralizačnou reakciou medzi kyselinou benzoovou a hydroxidom sodným. Výsledkom je biela tuhá látka (nižší obrázok) vo vode a rozkladá sa zahrievaním pri 120 ° C.
Túto soľ nájdete prirodzene v niekoľkých ovociach a ďalších častiach zeleniny, ako sú: čučoriedky, slivky, hrozienka, škorica, nechty a jablká čuch. Je to tiež metabolit rias a rastlín.
 Benzoát sodný. Zdroj: Chemik10 v poľskej wikipédii [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)]
Benzoát sodný. Zdroj: Chemik10 v poľskej wikipédii [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0)] Benzoát sodný sa v tele akumuluje, pretože sa rýchlo kombinuje s glycínovou aminokyselinou za vzniku kyseliny hippurovej, ktorá je voľne vylučovaná močom.
Táto zlúčenina sa používa s konzervačnými podmienkami potravín, jej účinok je účinnejší na kyslé pH. Je to spôsobené prítomnosťou organických kyselín, ktoré poskytujú potravinám pH vhodné na pôsobenie benzoátu sodného; To ako také skončí vyčnievajúcim v kyseline benzoovej.
Táto soľ sa používa aj pri liečbe dedičných metabolických porúch cyklu močoviny, čo vytvára akumuláciu medziproduktu metabolitu, pre ktoré enzým, ktorý jeho procesy, je zlý.
Medzinárodný program chemickej bezpečnosti nezistil žiadny škodlivý vplyv benzoátu sodného na ľudí na spotrebu medzi 647 - 825 mg/kg telesnej hmotnosti.
Uvádza sa však, že benzoát sodný môže vyvolať pseudoallergické reakcie a zhoršiť príznaky u pacientov s častými epizódami urtikárie a astmou.
[TOC]
Štruktúra sodného
 Štruktúra sodného. Zdroj: Kamil9243 [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]
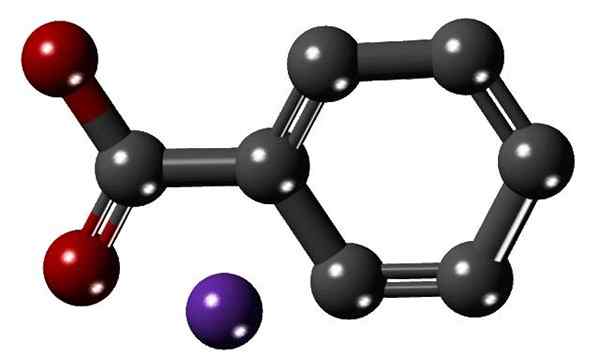
Štruktúra sodného. Zdroj: Kamil9243 [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)] Horný obrázok ukazuje štruktúru benzoátu sodného s modelom guľôčok a tyčí. Aromatický krúžok, so skupinou karboxylátu, sa môže všimnúť karboxylátom-, spojené s ním (červené sféry); a ten zase priťahuje elektrostaticky k katiónu+ (fialová guľa).
Pretože rozdiel vo veľkosti medzi oboma iónmi je veľký (porovnajte na obrázku), nie je zvláštne, že retikulárna energia kryštálov benzoátu sodného je nízka. To spôsobuje, že ich kryštály majú prirodzenú tendenciu solubilizovať v polárnych rozpúšťadlách alebo trpí sériou chemických reakcií.
Môže vám slúžiť: plynný stav: Charakteristiky, všeobecné právo, príkladyC6H5Coo- Môžete prijať dva mosty vodíka z dvoch molekúl vody, čo uprednostňuje jeho hydratáciu. Medzitým NA+ Končí tiež solvovanú vodou a prekonáva elektrostatické sily, ktoré ich udržiavajú spolu s C6H5Coo-.
Táto soľ teda pozostáva z C iónov6H5Coo- a na+, ktoré sú usporiadané usporiadaným spôsobom na stavbu kryštálov. V literatúre sa informácie nedosahujú, pokiaľ ide o jej kryštalickú štruktúru, takže nie je známe, aký je typ jednotkovej bunky pre túto soľ.
[TOC]
Vlastnosti
Chemické názvy
-Benzoát sodný
-Sodná soľ kyseliny benzoovej
-Sobenato
-Antimol.
Fyzický popis
Biele granule alebo kryštalický prach. Bezfarebný kryštalický prášok.
Vôňa
Záchod.
Príchuť
Horká, sťahová a nepríjemná.
zapaľovač
> 100 ° C.
Vlastné zapaľovanie
> 500 ° C.
Hustota
1,50 g/cm3.
Rozpustnosť
-Rozpustný v kvapalnom amónii a pyridíne.
-Malé rozpustné v etanole: 8,22 g/100 g pri 25 ° C.
-V metanolu je rozpustnejší ako v etanolu: 8,22 g/100 g pri 15 ° C.
Stabilita
Je stabilný za odporúčaných podmienok skladovania. Môže byť citlivý na vlhkosť, hydrolyzuje sa na kyselinu benzoovú. Nezlučiteľné so silnými oxidačnými činidlami, alkalismi a minerálnymi kyselinami.
Rozklad
Keď sa zahrieva na rozklad na 120 ° C (248 ° F), emituje aker dym oxidu sodného a ďalšie komponenty, ktoré môžu byť toxické a karcinogénne.
Rozkladom 120 ° C bráni presnému určovaniu jeho bodov varu a fúzie, pričom uvádzané hodnoty týchto parametrov sú teoretické odhady.
pH
Blízko 8, rozpustených vo vode. To znamená, že je to základná soľ. Je to preto, že je hydrolyzované na uvoľňovanie iónov OH-.
Povrchové napätie
72,9 Mn/cm pri 20 ° C v roztoku 1 g/l vody.
Syntéza
Kyselina benzoová zapojená do syntézy benzoátu sodného sa vytvára hlavne tromi metódami:
-Naftalén sa oxiduje vanádom pentoxidom za vzniku anhydridu ftálikovej. Táto zlúčenina môže byť nedostatočne boxilatel, aby vznikla kyselinou benzoovou, pretože vo svojej štruktúre s dvoma aromatickými kruhmi sa zdá.
-Toluén je oxidovaný na kyselinu benzoovú pridaním kyseliny dusičnej. V tejto reakcii „Simply“ Metilo Group oxiduje karboxylovú skupinu:
C6H5Chvály3 => C6H5Kohútik
-A nakoniec, benzotriclorid sa hydrolyzuje pôsobením minerálnych kyselín, čo spôsobuje kyselinu benzoovú.
Môže vám slúžiť: keramické materiály: charakteristiky, typy, príkladyZískala kyselina benzoová podľa ktorejkoľvek z týchto troch metód, potom sa rozpustí v hydroxidu sodného. Tieto zlúčeniny majú neutralizačnú reakciu, ktorá produkuje benzoát sodíka a vody.
C6H5COOH +NaOH => C6H5Cesta +h2Ani
Reakcia sa môže tiež vykonávať s uhličitanom sodným, hoci jeho výkon môže byť menší, ako je požadované.
Žiadosti
Jedlo
Benzoát sodný je činidlo konzervačného činidla v potravinách, ktoré je schopné inhibovať alebo oddialiť proces fermentácie, okyslení alebo akéhokoľvek procesu, ktorý ich spôsobuje zhoršenie. Okrem toho má benzoát sodný fungicídny účinok.
Táto soľ je schopná eliminovať kvasinky, baktérie a huby prítomné v potravinách. Jeho konzervačné pôsobenie je pre pH efektívnejšie < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Benzoát sodný sa používa aj na ochranu sýtených a nealkoholických nápojov, v ktorých je prítomná kyselina uhličitá. Tiež v džemoch bohatých na kyselinu citrónovú a všeobecne v potravinách s prítomnými kyselinami, ktoré vytvárajú kyslé médium.
Okrem toho sa používa v krmive s koncentráciou benzoátu sodného 0,1 %. Maximálne množstvo kyseliny benzoovej a benzoátu sodného, ako kondómy v potravinách, nepresiahne 2.000 mg/kg potravín.
Lekárske ošetrenie
Akútna hyperamonémia
Fenylaceate sodný a benzoát sodný sa používajú vo forme adjuvantných terapií pri liečbe akútnej hyperamonémie a súvisiacej flusopatie u pacientov s zmenami cyklu močoviny.
Tieto zlúčeniny sú klasifikované ako lieky na siroty. Táto nominálna hodnota sa vzťahuje na drogy, ktoré z ekonomického hľadiska nie sú ziskové.
Schizofrénia
Pri liečbe schizofrénie sa experimentálne používa benzoát sodný. Ústrednou časťou výskumu je úloha, že inhibícia oxidázových enzýmov d-uceinokyselín, aktivita, ktorú benzoát sodný spĺňa liečba pri liečbe.
Kyslý arginosuccín
Benzoát sodný sa používa pri liečbe kyseliny arginosukcínovej kyseliny, dedičnej metabolickej poruchy, ktorá môže spôsobiť u pacientov zvýšenie v koncentrácii amónneho, schopného ovplyvniť centrálny nervový systém.
Môže vám slúžiť: kyselina benzyová: syntéza, transpozícia a použitieInhibítor
-Je to inhibítor enzýmu Araquidonato 15-lipoxigenasa, enzýmu, ktorý vyšetruje farmaceutický priemysel za zapojenie sa do koronárnych plánov.
-Inhibuje pôsobenie trihaciridglyceridového lipázového enzýmu, enzýmu, ktorý pôsobí výrobu uvoľňovania glycerolu a mastných kyselín v tenkom čreve, čo umožňuje absorpciu týchto lipidov prítomných v potravinách.
Možno možné použitie benzoátu sodného na reguláciu črevnej absorpcie lipidov, ako sú triacylglyceridy.
Dedičné poruchy
Benzoát sodný sa používa pri liečbe niekoľkých dedičných porúch, ktoré súvisia s metabolizmom aminokyselín, medzi ktorými sa uvádza: Liečba hyperargininémie a liečba nedostatku translokázového enzýmu ornitinetinetine.
Ďalší
-Používa sa v alkoholických výplach. Okrem toho sa používa pri vypracovaní pyrotechnických zlúčenín, ktoré sú zodpovedné za píšťalku, ktorý sa vyrába, keď sú osvetlené.
-Používa sa ako antikorózne, čo je jednou z hlavných požiadaviek na výrobu tejto soli. Používa sa tiež v chladivách, nemrznúcej zmesi a iných systémoch založených na vode.
-Pri formulácii plastov, ako je polypropylén, sa používa na zlepšenie jeho odporu a čistoty.
-Slúži ako stabilizátor v kúpeľniach a fotografických procesoch.
Riziká
Benzoát sodný je podľa FDA klasifikovaný ako „všeobecne bezpečný“ v dávke 0,1 % hmotnosti potravín. Nepovažuje sa za dráždivé kontakt s kožou a očami, takže sa dá povedať, že akútna toxicita je nízka.
Benzoát sodný však môže prostredníctvom kontaktu produkovať neimunologické reakcie (pseudoallergia). Tento účinok je u normálnych ľudí zriedkavý, ale u pacientov s epizódami častých symptómov urtikov alebo astmy môže dôjsť k zvýšeniu frekvencie týchto príznakov.
V štúdiách uskutočňovaných u potkanov a myší sa nenašli žiadne náznaky karcinogénneho pôsobenia benzoátu sodného.
Nepohodlie jej použitia v prítomnosti kyseliny askorbovej, ktorá by mohla produkovať benzén; Toxická zlúčenina, naznačená ako karcinogénna.
Odkazy
- Priemysel. (2019). Výroba benzoátu sodného. Získané z: vedy.šarvák.orgán
- Wikipedia. (2019). Benzoát sodný. Zdroj: In.Wikipedia.orgán
- Publikácia. (2019). Benzoát sodný. Získané z: pubchem.Ncbi.Nim.NIH.Vláda
- Hanes t. (2019). Fakty o benzoáte sodného. Živý. Získané z: Livestrong.com
- Chemická kniha. (2017). Benzoát sodný. Obnovené z: Chemicalbook.com
- Pruh h. a kapusta. (2013) Jama Psichiatry. 70 (12): 1267 - 1275.
- Svetová zdravotnícka organizácia Ženeva. (12. apríla 2005). Kyselina benzoová a benzoát sodný. [PDF]. Uzdravil sa od: kto.int

