Benzylodénový bencil, karbocations, benzylové radikály

- 4103
- 1094
- Tomáš Mydlo
On benchíl alebo benzyl Je to bežná náhradná skupina v organickej chémii, ktorej vzorec je C6H5Chvály2- alebo bn-. Štrukturálne jednoducho pozostáva zo spojenia skupiny metylénu, Cho2, S fenylovou skupinou, c6H5; To znamená SP3 Spojené priamo s benzénovým krúžkom.
Preto je skupina Benchilo vnímaná ako aromatický krúžok pripevnený k malej reťazci. V niektorých textoch je uprednostňované použitie skratky BN namiesto C6H5Chvály2-, Rozpoznajte ho ľahko v akejkoľvek zlúčenine; Najmä ak je spojený s atómom kyslíka alebo dusíka, O-BN alebo NBN2, respektíve.
 Skupina Bencilo. Zdroj: Ingraralhaosului [verejná doména]
Skupina Bencilo. Zdroj: Ingraralhaosului [verejná doména] Táto skupina je tiež implicitne v sérii všeobecne známych zlúčenín. Napríklad na kyselinu benzoovú, C6H5Cooh, možno by sa považovať za lavenka, ktorého uhlík automobilu3 utrpel vyčerpávajúcu oxidáciu; alebo benzaldehyd, c6H5Cho, čiastočnej oxidácie; a benzylalkohol, c6H5Chvály2Och, ešte menej oxidované.
Ďalším trochu zrejmým príkladom tejto skupiny je v Tolueno, c6H5Chvály3, ktoré môžu trpieť určitým počtom reakcií po nezvyčajnej stabilite v dôsledku radikálov alebo benzylových karbocacií. Skupina Bencilo však slúži na ochranu skupín OH alebo NH2 reakcií, ktoré nepopierane modifikujú produkt na syntézu.
[TOC]
Príklady zlúčenín s grupo benchílom
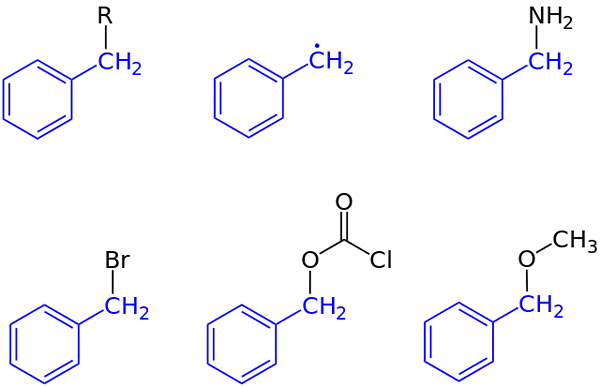 Zlúčeniny skupiny Bencilo. Zdroj: Jü [verejná doména]
Zlúčeniny skupiny Bencilo. Zdroj: Jü [verejná doména] Na prvom obrázku bolo uvedené všeobecné znázornenie zlúčeniny so skupinou Bencil: C6H5Chvály2-R, kde R môže byť akýkoľvek iný molekulárny fragment alebo atóm. Rôzny R teda môže získať vysoký počet príkladov; Niektoré jednoduché, iné len pre konkrétnu oblasť štruktúry alebo väčšie množstvo.
Napríklad benzylický alkohol odvodzuje z výmeny r za OH: C6H5Chvály2-Oh. Ak namiesto OH je to skupina NH2, Potom vzniká zlúčenina bencelamínu: C6H5Chvály2-NH2.
Môže vám slúžiť: Borohydrid sodný (NABH4): Štruktúra, vlastnosti, použitiaAk atóm, ktorý nahrádza R, je BR, zlúčenina je benchl bromid: C6H5Chvály2-BR; R od co2CL pochádza z esteru, chlorocarbonátu benchilu (alebo karobenzoxylchloridu); a ok3 vzniká benzilový metyléter, c6H5Chvály2-Okradnúť3.
Dokonca (aj keď vôbec nie správne), R sa dá predpokladať osamelým elektrónom: benzyl radikál, C6H5Chvály2·, Produkt uvoľňovania radikálneho r ·. Ďalším príkladom, hoci nie je zahrnutý do obrazu, je fenylacetonitril alebo kyanid lavicilo, C, C6H5Chvály2-CN.
Existujú zlúčeniny, v ktorých skupina Lachíl sotva predstavuje špecifickú oblasť. Ak je to tak, skratka BN sa zvyčajne používa na zjednodušenie štruktúry a jej ilustrácií.
Benzyldrogény
Vyššie uvedené zlúčeniny majú spoločné nielen aromatický alebo fenylový kruh, ale aj benzylové hydrogény; To sú tí, ktorí patria do SPO uhlíka3.
Takéto hydrogény môžu byť reprezentované ako: BN-CH3, BN-CH2R alebo bn-chr2. BN-CR zlúčenina3 Chýba mu benzyl vodík, a preto je jeho reaktivita menšia ako reaktivita ostatných.
Tieto hydrogény sa líšia od tých, ktoré sú zvyčajne spojené s uhlíkom SP A3.
Zvážte napríklad metán, Cho4, ktoré je možné napísať aj ako Cho3-H. Rozbiť odkaz Cho3-H V heterolytickom prasknutí (radikálna tvorba) sa musí dodať určité množstvo energie (104 kJ/mol).
Energia pre rovnaké väzobné prasknutie C však6H5Chvály2-H je nižší v porovnaní s metánom (85 kJ/mol). Je menej energie, naznačuje, že radikálne C6H5Chvály2· Je to stabilnejšie ako Cho3·. To isté sa stáva vo väčšej alebo menšej miere s inými benzyldrogénmi.
V dôsledku toho sú benzylové hydrogény reaktívnejšie pri vytváraní radikálov alebo karbocations stabilnejších ako tie, ktoré sú spôsobené inými hydrogénmi. Pretože? Otázka je zodpovedaná v nasledujúcej časti.
Môže vám slúžiť: Kyselina benzoová (C6H5COOH)Benzyické karbocations a radikály
Radical C sa už uvažoval6H5Chvály2·, Chýbajúce benzylové karbocation: C6H5Chvály2+. V prvom je zmiznutý a osamelý elektrón a v druhom elektronickom nedostatku. Tieto dva druhy sú veľmi reaktívne a predstavujú prechodné zlúčeniny, z ktorých pochádzajú konečné produkty reakcie.
Uhlík SP3, Po strate jedného alebo dvoch elektrónov za vzniku radikálnej alebo karbocation, respektíve, môžete prijať hybridizáciu SP2 (trigonálna rovina), takže medzi elektronickými skupinami existuje najmenší možný odpor. Ale ak sa stane SP2, Rovnako ako uhlíky aromatického kruhu, môže dôjsť k konjugácii? Odpoveď je áno.
Rezonancia v skupine Bencilo
Táto konjugácia alebo rezonancia je kľúčovým faktorom pri vysvetľovaní stability týchto benzylových druhov alebo bencilu. Na nasledujúcom obrázku je ilustrovaný taký jav:
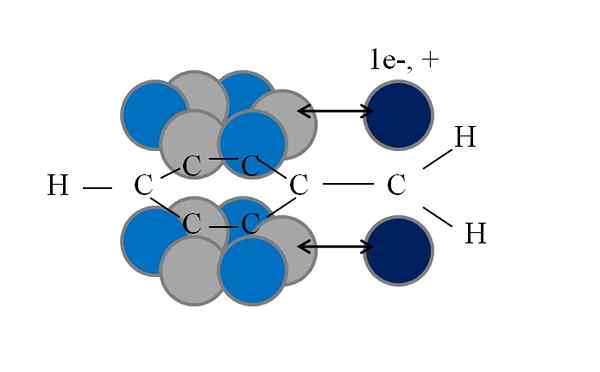 Konjugácia alebo rezonancia v skupine Benchilo. Ostatné hydrogény boli vynechané na zjednodušenie obrázka. Zdroj: Gabriel Bolívar.
Konjugácia alebo rezonancia v skupine Benchilo. Ostatné hydrogény boli vynechané na zjednodušenie obrázka. Zdroj: Gabriel Bolívar. Všimnite si, že tam, kde bol jedným z benzylových hydrogénov orbitál p So zmiznutým elektrónom (radikálne, 1E-) alebo prázdnota (karbocation, +). Ako je vidieť, tento orbitálny p Je rovnobežná s aromatickým systémom (sivé a modré kruhy), pričom dvojitá šípka označuje začiatok konjugácie.
Zmiznutý elektrón aj kladné zaťaženie sa teda môžu prenášať alebo dispergovať aromatickým kruhom, pretože paralelizmus jeho orbitálov ho geometricky uprednostňuje. Tieto sa však nenachádzajú v žiadnom orbitáli p aromatického kruhu; Iba v tých, ktorí patria k uhlíkom v orto pozíciách a pre ch2.
Môže vám slúžiť: kvantitatívna analýza v chémii: merania, prípravaZ tohto dôvodu je jasné modré kruhy vynikajúce nad šedým: v nich sa koncentruje negatívna alebo pozitívna hustota radikálu alebo karbocation.
Ďalšie radikály
Za zmienku stojí, že táto konjugácia alebo rezonancia sa nemôže vyskytnúť v uhlíkach SP3 vzdialenejší od aromatického kruhu.
Napríklad radikálne C6H5Chvály2Chvály2· Je to oveľa nestabilnejšie, pretože zmiznutý elektrón nemožno konjugovať s krúžkom, keď je skupina podaná2 medzi hybridizáciou SP a s3. To isté platí pre C6H5Chvály2Chvály2+.
Reakcie
Stručne povedané: benzylové hydrogény sú náchylné na reagovanie, buď generujú radikálnu alebo karbocation, čo končí zase a spôsobuje konečný produkt reakcie. Preto reagujú prostredníctvom mechanizmu SN1.
Príklad pozostáva z toluénovej bromácie pri ultrafialovom žiarení:
C6H5Chvály3 + 1/2br2 => C6H5Chvály2Br
C6H5Chvály2BR + 1/2BR2 => C6H5Chbr2
C6H5Chbr2 + 1/2br2 => C6H5CBR3
V skutočnosti v tejto reakcii existujú radikály BR ·.
Na druhej strane samotná skupina Lachilo reaguje na ochranu skupín OH alebo NH2 V jednoduchej náhradnej reakcii. Roh alkohol teda môže byť „benzilad“ pomocou benchilo bromidu a iných reagencií (KOH alebo NAH):
Roh + bnbr => robn + hbr
Robn je benzyléter, ku ktorému je možné jeho počiatočnú OH skupinu vrátiť, ak je vystavený reduktívnemu médiu. Tento éter musí zostať nezmenený, zatiaľ čo ďalšie reakcie sa vykonávajú v zlúčenine.
Odkazy
- Morrison, r.Tón. A Boyd, r. N. (1987). Organická chémia. (5. vydanie). Addison-Wesley Iberoamericana.
- Carey, f. Do. (2008). Organická chémia. (6. vydanie). McGraw-Hill, Intermerica, editor S.Do.
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. Amín. (10. vydanie.). Wiley Plus.
- Wikipedia. (2019). Benzylová skupina. Zdroj: In.Wikipedia.orgán
- DR. Donald L. Robertson. (5. decembra 2010). Fenyl alebo benzyl? Získané z: Domov.Miracosta.Edu
- Gamini Gunawardena. (12. októbra 2015). Benzylové karbocation. Chémia librettexts. Získané z: Chem.Librettexts.orgán
- « Vysvetlenie zloženej proporcionality, tri zložené pravidlo, cvičenia
- Funkcie hematopoyetického systému, tkaniny, histológia, orgány »

