Koncept nájomného, bežnejšie radikály, štruktúra
- 1686
- 217
- Gabriel Bahna
A Prenajímam sa Je to skupina alebo substituent, ktorý odvodzuje z alkánu odstránením jedného z jeho vodíkov. Preto sa skladá z uhlíka a vodíka a jeho všeobecný vzorec je CnH2n+1, namiesto cnH2n+2 Pre všetky necyklické alkány, to znamená lineárne alebo rozvetvené reťazce.
Nájomné ako skupina je symbolizované písmenom r. Molekulárna štruktúra mnohých organických zlúčenín sa teda dá zovšeobecniť zavedením R. V nich je R iba časťou molekuly, ktorá je spojená s jeho kostrou alebo reaktívnou funkčnou skupinou.
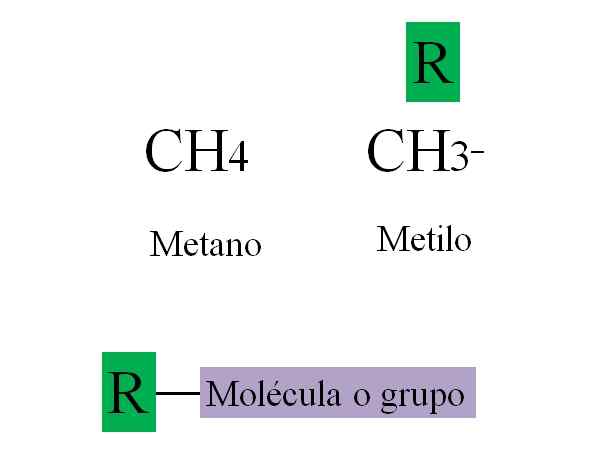 Prenájom. Zdroj: Gabriel Bolívar.
Prenájom. Zdroj: Gabriel Bolívar. Vynikajúci obrázok je uvedený vyššie uvedený. Metano, ch4, Je to alkán, a keď stratí jeden zo svojich vodíkov, spájajúci sa s molekulou alebo skupinou, transformuje sa na metyl, ch3-. Metyl nie je zlúčenina: neexistuje ako voľná molekula; Pokiaľ to nie je metyl radikál, cho3·, Ktorý je vysoko reaktívny.
Nájomné, symbolizované r, tvorí kovalentné puto so zvyškom molekuly. Teda alquilitické zlúčeniny sú znázornené ako RG, kde G je skupina, ktorá zahŕňa celú molekulu. Napríklad alkoholy majú receptúru ROH, takže sú to alkylové zlúčeniny.
[TOC]
Menovanie
Nomenklatúra nájomného nemá nič spoločné s príjmom nehnuteľnosti. To pochádza z tej istej nomenklatúry alkáne, z ktorej odvodzuje. Napríklad na obrázku vyššie sa metán transformuje do metylovej skupiny. Preto stačí nahradiť ukončenie -rok, názvu alkáne, ukončením -ilo.
Ďalší príklad má od etánu, Cho3Chvály3. Pri strate jedného zo svojich vodíkov a spojená s molekulou alebo skupinou sa transformuje do etylovej skupiny, ch3Chvály2-.
Môže vám slúžiť: Typ odkazu CO2Rovnakým spôsobom sa vyskytuje u všetkých ostatných alkánov, dokonca aj tie, ktoré pozostávajú z cyklických reťazcov, ako je cyklohexan, ktoré sa transformujú do cyklohexyl.
Radikály bežnejšie
Alkynd Radicals sú tie „voľné a reaktívne kúsky“, ktoré sa získajú, keď sa R oddelí od molekuly. Ich hojnosť je úmerná pre prenajaté skupiny, z ktorých odchádzajú. Napríklad skupina Metilo, Cho3- A radikálny metyl, cho3· Sú relatívne rovnaké ako bežné.
Všeobecne sú najbežnejšie radikály alebo prenájom skupín, ktoré pochádzajú z alkánov obsahujúcich menej ako päť atómov uhlíka v kostre. To znamená nad Pentano a všetky jeho izoméry, tieto radikály sa stávajú ťažšími nájdenými.
Pretože? Existujú dva dôvody. Prvým je, že molekuly uhľovodíkov v podmienkach s vysokou energiou majú tendenciu trpieť prasknutím väzieb, takže ich molekulárne veľkosti a hmoty sú znížené.
A druhým je, že v prírode existujú „izomérové polievky“, ktoré je veľmi ťažké vyčistiť destiláciou kvôli malému rozdielu medzi ich bodmi varu.
Je teda to, že najhojnejšie alkygly a ich radikály sú radikály s krátkym reťazcom, s množstvom atómov uhlíka menej ako šesť. Príklady týchto alks sú: ch3-, Chvály3Chvály2-, Chvály3Chvály2Chvály2-, Chvály3Chvály2Chvály2Chvály2-, a jeho možné izoméry.
Štruktúra
Doteraz mali adresované ALKS štruktúry lineárneho reťazca. Jeho štruktúry, ako sa očakávalo, sú rovnaké ako štruktúry Alkánov tých, ktorí postupujú.
Lineárne Lefes budú mať za následok lineárne alkimálne skupiny. Na druhej strane rozvetvené vrcholy budú generovať rozvetvené alkaly. To isté sa stáva s cyklickými alkanami.
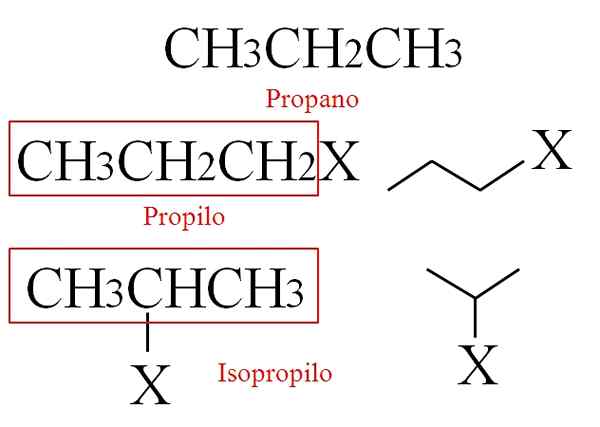
Môže vám slúžiť: jodometria: základy, reakcie, všeobecný postup, použitieLineárne alkány však môžu tiež spôsobiť zdanlivo rozvetvené alkaly, v závislosti od toho, ktoré z jeho atómov uhlíka stráca vodík. Zoberme si príklad propánu:
 Štruktúra propánu a jej odvodené skupiny alkle. Zdroj: Gabriel Bolívar.
Štruktúra propánu a jej odvodené skupiny alkle. Zdroj: Gabriel Bolívar. Ak stratíte vodík z ktoréhokoľvek zo svojich primárnych uhlíkov, to znamená z jej koncov3Chvály2Chvály2-.
Medzitým, ak ho vodík stráca zo svojho sekundárneho alebo centrálneho uhlíka, získa sa izopropylová skupina (ch3)2Chvály-. Na obrázku sú zobrazené dve zlúčeniny RX, pričom R je propyl alebo izopropil.
Vlastnosti
Skupiny prenájmu zvyčajne nereagujú, pretože ich odkazy C-C alebo C-H nie je ľahké rozbiť. Bez ohľadu na ich molekulárnu štruktúru, všetci zdieľajú spoločnú vlastnosť: hydrofóbnosť. To znamená, že nevykazujú afinitu k vode ani k polárnemu rozpúšťadlu. Ale robia pre tuky.
Keď je skupina Renta R veľmi veľká alebo keď je ich v molekule veľa, jej hydrofóbnosť sa zvyšuje. To isté tvrdí, že sa zvyšuje jeho lipofilita (láska k tukom). Čím viac je „prenajatejšia“ molekula je, tým väčšia afinita bude mať tuk a ťažšie bude ju odstrániť vodou.
Príklady alkylových zlúčenín
Pojem „alkylové zlúčeniny“ je mimoriadne nejednoznačný, pokiaľ ide o organickú chémiu. Skupina alebo molekula, ktorej je skupina Rento R vždy predoritívna, má vždy prioritu. A práve tieto skupiny alebo molekuly definujú rodiny organických zlúčenín.
Ak sú však tieto skupiny častejšie v anorganickej chémii, rovnako ako u halogénov a sulfátov, je daná určitá dôležitosť alquylovej zložke. Na objasnenie tohto bodu budú uvedené niektoré príklady.
Môže vám slúžiť: Vodík: História, štruktúra, vlastnosti a použitiaPrenášať hackery
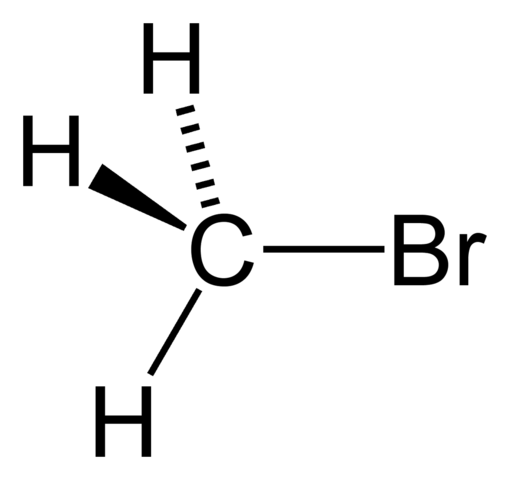 Metyl bromid
Metyl bromid Prenájom haluros má všeobecný recept RX, kde X je halogén atóm (F, Cl, Br a I) a r akejkoľvek náhrady skupiny alebo alkylu. Napríklad Cho3Br je metylbromid.
Prenájom sulfátov
 Sulfát
Sulfát Nájomné sulfáty majú všeobecný vzorec Roso3R ', kde r a r' sú dve alkal skupiny, ktoré môžu byť rovnaké alebo iné. Máme teda DiMetylsulfát, Cho3Nosiť3Chvály3 alebo ja2SW4.
Prenášať
Nájomné borati majú všeobecný vzorec (RO3) B. Napríklad (CHO3Chvály2Buď)3B o (eto)3B sa nazýva etyl boritar.
Triaquilboros
Podobne máme Triaquilboros, ktorého všeobecný vzorec je r3B. Napríklad (CHO3)3B o Me3B sa nazýva trimetylborano (TMB).
Alkoholy
Alkoholy sú tiež alquilické zlúčeniny a ich všeobecný vzorec je ROH. Jediná prítomnosť skupiny OH však stráca význam pre prenajaté skupiny. Alkoholy sa nazývajú „alkyl hydroxidy“, pretože nájomné ako také nie sú najzákladnejšími časťami ich molekúl, ale OH.
Na druhej strane, v predchádzajúcich príkladoch sa kladie dôraz na prítomnosť prenajatých skupín r; Pretože halogény, sulfáty, boros a boratos sú veľmi.
Odkazy
- Morrison, r. Tón. a Boyd, R, N. (1987). Organická chémia. 5. vydanie. Redakčný Addison-Wesley Inter-American.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. (10. vydanie.). Wiley Plus.
- Wikipedia. (2020). Alkyl. Zdroj: In.Wikipedia.orgán
- Danielle Reid. (2020). Alkyl Group: Definícia a prehľad. Štúdium. Získané z: štúdie.com
- Chémia librettexts. (6. apríla 2020). Alkylové skupiny. Získané z: Chem.Librettexts.orgán
- « Normy sociálneho koexistencie, formy, dôležitosť, príklady
- Charakteristické voltmeter, prevádzka, čo je pre, typy »

