Štruktúra oxidu hliníka, vlastnosti, použitie, nomenklatúra
- 1686
- 237
- Václav Višňovský
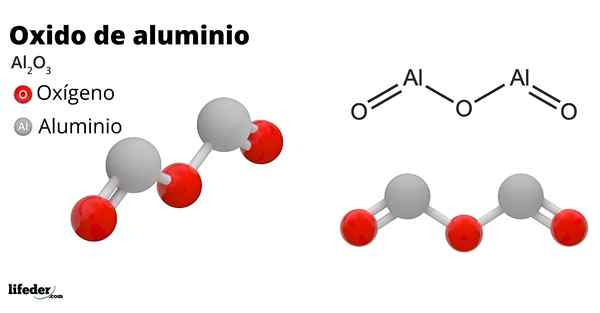
On oxid hliníka, Hliník, oxid hlinitý, oxid hlinitý, corindon alebo oxid hliníka, je to anorganická zlúčenina, ktorej chemický vzorec je do2Ani3. Je to oxid amfotera, hoci sa môže stať v dôsledku liečby takmer inertnou zlúčeninou.
Má veľkú tvrdosť, odolnosť proti korózii a vysoký elektrický odpor. Tieto vlastnosti okrem iného umožnili oxidu hliníka mať početné aplikácie, ako napríklad: elektrická izolácia, abrazívny materiál, implantáty kostí a zubov atď.
Bauxit je hlavným zdrojom získania oxidu hliníka. Na druhej strane Corindon je minerál oxidu hlinitého, ktorý je vo voľnom stave vo forme a-al2Ani3. Corindon má tvrdosť 9.0 a kvôli niektorým nečistotám produkuje drahé kamene, ako sú Sapphire a Ruby.
Elektrolýza oxidu hliníka slúžila ako základ pre izoláciu hliníka Humphry Davy v roku 1808. Rovnaká metóda s niektorými úpravami sa v súčasnosti používa pri výrobe kovového hliníka.
[TOC]
Štruktúra
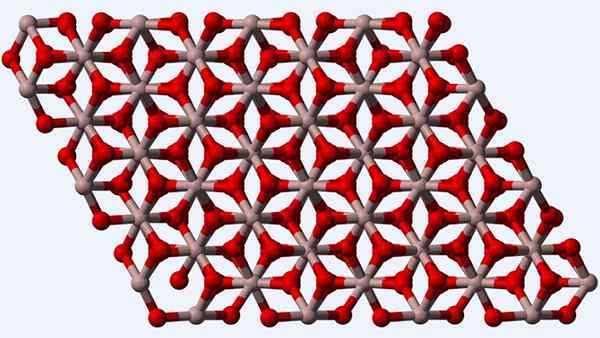 Kryštalická štruktúra fázy a-AL2O3 alebo Corindon
Kryštalická štruktúra fázy a-AL2O3 alebo Corindon Corindon alebo fáza a-al2Ani3, Pretože je termodynamicky stabilnejší polymorf pre oxid hlinitý, jeho štruktúra (vynikajúci obraz) sa považuje za hlavnú v čase jeho charakterizácie. Táto štruktúra je trigonálna, s iónmi do3+ obklopený šiestimi resp2-, a preto založenie Octaedros al6 s interakciami al-o u al-o.
Okrem Corindón, Al2Ani3 Existuje tiež ako iné metastabilné polymorfy, vrátane: y-al2Ani3 a η-al2Ani3 (kubické), 9-at2Ani3 (monoklinické), χ-al2Ani3 (Hexagonal), κ-al2Ani3 (Ortorrombické) a δ-al2Ani3 (Tetragonálne alebo ortorrombické).
Ako Al2Ani3, Octudra sa „láme“ v Tetrahedros al4 o pentaedros alo5. Po roztavení a znova vychladnite, môžete získať sklovecový oxid hlinitý, to znamená amorfný, so zmesami polyhedry alm5 a všetko6.
Môže vám slúžiť: Einstenio (S): Štruktúra, vlastnosti, získavanie, použitie, použitiaVlastnosti oxidu hliníka
 Hliníkový hliníkový hliníkový kus hliníka
Hliníkový hliníkový hliníkový kus hliníka Fyzický vzhľad
Pevný alebo biely kryštalický prášok
Molárna hmota
101.96 g/mol
Vôňa
Záchod
Hustota
3.798 g/cm3
Bod topenia
2072 ° C
Bod varu
2977 ° C
Rozpustnosť
Nerozpustný vo všetkých rozpúšťadlách vrátane vody.
Tepelná vodivosť
30 w · m-1· K-1. Napriek svojmu keramickému použitiu má relatívne vysokú tepelnú vodivosť.
Index lomu
1.768-1.760
Tvrdosť
Je to zlúčenina, ktorá predstavuje veľmi vysokú tvrdosť s hodnotou 9.0 na stupnici tvrdosti Mohs vo forme oxidu a-hliník (Corindón).
Elektrický odpor
Pri 300 ° C: 1.2 x 1013 Ohms · cm. Hliník alebo oxid hliníka je preto elektrický izolátor.
Reaktivita
Al2Ani3 Napriek slabo reagovaním s alkalismi a vo väčšej miere s kyselinami sa považuje za chemický amfoter. Keď sa však zahrieva pri viac ako 800 ° C, získa takmer inertný stav k pôsobeniu kyselín.
Tento oxid je zodpovedný za ochranu hliníka pred korozívnymi činidlami v oblasti životného prostredia, pretože pevne pokrýva povrch kovu bez rozpadnutia alebo prasknutia.
Menovanie
Nomenklatúra Al2Ani3 Je to jednoduché. Systematicky známy ako Diauminum Trioxid. Pretože tento oxid hliníka existuje, vo svojej zásobnej nomenklatúre nie je špecifikovaná kovová valencia (III). Jeho názov je tiež tradične zhrnutý s oxidom hliníka tým, že má iba jednu valenciu.
Použitie/aplikácie
Pohár
Oxid z hliníka zasahuje do vypracovania skla hliníka silikato. Toto žiaruvzdorné sklo, odolné voči tepelnému šoku, sa môže použiť pri vyšších teplotách ako sklo-bórové sklo; Aj keď má nižšiu chemickú odolnosť.
Pridanie malého množstva magnézie transformuje nepriehľadné sklo hlinitého na priesvitný, čo je možné použiť ako plyn. Používa sa tiež pri príprave poťahovacích suspenzií určitých typov fluorescenčných žiaroviek.
Môže vám slúžiť: Rodio: História, vlastnosti, štruktúra, použitie, rizikoKatalyzátor
Aktivovaný hliník má granulárnu a pórovitú charakteristiku, ktorá môže mať katalytickú aktivitu alebo slúži ako podpora aktivity iných katalyzátorov. Okrem iných procesov hliníka zasahuje do katalýzy polymerizácie etylénexidu.
Mikrobicídna aktivita
Častice oxidu nano-hliníka priľnú na povrch baktérií, čo spôsobuje ich smrť. Podobne bol preukázaný podobný účinok na huby rodu Candida.
Elektrický izolátor
Oxid z hliníka má vysoký elektrický odpor, čo mu dáva schopnosť pôsobiť ako elektrický izolátor. Preto sa používa v integrovaných obvodových balíkoch. Používa sa tiež v supravodičových zariadeniach a ako dielektrický kondenzátor alebo kondenzátory. Okrem toho sa používa ako izolátor v elektrických zapaľovacích sviečkach.
Drsný
 Corindon, kryštalický a tvrdší oxid hlinitý, slúži na zostavenie abrazívnych nástrojov. Zdroj: Rob Lavinsky, Irocks.com-ccy-SA-3.0, CC By-SA 3.0, cez Wikimedia Commons
Corindon, kryštalický a tvrdší oxid hlinitý, slúži na zostavenie abrazívnych nástrojov. Zdroj: Rob Lavinsky, Irocks.com-ccy-SA-3.0, CC By-SA 3.0, cez Wikimedia Commons Vysoká tvrdosť minerálu Corindonu umožňuje jeho používanie ako abrazívne náklady ako diamanty, v priemysle a pri vŕtaní ropy.
Corindon získava tok drahého kameňa, ako je červený rubín, kvôli kontaminácii chrómov; Alebo ako modrý zafír, kvôli znečisteniu železa a titánu. Mnoho druhov brúsneho papiera používaného v kovu a dreve má kryštály oxidu hliníka.
Húževnatosť alebo schopnosť vyhnúť sa prasknutiu oxidu hlinitého s pridaním zirkónia alebo karbidu kremíka, čo umožňuje jeho použitie v priemyselných nástrojoch rezania. Okrem toho sa oxid hliníka používa v zubných krémoch na leštenie zubov.
Môže vám slúžiť: chromát zinku: štruktúra, vlastnosti, získanie, použitieNiektoré prezentácie oxidu hlinitého sa používajú ako brúsivy dermatológmi pri liečbe určitých kožných stavov.
Odvlhčovač plynu
Oxid z hliníka je zlúčenina s avid vodou, takže sa môže použiť na jeho extrahovanie z plynných prúdov.
Spomaľovač horenia
Nano-častice hydroxidu oxidu hlinitého (Bohemita) pôsobí ako rozptyľovač tepla, uvoľňuje vodu a oneskorenie vzhľadu plameňov.
Tvrdé tkanivové implantáty
Oxid z hliníka je zlúčenina s veľkou tvrdosťou, chemicky inertný a odolný voči korózii, okrem toho, že má bielu farbu. Pre tieto vlastnosti sa používa ako náhrada za tvrdé tkanivá, ako sú kosti a zuby. Podobne sa materiál postavený z oxidu z hliníka použil pri výmene kĺbu.
Získanie
 Bauxit. Zdroj: max.Kit, CC BY-SA 4.0, cez Wikimedia Commons
Bauxit. Zdroj: max.Kit, CC BY-SA 4.0, cez Wikimedia Commons Bauxitu je hlavným minerálom, ktorý získal oxid hlinitý, ktorý sa tvorí zmesou troch minerálov: gibbsite, laboehmita a diaspóra.
Oxid z hliníka sa extrahuje z minerálov podľa Bayerovho postupu. Pozostáva z horúcej bauxitu reakcie s hydroxidom sodným, reakciu produkovanú hlinitou sodným [Naal (OH)4].
Keď je predchádzajúci roztok ochladený, zrážanie hydroxidu hlinitého sa vyrába v tuhej forme. Potom sa tento hydroxid zahrieva do 1100 ° C, čo produkuje oxid hlinitý.
Odkazy
- Whitten, Davis, Peck & Stanley. (2008). Chémia. (8. vydanie.). Učenie sa.
- Triasť a Atkins. (2008). Anorganická chémia. (Štvrté vydanie). MC Graw Hill.
- Wikipedia. (2020). Oxidový hliník. Zdroj: In.Wikipedia.orgán
- Národné centrum pre biotechnologické informácie. (2020). Oxidový hliník. Pubchem Comunund Zhrnutie pre CID 9989226. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Kushagri s. a kol. (2019). Antivírusový a antimikrobiálny potenciál nano liečiv: oxid hlinitý nanočastíc. Zdroj: ScienceDirect.com
- Redaktori Enyclopaedia Britannica. (2020). Alumina. Získané z: Britannica.com
- Lohninger Hans. (15. augusta 2020). Oxidový hliník. Chémia librettexts. Získané z: Chem.Librettexts.orgán
- « Aromatický elektrofilný substitučný mechanizmus a príklady
- 30 príklady etiky a morálky v každodennom živote »

