Charakteristiky Valina, funkcie, bohaté potraviny, výhody
- 2203
- 406
- JUDr. Rudolf Čapkovič
Ten Valina Patrí do 22 aminokyselín identifikovaných ako „základné“ zložky proteínov; Je identifikovaný s skratkou „Val“ a písmenom „V“. Táto aminokyselina nemôže byť syntetizovaná ľudským telom, preto je katalogizovaná v skupine deviatich esenciálnych aminokyselín pre ľudí.
Mnoho guľových proteínov má vnútorný vnútorný valín a leucínový odpad, pretože obidve sú spojené hydrofóbnymi interakciami a sú nevyhnutné pre skladanie štruktúry a trojrozmernú konformáciu proteínov.
 Chemická štruktúra aminokyselinového valínu (zdroj: klavecín [CC By-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)] Via Wikimedia Commons)
Chemická štruktúra aminokyselinového valínu (zdroj: klavecín [CC By-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)] Via Wikimedia Commons) La Valina bol prvýkrát očistený v roku 1856 V V. Grup-Besanez z vodného extraktu z pankreasu. Názov „Valina“ však vytvoril e. Fisher v roku 1906, keď sa mu podarilo umelo syntetizovať a poznamenal, že jej štruktúra bola veľmi podobná štruktúre kyseliny, ktorá sa nachádza v rastlinách bežne známych ako „Valerianas“.
Valín je jednou z aminokyselín nachádzajúcich sa v polohách zachovaných v určitých proteínoch zdieľaných stavovcami, napríklad v 80 polohe cytochrómu C stavovcov sú leucín, valín, izoleucín a metóda v rovnakom poradí v rovnakom poradí.
V tkanivách alebo biomateriáloch s rezistentnými, tvrdými a elastickými charakteristikami, ako sú väzy, šľachy, krvné cievy, vlákna alebo web, existuje veľké množstvo valínu, ktoré poskytujú flexibilitu a odolnosť vďaka svojim hydrofóbnym interakciám s inými aminokyselinami.
Nahradenie glutamátového zvyšku jedným z valínu v β reťazci hemoglobínu, proteín zodpovedný za transport kyslíka krvou spôsobuje zlú tvorbu v proteínovej štruktúre, čo spôsobuje hemoglobín „S“.
Táto mutácia produkuje falciformnú anémiu alebo drepanocytózu, patologický stav, v ktorom červené krvinky získavajú formu polmesiaca alebo charakteristického hozu, čo ich odlišuje od normálneho, zaobleného a splošteného vzhľadu.
Niektoré z najpoužívanejších herbicídov majú v súčasnosti aktívne zlúčeniny na sulfonylmočovinu a metylsulfometurón, ktoré spôsobujú poškodenie enzýmovej acetolaktátovej syntázy, ktoré sú potrebné pre prvý krok syntézy valínu, leucínu a izoleukínu. Poškodenie spôsobené týmito pesticídmi bráni bylinám a burinám, ktoré sa zvyčajne môžu vyvinúť.
[TOC]
Charakteristika
Valina je aminokyselina s päťkarbónovým kostrom a patrí do aminokyselinovej skupiny s alifatickými bočnými reťazcami. Jeho hydrofóbny charakter je taký, že sa dá porovnávať s fenylalanínom, leucínom a izoleucínom.
Aminokyseliny, ktoré majú uhľovodíkové reťazce vo svojich R R alebo postranných reťazcoch, sú bežne známe v bibliografii ako rozvetvené alebo rozvetvené aminokyseliny reťazca. V tejto skupine sú valín, fenylalanín, leucín a izoleucín.
Všeobecne sa aminokyseliny tejto skupiny používajú ako vnútorné štrukturálne prvky v syntéze proteínov, pretože tieto môžu byť spojené navzájom prostredníctvom hydrofóbnych interakcií, „utekajú“ z vody a stanovujú charakteristické štrukturálne skladanie mnohých proteínov.
Jeho molekulová hmotnosť je okolo 117 g/mol a keďže jeho skupina R alebo bočné reťazce je rozvetvený uhľovodík, nemá žiadne zaťaženie a jeho relatívny počet v proteínových štruktúrach je o niečo väčší ako 6%.
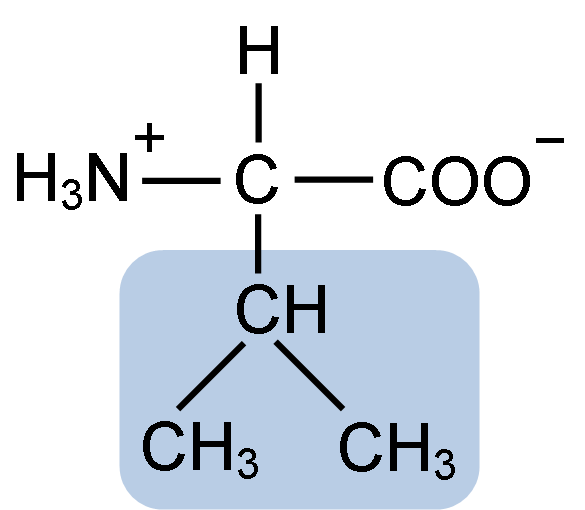
Štruktúra
La Valina zdieľa všeobecnú štruktúru a tri typické chemické skupiny všetkých aminokyselín: karboxylová skupina (COOH), aminoskupina (NH2) a atóm vodíka (-H). Vo svojej skupine R alebo bočného reťazca má tri atómy uhlíka, ktoré mu dodávajú veľmi hydrofóbne vlastnosti.
Môže vám slúžiť: Inertné bytosti: Charakteristiky, príklady, rozdiely so živými bytosťamiAko platí pre všetky chemické zlúčeniny klasifikované ako „aminokyseliny“, valín má centrálny atóm uhlíka, ktorý je chirálny a ktorý je známy ako α uhlík, do ktorého spomenuté štyri chemické skupiny.
Názov IUPAC Valine je 2-3-amino-3-butanóic.
Všetky aminokyseliny sa nachádzajú vo forme D alebo L a valín nie je výnimkou. Forma L-hodnoty je však oveľa hojnejšia ako forma D-Vallein a navyše je spektroskopicky aktívnejšia ako forma D.
L-hodnota je forma použitá na tvorbu bunkových proteínov, a preto je z týchto dvoch biologicky aktívnej formy. Plní funkcie, ako je nutraceutický, mikronutrient pre rastliny, metabolit pre ľudí, riasy, kvasinky a baktérie, medzi mnohými ďalšími funkciami.
Funkcia
Valina, napriek tomu, že je jednou z deviatich esenciálnych aminokyselín, nehrá ďalšiu úlohu pri účasti na syntéze proteínov a ako metabolit na svojej vlastnej degradačnej ceste.
Objemné aminokyseliny, ako je valín a tyrozín Bombyx mori, bežne známe ako červy z hodvábu alebo moruše.
Tkanivá, ako sú arteriálne väzy a okuliare, sa skladajú z vláknitého proteínu známeho ako elastín. Skladá sa z polypeptidových reťazcov s opakovanými sekvenciami glycínu, alanínu a valínových aminokyselín, najdôležitejšieho zvyšku s proteínom.
Valina sa podieľa na hlavných syntéznych trasách zlúčenín zodpovedných za charakteristickú vôňu ovocia. Molekuly Valina sa transformujú na metylované a rozvetvené deriváty esterov a alkoholov.
V potravinárskom priemysle
Existuje veľa chemických prísad, ktoré používajú valín v kombinácii s glukózou na získanie chutných pachy v určitých kulinárskych prípravkoch.
Pri teplote 100 ° C majú tieto prísady charakteristickú vôňu raže a viac ako 170 ° C v horúcej čokoláde, takže sú populárne pri výrobe potravín v pekárskom a pečivom (pečivo).
Tieto chemické prísady používajú umelo syntetizované L-Valin.
Biosyntéza
Všetky aminokyseliny rozvetveného reťazca, ako je valín, leucín a izoleucín, sa syntetizujú hlavne v rastlinách a baktériách. Čo znamená, že zvieratá, ako je ľudská bytosť a iné cicavce.
Zvyčajne biosyntéza valínu začína prenosom dvoch atómov uhlíka z hydroxyetyl -teamínového pyrofosfátu do pyruvátu pôsobením enzýmu ocetohydroxi -izomérnej kyseliny kyseliny kyseliny kyseliny reduktázy kyseliny.
Dva atómy uhlíka pochádzajú z druhej pyruvátovej molekuly prostredníctvom reakcie závislej od TPP veľmi podobnú atmosfére katalyzovanej enzýmom Discarboxylázou pyruvát, ale ktorá je katalyzovaná dihydroxy-kyselinou dehydratázou dehydratázy.
Enzýmová valina aminotransferáza, konečne obsahuje aminoskupinu do ketoacidovej zlúčeniny, ktorá je výsledkom prednej dekarboxylácie, ktorá tvorí L-valin. Aminokyseliny leucínu, izoleucínu a valínu majú veľkú štrukturálnu podobnosť, a to preto, že mnohí sprostredkovatelia a enzýmy zdieľajú na svojich biosyntetických trasách.
Môže vám slúžiť: Flora a fauna de salta: Reprezentatívnejšie druhyKetoacid produkovaný počas biosyntézy L-valínu reguluje niektoré enzymatické kroky negatívnou spätnou väzbou alebo volarickou reguláciou na biosyntetickej ceste leucínu a iných príbuzných aminokyselín.
To znamená, že biosyntetické trasy sú inhibované metabolitom generovaným v nich, ktorý pri akumulácii poskytuje bunkám špecifický signál, ktorý im hovorí, že určitá aminokyselina je nadmerne, a preto jej syntéza môže zastaviť.
Degradácia
Prvé tri kroky degradácie valínu sú zdieľané na trase degradácie všetkých aminokyselín rozvetveného reťazca.
Valina môže vstúpiť do cyklu kyseliny citrónovej Krebs, ktorá sa má transformovať na sukcinyl-coA. Degradačná cesta pozostáva z počiatočnej transaminácie, katalyzovanej enzýmom známym ako aminotransferáza aminokyselín rozvetveného reťazca (BCAT).
Tento enzým katalyzuje reverzibilnú transamináciu, ktorá dokáže previesť aminokyseliny rozvetveného reťazca na ich zodpovedajúci vetvený reťazec a-Zo-stonát.
V tejto reakcii je nevyhnutná účasť momentu glutamátu/2-zotoglutarátu, pretože 2-zotoglutarát prijíma aminoskupinu, ktorá je odstránená z aminokyseliny, ktorá sa metabolizuje a stáva glutamátom.
Tento prvý reakčný krok katabolizmu valínu produkuje 2-cethoizvalerát a je sprevádzaný konverziou pyridoxálneho 5'-fosfátu (PLP) v pyridoxamíne 5'-fosfátu (PMP).
Potom sa 2-cethoisvalerát používa ako substrát mitochondriálneho enzymatického komplexu, známy ako a-a-z-zo-stíhanie rozvetveného reťazca, ktorý pridáva časť COASH a tvorí izobutiril-coA, ktorý je následne dehydrogenovaný a zmenený na metatakrílil -Coa.
Metakrylil-CoA sa spracováva po prúde v 5 ďalších enzymatických krokoch, ktoré zahŕňajú hydratáciu, elimináciu koasovej časti, oxidáciu, pridanie inej časti koasla a molekulárna reorganizácia, ktorá končí produkciou sukcinyl-CoA, ktorá okamžite vstupuje do cyklu Krebsov.
Potraviny bohaté na Valinu
Proteíny obsiahnuté v sezame alebo sezamových semenách sú bohaté na Valinu, s takmer 60 mg aminokyseliny pre každý gram proteínu. Z tohto dôvodu sa pre deti s nedostatočnou stravou tejto aminokyseliny odporúčajú súbory cookies, sušienok a sezamové tyčinky alebo nugat.
Sójové zrná sú vo všeobecnosti bohaté na všetky esenciálne aminokyseliny, dokonca aj v Valine. Sú však chudobní v metrií a cysteine. Proteín alebo sójová štruktúra má veľmi zložité kvartérne štruktúry, ale ktoré sa ľahko rozpustia a oddeľujú na menšie podjednotky v prítomnosti žalúdočných štiav.
Casein, ktorý je zvyčajne v mlieku a jeho derivátoch, je bohatý na opakované sekvencie Valiny. Rovnako ako sójové bôby, aj tento proteín sa ľahko degraduje a absorbuje v črevnom trakte cicavcov.
Odhaduje sa, že na každých 100 gramov sójového proteínu sa požije asi 4,9 gramov valínu; Zatiaľ čo za každých 100 ml mlieka, požíva sa asi 4,6 ml Valina.
Ďalšie potraviny bohaté na uvedenú aminokyselinu sú hovädzie mäso, ryby a rôzne druhy zeleniny a zeleniny.
Výhody vášho príjmu
Valín, podobne ako veľká časť aminokyselín, je glykogénna aminokyselina, to znamená, že sa môže začleniť do glukoneogénnej cesty a mnohí neurológovia potvrdzujú, že ich príjem pomáha udržiavať duševné zdravie, svalovú koordináciu a znižovať stres.
Môže vám slúžiť: 5 vetiev hlavnej biotechnológieMnoho športovcov konzumuje komprimované komprimované vo Valine, pretože pomáhajú regenerácii tkanív, najmä svalových tkanív. Byť aminokyselinou schopnou spájať glukoneogenézu pomáha produkcii energie, čo je nielen dôležité pre fyzickú aktivitu, ale aj pre nervové fungovanie.
Potraviny Valina pomáhajú udržiavať rovnováhu dusíkových zlúčenín v tele. Táto rovnováha je nevyhnutná pre tvorbu energie z požitých proteínov, pre rast tela a hojenie.
Jeho spotreba zabraňuje poškodeniu pečene a žlčníka a prispieva k optimalizácii mnohých telesných funkcií.
Jedným z najpopulárnejších doplnkov výživy medzi športovcami na zvýšenie objemu svalov a regenerácie svalov je BCAA.
Tieto typy tabliet pozostávajú z tabliet so zmesami rôznych aminokyselín, medzi ktorými sa všeobecne zahŕňajú aminokyseliny, ako je L-Valin, L-izoleucín a L-Leucina; Sú tiež bohatí na vitamín B12 a ďalšie vitamíny.
Niektoré experimenty s ošípanými ukázali, že požiadavky na valín sú oveľa vyššie a obmedzujúce pre matky počas fázy dojčenia, pretože táto aminokyselina pomáha vylučovať mlieko a vytvára zlepšenie rýchlosti rastu detských novorodencov.
Poruchy nedostatku
Denný príjem valínu odporúčaný pre dojčatá je okolo 35 mg pre každý konzumovaný gram bielkovín, zatiaľ čo u dospelých je množstvo o niečo nižšie (okolo 13 mg).
Najbežnejšie ochorenie súvisiace s aminokyselinami valínu a iných rozvetvených reťazcov je známe ako „choroba moču so sirupom arce“ alebo „ketoacidúria“.
Toto je dedičný stav spôsobený defektom v génoch, ktoré kódujú dehydrogénne enzýmy a-zocidov odvodených od leucínu, izoleucínu a valínu, ktoré sú potrebné na ich metabolizáciu.
Pri tejto chorobe organizmus nemôže asimilovať žiadnu z týchto troch aminokyselín, keď sa získajú z diéty, a preto sa odvodené ketoacidy hromadia a sú vylúčené v moči (môžu sa tiež detegovať v krvnom sére a v mozgovomiechovom múdrosti).
Na druhej strane zlá strava vo Valine súvisí s neurologickými patológiami, ako je epilepsia. Môže tiež spôsobiť chudnutie, Huntingtonovu chorobu a môže dokonca skončiť vo vývoji určitých typov rakoviny, pretože systém opravy tkanív a syntéza biomolekúl sú ohrozené.
Odkazy
- Abu-Baker, s. (2015). Preskúmanie biochémie: Koncepty a spojenia
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger princípy biochémie. Macmillan.
- Plimmer, R. H. Do., & Phillips, h. (1924). Analýza proteínov. Iii. Odhad histidínu a tyrozínu bomináciou. Biochemical Journal, 18 (2), 312
- Plimmer, R. H. Do. (1912). Chemická konštitúcia proteínov (zv. 1). Longmans, zelený.
- Torii, K. Do. Z. Alebo. Ani., & Iitaka a. (1970). Kryštalická štruktúra L-valínu. Crystallographica Section B: Štrukturálna kryštalografia a kryštálová chémia, 26 (9), 1317-1326.
- Tosti, v., Bertozzi, b., & Fontana, L. (2017). Zdravotné prínosy stredomorskej stravy: Metabolické a molekulárne mechanizmy. Časopisy Gerontology: Series A, 73 (3), 318-326.

