Transformácia hmoty
- 3584
- 57
- Alan Milota
 Transformácie hmoty sú tie transformácie, ktoré trpia bez zmeny jej zloženia. Napríklad voda vo svojej tekutine, tuhej (ľadovej) alebo sóde (para) zostáva vodou
Transformácie hmoty sú tie transformácie, ktoré trpia bez zmeny jej zloženia. Napríklad voda vo svojej tekutine, tuhej (ľadovej) alebo sóde (para) zostáva vodou Aké sú transformácie hmoty?
Transformácie hmoty sú zmeny, ktoré trpia bez zmeny jej zloženia. To znamená, že hmota sa transformuje, keď prechádza fyzikálnymi a chemickými zmenami.
Príkladmi fyzikálnych zmien je tvorba ľadu, keď teplota klesá, rosa na listoch, ktoré sa objavujú v dopoludňajších hodinách, dilatácia predmetov pri zahrievaní a magnetizácia tela.
Oxidácia skrutiek a nechtov je chemická zmena, pretože oxid je látka iná ako pôvodné železo. V každom prípade sú potrebné zmeny energie, aby sa tieto transformácie uskutočnili.
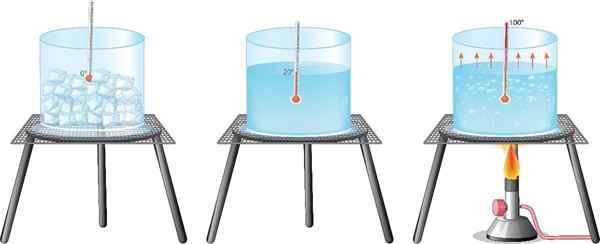
Transformácia ľadu je zmena stavu, v ktorom voda stuhne, ale existuje viac možností. Matho sa vyskytuje v prírode a v laboratóriu v rôznych štátoch, z ktorých plyn, tekutina a tuhá látka sú tri najbežnejšie, prinajmenšom za pozemských podmienok.
Ale keďže sa záležitosť mení, vedci sa stretli s viacerými štátmi trochu exotickou povahou, experimentálnou a teoretickou základňou.
Možno potvrdiť, že existuje päť základných stavov hmoty:
- Tuhý
- Tekutý
- Plyn
- Plazma
- Kondenzát Bose-Einstein
Z nich sú prvé tri stabilné v podmienkach našej planéty, zatiaľ čo posledné dva vyžadujú technologické prostriedky, hoci vo vesmíre sú časté. Plazma je v skutočnosti najbežnejším stavom hmoty vo vesmíre.
Základné štáty hmoty
Za tlakových a teplotných podmienok Zeme je hmota obvykle prezentovaná v troch štátoch: tuhá látka, tekutina a plyn, zatiaľ čo stavy plazmy a kondenzátu bose-einsteínu sa získavajú v rôznych podmienkach, ktoré sa dajú dosiahnuť v laboratóriu.
Môže vám slúžiť: nekonvenčné opatreniaAby som vysvetlil, prečo je potrebné pamätať na to, že hmota sa skladá z častíc, prepojených prostredníctvom síl, atraktívnych aj odporných. Príťažlivé sily, ako už názov napovedá, majú tendenciu zostaviť častice, zatiaľ čo odpudivé majú opačný účinok.
Pevné látky, kvapaliny a plyny
Ak prevládajú sily príťažlivosti medzi časticami, zostávajú blízko seba, spolu vo viac alebo menej pevných pozíciách, čo vedie k vzniku tuhá látka. Častice môžu vibrovať, ale nie opustiť svoju polohu v pevnej látke, preto to zachováva definovaný tvar a objem.
V Kvapalina, Príťažlivé sily umožňujú časticiam pokračovať v blízkosti, ale sú menej intenzívne ako v tuhých látkach tým, že im poskytujú možnosť „navzájom sa„ skĺznuť “určitým spôsobom. Z tohto dôvodu tekutiny prispôsobujú svoj tvar nádobe, ktorá ich obsahuje, ale udržiavajte svoj pevný objem.
Nakoniec v Plyny, Atraktívne sily sú ešte slabšie, prevažne odporné sily. Vďaka tomu sú častice navzájom dobre preč a s oveľa väčšou slobodou pohybu. Z tohto dôvodu sa plyny rozširujú, kým objem dostupný úplne nezaberá.
Kondenzát a kondenzát Bose-Einstein
Dostatočne zahrievaním plynu, iónov a elektrónov sa v procese nazývané ionizácia, Takto a plazma v laboratóriu. Plazmový stav nie je ľahké prirodzene vidieť blízko Zeme, ale z neho ho možno vidieť v severných a južných svetlách.
Tento krásny prírodný fenomén sa vyskytuje, keď častice slnečného vetra, dosť rozptýlená plazma, ovplyvňujú atmosféru Zeme, ionizujú.
Na druhom konci stupnice, chladenie veľa, tesne nad absolútnou nulou, sa objaví nový stav hmoty, v ktorom je väčšina častíc v základnom stave, ktorý je najnižšou energiou.
Môže vám slúžiť: najdôležitejší aspekt malej vedy, veľkej vedy a technofienkyTento stav hmoty sa volá Kondenzát Bose-Einstein, fyzikmi Satyendra Bose a Albert Einstein, ktorí predpovedali svoju existenciu v roku 1924.
O mnoho rokov neskôr, v roku 1995, sa viacerým vedcom podarilo preniesť veľmi zriedené plyny do tohto štátu, ľahká úloha, vzhľadom na to, že teploty iba nano-kelvinu sú potrebné nad absolútnou nulou.
Zmeny stavu vo veci
V prírode je veľmi bežné, že záležitosť prechádza z jedného štátu do druhého. Normálne sú tieto fyzikálne zmeny spôsobené zmenami tlaku a teploty, odvodené od zvýšenia alebo zníženia energie častíc.
Keď sa do materiálu pridá tepelná energia, zvyšuje sa kinetická energia jeho častíc, čím sa znižuje príťažlivosť, ktorá ich udržuje v súdržnosti. Ak bol materiál v tuhom stave, môže sa potom presunúť do tekutého stavu alebo dokonca ísť priamo do plynného stavu.
Naopak, odstránenie dostatočnej tepelnej energie je možné transformovať plynný materiál na kvapalinu alebo že prechádza z kvapaliny na pevnú látku. V žiadnom prípade sa zloženie látky nemení.
Najznámejším príkladom pre všetkých je voda: je dobre známe, že časť tekutej vody sa pri varení transformuje do pary, zatiaľ čo jej prechádza na ľad chladenie do mrazničky.
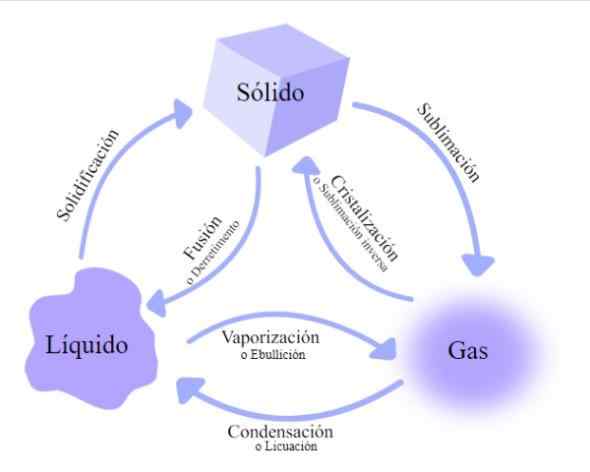 Zmeny v stave hmoty. Zdroj: Wikimedia Commons
Zmeny v stave hmoty. Zdroj: Wikimedia Commons Existuje niekoľko výmenných kurzov, cez ktoré prechádza hmota, klasifikovaná podľa toho, či sa tepelná energia zvyšuje alebo klesá:
- Progresívny, Uskutočňujú sa, keď materiál absorbuje tepelnú energiu.
- Regresívny, Sú tí, ktorí sa vyskytujú, keď materiál poskytne energiu.
Progresívne transformácie
Medzi rôzne progresívne transformácie, ktoré sa odohrávajú v veci pridaním energie, patria:
Fúzia
Zmena, ku ktorej dochádza, keď materiál prechádza z jeho tuhej fázy do jej kvapalnej fázy. Napríklad tavením ľadového bloku alebo zahrievania alebo vosku na panvici.
Odparovanie
V tomto prípade sa záležitosť transformuje tekutým stavom do plynného stavu.
Môže vám slúžiť: metodikaOdparovanie sa vyskytuje dvoma spôsobmi:
- Vriaci, sa uskutoční, keď materiál dosiahne svoj teplota varu, Týmto spôsobom stačí energia na prekonanie intermolekulárnych síl, ktoré udržiavajú častice v ich kvapalnom stave. Každá látka má charakteristickú teplotu varu pri určitom tlaku.
- Odparovanie, Menia iba povrchové častice, pretože materiál nie je pri teplote potrebnej na vstup do varu. Najznámejším príkladom je odparovanie vody, ktorá zostala v nádobe, pri teplote miestnosti.
Plesanie
Volali tiež sublimácia, Uskutočňuje sa, keď materiál prevedie priamo z plynovej pevnej látky bez toho, aby prešiel kvapalnou fázou.
Napríklad suchý ľad je oxid uhličitý2 zosunuté pri izbovej teplote. Naftalén, ktorý sa používa na ochranu odevov hmyzu, pomaly prechádza z pevnosti k plynu.
Ionizácia
Je to priechod plazmového plynu.
Regresívne transformácie
Sú transformácie spôsobené poklesom tepelnej energie častíc. Medzi nimi sú:
Tulifikácia
Je to zmena hmoty z tekutého stavu na pevnú látku ochladením, ako sa to stáva pri umiestňovaní vody do mrazničky. Proces je preto, že látka poskytuje energiu do chladného prostredia a tvorí ľad.
Kondenzácia
Vyskytuje sa pri prechode z plynného stavu do kvapalnej fázy, rovnako ako pri vodnej pary vo vzduchu, pri kontakte so studeným povrchom čelného skla automobilu.
Skvapalnenie
Je to transformácia hmoty pri prechode z plynu na kvapalinu, ako sa to stane, chladenie amoniaku alebo vysokotlakového oxidu uhličitého.
Inverzná sublimácia
Toto je priechod hmoty v plynnom až tuhom stave, rovnako ako v prípade plynného jódu, ktorý sa stretáva s chladným povrchom, čo vedie k tvorbe tuhých kryštálov. Je tiež známy ako kryštalizácia.
Sprevádzanie
Zmena plazmového stavu na plynný stav.
Odkazy
- Chang, R. (2013). Chémia. 11 VA. Vydanie. McGraw Hill Education.
- Giancoli, D. (2006 =. Fyzika: Princípy s aplikáciami. 6. Ed Prentice Hall.
- Hmota a jej vlastnosti. Získané z: elbibliote.com.
- Opentax. Chémia. Zdroj: Openstax.orgán.
- Shipman, J. (2009). Úvod do fyzickej vedy. Dvanáste vydanie. Brooks/Cole, edície Cengage.

