Transaminácia
- 4613
- 8
- MUDr. Miloslav Habšuda
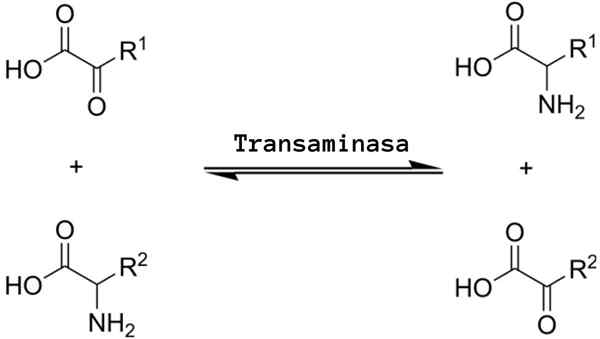 Schéma aminotransferenčnej reakcie medzi aminokyselinou a alfa-zoacidou (zdroj: Alcibiades prostredníctvom Wikimedia Commons)
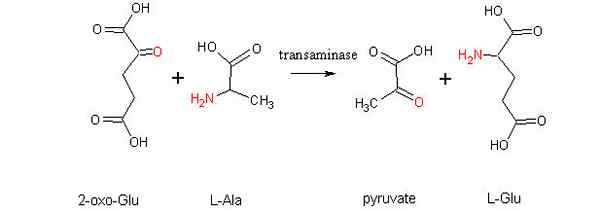
Schéma aminotransferenčnej reakcie medzi aminokyselinou a alfa-zoacidou (zdroj: Alcibiades prostredníctvom Wikimedia Commons) Čo je transaminácia?
Ten transaminácia Je to typ chemickej reakcie, ktorá funguje v „redistribúcii“ skupín aminokyselín, pretože obklopuje reverzibilné procesy aminácie (pridanie aminoskupiny) a srdcového zlomu (eliminácia aminoskupiny), ktoré sú katalyzované špecifickými enzýmami známe ako transaminázy alebo aminotransferázy.
Všeobecná transaminačná reakcia znamená výmenu medzi aminokyselinou a akýmkoľvek a-Zo-skladom, kde výmena aminoskupiny poskytuje ketoacidovú verziu prvej substrátovej aminokyseliny a aminokyselinová verzia prvého a-zo-enkoacidového substrátu substrátu.
Aminoskupina, ktorá sa zvyčajne vymieňa, je amino „alfa“, to znamená, že sa podieľa na tvorbe peptidových väzieb a definuje štruktúru aminokyselín, hoci reakcie, ktoré zahŕňajú ďalšie aminoskupiny prítomné v rôznych pozíciách v rôznych pozíciách v rôznych pozíciách V rôznych pozíciách sa môžu vyskytnúť v.
S výnimkou lyzínu, treonínu, prolínu a hydroxyprolínu sa všetky aminokyseliny zúčastňujú na transaminačných reakciách, hoci pre histidín, serín, metóda a fenylalanín boli opísané transaminázy, ale ich metabolické trasy neznamená tento typ reakcií tento typ reakcií.
Transaminačné reakcie medzi aminokyselinami a a-cethoacidmi objavili v roku 1937 Braunstein a Kritzmann a odvtedy boli predmetom intenzívnych štúdií, pretože sa vyskytujú v mnohých tkaninách rôznych organizmov a s rôznymi účelmi.
Napríklad u ľudí sú transaminázy široko distribuované v telesných tkanivách a sú obzvlášť aktívne v tkanive srdcového svalu, v pečeni, v tkanive kostrových svalov a v obličkách.
Mechanizmus reakcie
Transaminačné reakcie naznačujú viac -menej rovnaký mechanizmus. Ako je uvedené vyššie, tieto reakcie sa vyskytujú ako reverzibilná výmena aminokyseliny medzi aminokyselinou a a-zo-cid.
Môže vám slúžiť: keramické materiály: charakteristiky, typy, príkladyTieto reakcie závisia od zlúčeniny známeho ako fosfátový pyridoxálny, derivát vitamínu B6, ktorý sa zúčastňuje ako transportér aminoskupinovej skupiny a viaže sa na transaminázové enzýmy tvorbou Schiffovej bázy medzi skupinou aldehydovej skupiny tejto molekuly a e-amino lyzín zvyšok na aktívnom mieste enzýmu.
Spoja medzi fosfátovým pyridoxálnym a lyzínovým zvyškom na aktívnom mieste nie je kovalentný, ale je podávaný elektrostatickou interakciou medzi pozitívnou záťažou dusíka v lyzínu a negatívnou zaťažením vo fosfátovej skupine pyridoxal.
V priebehu reakcie aminokyselina, ktorá funguje ako substrát.
Medzitým sa dvojica aminokyselinových alfa uhlíkových elektrónov odstraňuje a prenesie do pyridínového kruhu, ktorý tvorí fosfát pyridoxal (s kladným nábojom) a potom sa „dodávajú“ do a-Zo-ZID, ktorý funguje ako druhý substrát.
Týmto spôsobom sa pyridoxálny fosfát nezúčastňuje nielen na prenos alebo transport aminokyselín medzi aminokyselinami a a-ekotocidami, ktoré sú substrátom transamináz, ale tiež pôsobia ako „umývadlo“ elektrónov, uľahčujúce disociáciu disociácie vodík kyseliny Alfa.
Stručne povedané, prvý substrát, aminokyselina, prenáša svoju aminoskupinu do fosfátového pyridoxálu, odkiaľ sa následne prenesie na druhý substrát, a-zo-ekotoid, ktorý sa vytvára v medziprodukte, medzipomáda známa ako pyridoxamín fosfát.
Môže vám slúžiť: stĺpková chromatografiaTransaminačná funkcia
Transaminázové enzýmy sa všeobecne vyskytujú v cytosóle a mitochondriách a pracujú na integrácii rôznych metabolických trás.
Napríklad glutamát dehydrogenáza v jeho inverznej reakcii môže zmeniť glutamát na amónny, NADH (alebo NADPH) a a-zetoglutarát, ktorý môže vstúpiť do cyklu trikarboxylových kyselín a fungovať pri výrobe energie.
Tento enzým, ktorý je v mitochondriálnej matrici, predstavuje pobočkový bod, ktorý spája aminokyseliny s energetickým metabolizmom, takže keď bunka chýba dostatočná energia vo forme uhľohydrátov alebo tukov, môže to striedavo používať niektoré aminokyseliny pre rovnaké kyseliny účel.
Tvorba enzýmu (glutamát dehydrogenáza) počas vývoja mozgu je nevyhnutná pre kontrolu detoxikácie amónneho, pretože sa ukázalo, že niektoré prípady mentálnej retardácie sa týkajú nízkej aktivity, čo vedie k akumulácii amoniak, čo škodí zdraviu mozgu.
V niektorých pečeňových bunkách sa môžu transaminačné reakcie použiť aj na syntézu glukoneogenézy glukózy.
Glutamín sa premieňa na glutamát a amónny pomocou glutaminázového enzýmu. Potom sa glutamát prevedie na a-zetoglutarát, ktorý vstupuje do cyklu Krebs a potom na glukoneogenézu. Tento posledný krok sa vyskytuje vďaka Malo, jedným z výrobkov na trase, sa prepravuje mimo mitochondrií pomocou raketoplánu.
Tento raketoplán zanecháva a-cethoglutarát na milosrdenstvo enzýmu malica, čo ho robí pyruvátmi. Dve pyruvátové molekuly sa môžu previesť, potom glukózová molekula glukoneogenézou.
Môže vám slúžiť: Flaka na pozadíPríklady
Najbežnejšie transaminačné reakcie súvisia s alanínovými aminokyselinami, kyselinou glutámou a kyselinou asfartárovou.
Niektoré enzýmy aminotransferázy môžu okrem pyridoxálneho fosfátu používať pyruvát ako „koenzým“, ako je to v prípade transaminázy glutamátového piruvátu, ktorý katalyzuje nasledujúcu reakciu:
glutamát + pyruvát ↔ alanín + a-ceglutarát
Svalové bunky závisia od tejto reakcie na výrobu alanínu z pyruvátu a na získanie energie prostredníctvom cyklu Krebs pomocou a-zetoglutorát. V týchto bunkách použitie alanínu ako zdroja energie závisí od eliminácie aminoskupín ako amónnych iónov v pečeni, cez cyklus močoviny.
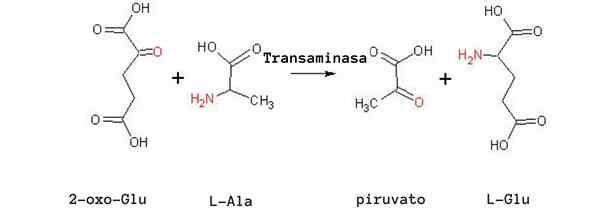 Transaminačná reakcia alanínu (zdroj: Tomas Drab [verejná doména] cez Wikimedia Commons)
Transaminačná reakcia alanínu (zdroj: Tomas Drab [verejná doména] cez Wikimedia Commons) Ďalšou veľmi dôležitou transaminačnou reakciou u rôznych druhov je katalyzovaná enzýmovou aspartátovou aminotransferázou:
L-sparto + a-ketoglutarát ↔ oxalacetát + L-glutamát
Nakoniec, ale v neposlednom rade, transaminačná reakcia kyseliny y-aminomaslovej (GABA), neproteínová aminokyselina pre centrálny nervový systém, ktorý funguje ako inhibičný neurotransmiter. Reakcia je katalyzovaná y-aminobutirickou transaminázovou kyselinou a je viac-menej nasledovná:
α-ketoglutarát + kyselina 4-aminobutánová ↔ glutamát + semi-aucar Succinic
Succinic Semi -Polmi -použitie sa konvertuje na kyselinu subpinovú oxidačnou reakciou a posledne menovaný môže vstúpiť do Krebsovho cyklu na výrobu energie.

