Torio štruktúra, vlastnosti, získanie, použitia

- 2368
- 427
- Alan Milota
On Torio Je to kovový prvok, ktorý patrí do série aktinidov, takzvaných vzácnych zemín a ktorých chemický symbol je th. Má atómový počet 90 a atómovú hmotnosť 232 g/mol. Torio zlúčeniny ho zvyčajne obsahujú s oxidačným číslom +4 (th4+).
Zlúčenina oxidu torio, tho2, Je známa priemyselne ako Toria a používa sa vo väčšine aplikácií Torium, ktoré sa vyznačuje chemickou zlúčeninou s najväčším bodom topenia (3.300 ° C).
 Vzorka kovového tória uložená v sklenenom pľuzgieri pod argónom. Jeho načervený povlak je spôsobený jeho oxidom. Zdroj: Alchymist-HP (Talk) (www.PSE-Mendelejew.de) / fal
Vzorka kovového tória uložená v sklenenom pľuzgieri pod argónom. Jeho načervený povlak je spôsobený jeho oxidom. Zdroj: Alchymist-HP (Talk) (www.PSE-Mendelejew.de) / fal Torio objavil v roku 1828 Mortar Thrane Esmark, ktorý našiel na nórskom ostrove Løvøya čierny minerál. Esark vydal minerál Jönsovi Jacobovi Berzeliusovi, ktorý ho analyzoval, že v ňom nájde neznámy kov.
Na počesť škandinávskeho boha Thora nazval čierny minerál ako Torita (Thorita). Medzitým sa neznámy kov nazýval Torio (thorium). Rádioaktívny charakter tória založil Anton Edward Van Arkel a Jan Hendrik de Boer a nezávisle Pierre Curie a Marie Curie.
[TOC]
Vlastnosti Torium
Fyzický
Tórium je rádioaktívne, svetlé, mierne tvrdé, strieborné, ťažisko a poddajný biely kov, ktorý vo vzduchu hmla veľmi pomaly, so sivou a neskôr čiernou farbou. Patrí do skupiny aktinidov, identifikuje sa s atómovým číslom 90 a atómovou hmotnosťou 232 g/mol.
Rádioaktivita
Torio-232 (232Th90) predstavuje viac ako 99% celkového prvku tória prítomných v zemskej kôre. Dá sa uvažovať o tom, že ide o stabilný izotop, napriek tomu, že je rádioaktívny, pretože jeho polovičný život je 1.405 x 1010 roky. Rádioaktívne klesá emisiou a a p častíc a y žiarenie.
Torio-232 sa transformuje na rádio-268 (268Rana88) vydaním alfa častíc vytvorenej dvoma protónmi a dvoma neutrónmi. Tórium môže trpieť sériou rádioaktívnych dezintegrácií, kým sa nestane stabilným prvkom: olovo-208.
Môže vám slúžiť: chlorid olovom: vlastnosti, štruktúra, použitieTorio-232 je schopný zachytiť neutróny, aby sa transformoval na rádioaktívny prvok uránu-233 a emitoval β typu žiarenie. Urán sa na druhej strane používa v jadrových reaktoroch na výrobu energie.
Reaktivita
Tórium je elektropozitívny a vysoko reaktívny kov. Oxiduje veľmi pomaly vo vzduchu, hoci korózia sa môže vyskytnúť po niekoľkých mesiacoch. Keď sa zahrieva vo vzduchu, zapne sa a emituje jasne biele svetlo, zatiaľ čo výroba oxidu Torio, tho2.
Pri štandardných podmienkach teploty a tlaku je tória pomaly napadnutá vodou. Podobne sa tória nerozpustí v najbežnejších kyselinách, s výnimkou kyseliny chlorovodíkovej, kde sa rozpúšťa, zanecháva čierny, nerozpustný zvyšok.
Rozpúšťa sa tiež v koncentrovanej kyseline dusičnej s malým množstvom katalytického alebo fluorosylikačného fluoridu. Thorium je pyroforický kov: keď sa stane práškom, je schopný spontánne zapáliť.
Štruktúra
Torio atómy tvoria kryštál kubickej štruktúry sústredený na tváre (FCC) pri teplote miestnosti. Keď sa zahrieva nad 1360 ° C, sklo utrpí prechod do kubickej fázy zameranej na telo (BCC), s nižšou hustotou. Medzitým tória pri vysokých tlakoch (100 GPA alebo viac) získava hustú tetragonálnu štruktúru sústredenú na tele (BCT).
Elektronická konfigurácia
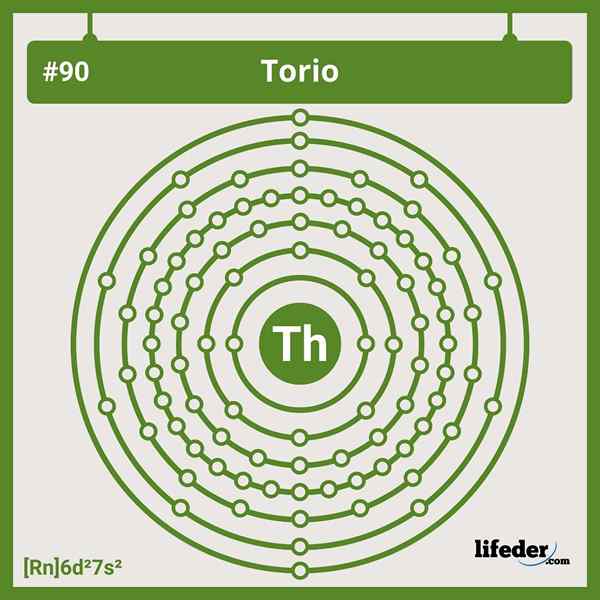 Elektronické nastavenia Torium
Elektronické nastavenia Torium Skrátená elektronická konfigurácia tória je nasledovná:
[Rn] 6d2 7s2
Strata štyroch elektrónov vo Valencii sa transformuje na katión4+. Všimnite si, že napriek tomu, že pôsobí, chýba mu elektróny na svojich orbitáloch 5F, na rozdiel od ostatných aktinidov.
Môže vám slúžiť: dispergingová fázaZískanie
Hlavným minerálom používaným na získanie tória je monacita. Počiatočný krok je jeho oddelenie od primárneho ložiska: Pegmatita. Alkalinoterrózne kovy uhličitany sú eliminované z pegmatitu reakciou ich fragmentov chloridom vodíka.
Výsledné fragmenty sú kalcinované a filtrované a potom podstupujú magnetickú separáciu. Získa sa teda piesočný materiál monacity. Tento piesok je podrobený 93%tráveniu kyseliny sírovej, pri teplote 210 až 230 ° C a niekoľko hodín. Vytvorený kyslý roztok sa neskôr zriedi vodou desaťkrát jej objem.
Monacita zostáva potápanie na dno, zatiaľ čo tória a ďalšie prvky vzácnej Zeme plávajú v príprave kyseliny. PH do 1 je upravený.3, ktoré vytvára zrážky tória ako fosfátu, zatiaľ čo zvyšok zriedkavej pôdy v suspenzii zostáva v roztoku.
V súčasnosti sa separácia a čistenie vykonáva pomocou kvapalných rozpúšťadiel, napríklad fosforečnanu Tribute v Querosenu.
Torio Metal sa môže vyskytnúť v komerčných množstvách metalotermálnym znížením totrafluoruro de torio (thf4) a oxid torio (this tho2) alebo elektrolýzou tetrachloridu tória (thcl4).
Žiadosti
Tórium malo veľa aplikácií, z ktorých mnohé boli odhodené od 50. rokov 20. storočia, pretože jeho rádioaktívny charakter predstavoval zdravotné riziko.
Priemyselný pracovník
Zliatiny
Tórium bolo legované volfrámom ako elektróda pri zváraní TIG (volfrámový inertný plyn), ktorý predstavuje 2% zliatiny.
V malom množstve sa Torio pridal do volfrámových vlákien, aby sa znížila jeho kryštalizácia, čo umožňuje emisii elektrónov znížiť teploty. Drôty z volfrámu-torio sa používajú v elektronických skúmavkách a v elektródach röntgenových a usmerňovacích skúmaviek.
Oxid torio sa používa pri zváraní volfrámového oblúka, pretože volfrámový odpor voči vysokým teplotám kovových elektród sa zvyšuje. V tejto žiadosti ho však nahradil oxidy obvodov, cerio alebo Lantano.
Môže vám slúžiť: Odkiaľ pochádza plast? HistóriaBlesk
Na druhej strane totrafluoruro de torio sa používa ako materiál na zníženie reflexov v optických povlakoch multicapa, ktoré sú priehľadné pre svetlo s vlnovou dĺžkou medzi 0.350 až 1.2 µm. Torio soľ však v tomto použití nahradila Tetrafluoruro de Lantano.
Oxid torio sa používa pri osvetlení svetla na vyžarovanie brilantného svetla zodpovedajúceho viditeľnému svetlu. Aj keď sa v tejto aplikácii stále používa tória, čiastočne ho nahradilo ITE.
Refraktérny materiál
Tórium sa používa aj pri vypracovaní žiaruvzdorných materiálov pre metalurgický priemysel a v keramických krízoch na výučbu a výskumné laboratóriá.
Jadrová reaktory
Torio-232 sa používa v jadrových reaktoroch na zachytenie neutrónov pomalého pohybu, pretože to sa transformuje na urán-233. Tento rádioaktívny prvok je fyzicky a používa sa na výrobu energie.
Vývoj jadrových reaktorov založených na Torio-32 bol pomalý a vytvoril prvý reaktor s touto charakteristikou v Indian Point Energy Center, ktorý sa nachádza v Buchanane v USA v roku 1962. Jadrové reaktory Torio-232 nemitujú plutónia, čo z nich robí menej znečisťujúce látky.
Odkazy
- Triasť a Atkins. (2008). Anorganická chémia. (Štvrté vydanie). MC Graw Hill.
- Wikipedia. (2020). Tón. Zdroj: In.Wikipedia.orgán
- Národné centrum pre biotechnologické informácie (2020). Tón. PubChem Comunund Zhrnutie pre CID 23974. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- DR. Doug Stewart. (2020). Fakty o elemente tória. Získané z: Chemicool.com
- Redaktori Enyclopaedia Britannica. (2020). Tón. Získané z: Britannica.com
- Šošovica B.Vložka. (2020). Tón. Získané z: Lentech.com
- Rachel Ross. (1. marca 2017). Fakty o tórii. Zotavené z: Livescience.com
- ADVAMEG. (2020). Tón. Získané z: ChemistryExplaed.com

