Príčiny povrchového napätia, príklady, aplikácie a experimenty

- 4900
- 296
- Alfréd Blaho
Ten povrchové napätie Je to fyzická vlastnosť, že všetky kvapaliny prítomné a vyznačujú sa odporom, že ich povrchy sú proti akémukoľvek zvýšeniu svojej oblasti. Je to rovnaké ako tvrdenie, že tento povrch bude hľadať najmenej možnú oblasť. Tento jav prelína niekoľko chemických konceptov, ako je súdržnosť, adhézia a intermolekulárne sily.
Povrchové napätie je zodpovedné za tvorbu zakrivení povrchu tekutín v rúrkových nádobách (odstupňované valce, stĺpce, testovacie trubice atď.). Môžu to byť konkávne (údolie zakrivené) alebo konvexné (zakrivená kupola). Mnoho fyzikálnych javov možno vysvetliť vzhľadom na zmeny, ktoré utrpeli povrchové napätie tekutiny.
 Sférické formy prijaté vodnými kvapkami na listoch sú čiastočne spôsobené ich povrchovým napätím. Zdroj: Fotografia, ktorú urobil užívateľ Flickr Tanakawho [CC Autor (https: // creativeCommons.Org/licencie/BY/2.0)]
Sférické formy prijaté vodnými kvapkami na listoch sú čiastočne spôsobené ich povrchovým napätím. Zdroj: Fotografia, ktorú urobil užívateľ Flickr Tanakawho [CC Autor (https: // creativeCommons.Org/licencie/BY/2.0)] Jedným z týchto javov je trend, ktorý molekuly kvapalín musia aglomerovať vo forme kvapiek, keď spočívajú na povrchoch, ktoré ich odrazujú. Napríklad voda kvapká, ktorú vidíme nad listami, ju nemôžu zvlhčiť kvôli svojmu kopcu, hydrofóbne povrchu.
Prichádza však čas, keď gravitácia uplatňuje svoju úlohu a kvapka sa vyliala ako vodný stĺp. Podobný fenomén sa vyskytuje v sférických kvapkách ortuti, keď je teplomer rozliaty.
Na druhej strane je napätie povrchovej vody najdôležitejšie zo všetkých, pretože prispieva a organizuje stav mikroskopických telies vo vodnom médiu, ako sú bunky a ich lipidové membrány. Okrem toho je toto napätie zodpovedné za to, že sa voda pomaly odparí, a niektoré hustejšie telá, ktoré sa môžu vznášať na jej povrchu.
[TOC]
Príčiny povrchového napätia
Vysvetlenie javu povrchového napätia je na molekulárnej úrovni. Molekuly kvapaliny navzájom interagujú, takže sú súdržné vo svojich nevyspytateľných pohyboch. Molekula interaguje so svojimi susedmi vedľa a tými, ktorí sú nad alebo pod ňou.
To sa však nestane rovnako ako molekuly povrchu kvapaliny, ktoré sú v kontakte so vzduchom (alebo s iným plynom) alebo s pevnou látkou. Povrchové molekuly nemôžu súdržné s telesami vonkajšieho prostredia.
V dôsledku toho nezažívajú žiadnu silu, ktorá ich priťahuje; Iba dole, od svojich susedov tekutého média. Na pôsobenie proti tejto nerovnováhe sú povrchové molekuly „stlačené“, pretože až potom sa im podarí prekonať silu, ktorá ich tlačí nadol.
Môže vám slúžiť: kremičitan sodný (NA2SIO3): Štruktúra, vlastnosti, použitia, rizikáPotom sa vytvorí povrch tam, kde sú molekuly v napätejšej likvidácii. Ak chce častica preniknúť do kvapaliny, musí najprv prekročiť túto molekulárnu bariéru úmernú povrchovému napätiu uvedenej kvapaliny. To isté platí pre častice, ktorá chce uniknúť do vonkajšieho prostredia z hĺbky kvapaliny.
Preto sa jeho povrch správa, akoby to bol elastický film, ktorý vykazuje odpor voči deformovaniu.
Jednotky
Povrchové napätie je zvyčajne znázornené symbolom y a je vyjadrené v N/M jednotkám, sila podľa dĺžky. Väčšinu času však je vaša jednotka DYN/CM. Jeden sa môže stať druhým prostredníctvom ďalšieho konverzného faktora:
1 dyn/cm = 0,001 n/m
Napätie
Voda je západ a najviac prekvapujúce zo všetkých tekutín. Jeho povrchové napätie, ako aj niekoľko jeho vlastností, majú nezvyčajne vysokú hodnotu: 72 dyn/cm pri teplote miestnosti. Táto hodnota sa môže zvýšiť na 75,64 dyn/cm pri teplote 0 ° C; alebo znížiť na 58,85 ° C, pri teplote 100 ° C.
Tieto pozorovania majú zmysel, ak sa predpokladá, že molekulárna bariéra je napätá ešte viac pri teplotách blízko bodu mrazu alebo „uvoľní“ trochu viac okolo bodu varu.
Voda má po vodíkových mostoch veľké povrchové napätie. Ak sú v tekutine známe, sú ešte viac na povrchu. Molekuly vody sú silne vzájomne prepojené vytvorením dipólových depolo interakcií typu H2Oh.
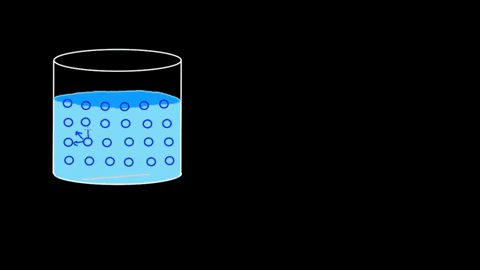 Molekuly vody sa navzájom priťahujú; Sú spojené s vodíkovými mostmi
Molekuly vody sa navzájom priťahujú; Sú spojené s vodíkovými mostmi Účinnosť jej interakcií je taká, že vodná molekulárna bariéra môže dokonca udržať niektoré telá skôr, ako sa potopia. V časti aplikácií a experimentov sa tento bod obnoví.
Ďalšie príklady
Všetky kvapaliny majú povrchové napätie, buď v menšej alebo väčšej miere ako voda, alebo ak ide o čisté látky alebo roztoky. Aké silné a napäté sú molekulárne bariéry ich povrchu, bude závisieť priamo od svojich intermolekulárnych interakcií, okrem štrukturálnych a energetických faktorov.
Kondenzované plyny
Napríklad molekuly plynu v kvapalnom stave interagujú iba navzájom prostredníctvom disperzných síl v Londýne. To súhlasí so skutočnosťou, že ich povrchné napätie má nízke hodnoty:
-Kvapalný hélium, 0,37 dyn/cm a -273 ° C
Môže vám slúžiť: chlorid amónny (NH4CL)-Kvapalný dusík, 8,85 dyn/cm a -196 ° C
-Kvapalný kyslík, 13,2 dyn/cm a -182 ° C
Povrchové napätie kvapalného kyslíka je väčšie ako napätie hélia, pretože jeho molekuly majú väčšiu hmotnosť.
Apolárne kvapaliny
Z apolárnych a organických tekutín sa očakáva, že budú mať vyššie povrchové napätie ako v týchto kondenzovaných plynoch. Medzi niektorými z nich máme nasledujúce:
-Dietileter, 17 dyn/cm pri 20 ° C
-n-Hexano, 18,40 dyn/cm pri 20 ° C
-n-Oktán, 21,80 dyn/cm pri 20 ° C
-Toluene, 27,73 dyn/cm pri 25 ° C
Podobný trend sa pozoruje pre tieto kvapaliny: povrchové napätie sa zvyšuje so zvyšovaním jeho molekulárnych hmôt. Však n-Oktán by mal mať podľa toho najväčšie povrchové napätie a nie toluén. Tu prichádzajú do hry molekulárne štruktúry a geometrie.
Molekuly toluénu, plánu a anillares majú účinnejšie interakcie ako interakcie n-oktán. Preto je povrch toluénu „napätý“ ako povrch n-oktán.
Polárne kvapaliny
Byť silnejším dipólom-dipolom. Ale nie vždy to tak. Medzi niektoré príklady máme:
-Kyselina octová, 27,60 dyn/cm pri 20 ° C
-Acetón, 23,70 dyn/cm pri 20 ° C
-Krv, 55,89 dyn/cm pri 22 ° C
-Etanol, 22,27 dyn/cm pri 20 ° C
-Glycerol, 63 dyn/cm pri 20 ° C
-Chlorid s roztaveným sodným, 163 dyn/cm pri 650 ° C
-Roztok NaCl 6 M, 82,55 dyn/cm pri 20 ° C
Očakáva sa, že chlorid roztaveného sodného bude mať obrovské povrchové napätie: je to viskózna a iónová kvapalina.
Na druhej strane, ortuť je jednou z kvapalín s najvyšším povrchovým napätím: 487 dyn/cm. V ňom je jeho povrch zložený zo silne súdržných atómov ortuti, oveľa viac, ako môžu byť molekuly vody.
Žiadosti
 Niektoré hmyz používajú povrchové napätie vody na ňu. Zdroj: Pixabay.
Niektoré hmyz používajú povrchové napätie vody na ňu. Zdroj: Pixabay. Samotné povrchové napätie chýbajú aplikácie. To však neznamená, že sa nezúčastňuje na niekoľkých denných fenoménoch, že ak by to tak nebolo, nestalo by sa to.
Napríklad komáre a iný hmyz sú schopné prechádzať vodou. Je to preto, že ich hydrofóbne nohy odrazujú vodu, súčasne, keď im ich malá hmota umožní.

Povrchové napätie tiež spĺňa úlohu pri zmáčaní tekutín. Čím väčšie je jeho povrchové napätie, tým menšia je jeho tendencia uniknúť cez póry alebo kurčatá materiálu. Okrem toho sú to málo užitočných tekutín na čistenie povrchov.
Môže vám slúžiť: neutralizačná reakciaDetergenty
Práve tu pôsobia detergenty, znižujú povrchové napätie vody a pomáhajú jej pokryť väčšie povrchy; pri zlepšovaní akcie odmasťovača. Znížením jeho povrchového napätia je prispôsobený molekúl vzduchu, s ktorými sa tvoria bubliny.
Emulzia
Na druhej strane, nízke vyššie napätie sú spojené so stabilizáciou emulzií, veľmi dôležité pri formulácii sortimentu rôznych produktov.
Jednoduché experimenty
 Kovová spona plávajúca v dôsledku napätia povrchovej vody. Zdroj: Alvesgaspar [CC By-S (https: // creativeCommons.Org/licencie/By-SA/3.0)]
Kovová spona plávajúca v dôsledku napätia povrchovej vody. Zdroj: Alvesgaspar [CC By-S (https: // creativeCommons.Org/licencie/By-SA/3.0)] Nakoniec budú citované niektoré experimenty, ktoré sa dajú vykonať v akomkoľvek domácom priestore.
Experiment
V pohári so studenou vodou sa na jeho povrch umiestni kovová spona. Ako je vidieť na hornom obrázku, klip zostane nad vodou vďaka povrchovému napätiu vody. Ale ak sa do skla pridá malá láva Loza, povrchové napätie sa dramaticky zníži a spona náhle klesne.

Papierová loďka
Ak máme papierovú loď alebo drevenú paletu, a ak si umývate malú alebo čistiaci prostriedok, pridá sa do hlavy tampónu, potom dôjde k zaujímavému javu: dôjde k odporu, ktorý ich roztiahne smerom k okrajom sklo. Papierová loď a drevená paleta sa presunie od tampónu rozmazaného čistiacim prostriedkom.

Ďalším podobným a grafickejším experimentom je opakovanie tej istej operácie, ale v vedre s vodou nastriekanou čiernym korením. Častice korenia sa pohnú preč a povrch pôjde z korenia na kryštalický, s okrajmi na okrajoch.
Odkazy
- Whitten, Davis, Peck & Stanley. (2008). Chémia. (8. vydanie.). Učenie sa.
- Wikipedia. (2020). Povrchové napätie. Zdroj: In.Wikipedia.orgán
- USGS. (s.F.). Napätie a voda. Zdroj: USGS.Vláda
- Jones, Andrew Zimmerman. (12. februára 2020). Povrchové napätie - definícia a experimenty. Zotavené z: Thoughtco.com
- Susanna Lauren. (15. novembra 2017). Prečo je povrchové napätie dôležité? Vedecký biolín. Obnovené z: blogu.Biolinscientifický.com
- Nováčik. (7. novembra 2019). Čo je povrchové napätie Cool vedecký experiment. Získané z: nováčika.com
- Jessica Mock. (2020). Experiment s povrchovým napätím. Štúdium. Získané z: štúdie.com
- Dieťa by to malo vidieť. (2020). Sedem experimentov povrchového napätia - Fyzikálna dievča. Získané z: thekidshouldsseethis.com

