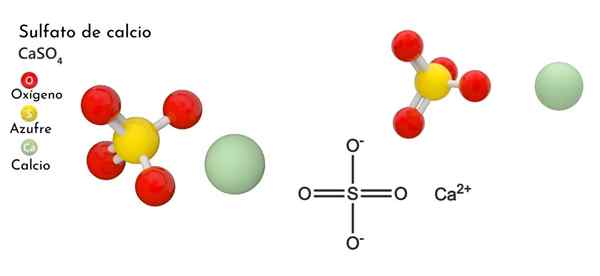
Chemická štruktúra vápenatého sulfátu (Case4), Vlastnosti, použitie
- 1561
- 290
- Denis Škriniar
Čo je síran vápnik?
On sírany vápena Je to ternárna soľ vápnika, zásadité kovy (MR. Schoambara), Síra a kyslík. Jeho chemický vzorec je prípad4, Čo znamená, že pre každú katión CA2+ je tu anión42- Interakcia s tým. Predstavuje zlúčeninu so širokým distribúciou v prírode.
Jeho najhojnejšími formami sú prípad4· 2h2Alebo (omietka) a prípad bezvodej formy4 (Anhydrit). K dispozícii je tiež tretia forma: omietka alebo omietka v Paríži, produkovaná zahrievaním omietky (hemidrate, puzdro4· 1/2h2Buď).
Sulfát vápenatého je veľmi užitočnou zlúčeninou v práci ľudskej bytosti, pretože sa používa v mnohých funkciách, ktoré zahŕňajú konštrukciu ciest, domácu ozdobu a dokonca aj opravu kostí.
Chemická štruktúra síranu vápenatého

Na hornom obrázku je pre tento prípad zobrazený orhorrombická jednotná bunka4. Tu sa predpokladá, že interakcie sú čisto elektrostatické; to znamená, že CA katióny2+ Priťahujú tetraedrálne anióny42-.
Avšak CA2+ Je veľmi náchylný na koordináciu a vytvára okolo neho polyhedrálne štruktúry. Za čo je toto? Na elektronickú dostupnosť vápnika na prijatie elektrónov základných alebo negatívnych druhov (napríklad atómy O SO42-).
Berúc do úvahy predchádzajúci bod, teraz CA ióny2+ Prijímajú datívne odkazy (poskytnuté O) a jednotková bunka sa transformuje, ako je uvedené v dolnom obrázku:
V dôsledku toho sa tvorí Polyhedro CAO8 (Zelená guľa CA2+ obklopené ôsmimi červenými guľami alebo tetrahedra4 Zavrieť). Vápenaté polyhedros a sulfát tetraedra; Toto je kryštalická štruktúra prípadu4 bezvodý.
Môže vám slúžiť: Bipe Beraral: Čo je, vlastnosti, čo je preOkrem toho, keď sú kryštály hydratované -di -hydratovaná soľ alebo hemidrarát (puzdro (puzdro4· 1/2 h2O)- Štruktúra je oneskorená na začlenenie molekúl vody.
Tieto molekuly môžu byť rozptýlené a koordinované s vápnikom; to znamená, že nahrádzajú jednu alebo dve skupiny sulfátov.
Na druhej strane nie všetka voda pokračuje v integrácii Cao polyhedronu8. Niektorí na druhej strane tvoria vodíkové mosty s sulfátmi. Tieto slúžia ako únia pre dve časti v kľukatej časti, produkty usporiadania iónov v skle.
Vlastnosti síranu vápenatého
 Vzhľad síranu vápenatého
Vzhľad síranu vápenatého Molekulárna receptúra
Case4 · NH2O.
Bezvodá molekulová hmotnosť
136,134 g/mol.
Vôňa
Je to toaleta.
Aspekt
V prípade anhydritu to vyzerá ako biely ortorbický alebo monoklinický tuhý prášok. Kryštály majú variabilnú farbu: môžu byť biele alebo s modrým, šedivým alebo červenkastým farbivom; Môže to byť tiež tehlová červená.
Hustota
2,96 GR/CM3 (bezdôvodná forma). 2,32 GR/CM3 (forma dihydrátu).
Bod topenia
1450 ° C (2840 ° F). Charakteristika silných elektrostatických interakcií medzi dvojmocnými iónmi CA2+ A tak42-.
Rozpustnosť
0,2-0,3 % vo vode pri 25 ° C. Je málo rozpustný vo vode a nerozpustný v etanole.
Stabilita
Stabilné pri izbovej teplote.
Použitie síranu vápenatého
V stavebníctve a umení
Používa sa na vypracovanie štuku na frisar steny domov a ďalších konštrukcií, ktoré prispievajú k jeho skrášľovaniu. Okrem toho sa médiá vyrábajú na streche a rámoch okien. Priehrada je tiež na Rush oblohe.
Síran vápenatý sa používa na vyriešenie problému, ktorý sa vyskytuje pri hydratácii betónu, a tak spolupracuje pri výstavbe ciest, spôsobov atď.
Môže vám slúžiť: elektrofil: reakcie, príklady, elektrofylitaS omietkou sú sochy rozpracované, najmä náboženské postavy, a na cintorínoch, ktoré sa používajú v náhrobkoch.
Terapeutika
Veterinár
Experimentálne sa u veterinárnych lekárov použili sterilné kusy síranu vápenatého.
Priehrada alebo parížska omietka sa môže použiť na opravu kostných defektov pre svoju jedinečnú schopnosť stimulovať osteogenézu. Štúdie X -Ray a Techecium (TC99M) Medronate.
Regenerácia kostí bola preukázaná u šiestich psov v období 4 až 6 mesiacov. V tejto oblasti sa začal v tomto poli používať sulfát.
Nahradenie kostí síranu vápenatého je porovnateľná s výmenou pozorovanou v autogénnej kosti.
Ruhaimi (2001) aplikoval sulfát vápenatého v novo zničenej kosti králikovej čeľuste, pričom pozoroval zvýšenie osteogenézy a kalcifikácie kostí.
Liek
Sulfát vápenatý sa používa v medicíne na imobilizáciu kĺbov, ktoré utrpeli dislokácie a v zlomených kostiach, okrem toho, že sa používa ako pomocník pri vypracovaní tabliet.
odontológia
V stomatológii sa používa ako základ na vypracovanie zubných protéz, na výplne a dojmy zubov.
V rozpracovaní potravín
Používa sa ako koagulant pri vypracovaní tofu, potravín vyrobeného zo sóje a veľkej spotreby vo východných krajinách ako náhrada mäsa. Okrem toho sa používa ako opätovné potvrdenie potravín a pri liečbe múky.
Môže vám slúžiť: alotropiaAko hnojivo a kondicionér úrodných pôd
Omietka (puzdro4· 2h2O) Používa sa ako hnojivo v Európe od 18 rokov.
Vápnik musí byť k dispozícii pre korene rastlín pre primeraný dodávok. Potom pridanie vápnika zlepšuje záhradnícke a arašidové plodiny (arašidy).
Hniloba arašidových koreňov produkovaných biologickými patogénmi, ako aj apikálna hniloba melónu a paradajok, sú čiastočne kontrolované pomocou poľnohospodárskych omáčkových aplikácií.
Priehrada pomáha znižovať disperziu hliny a spôsobuje tvorbu chrasty na zemi. Znížením chrasty vytvorených na zemi sa omietka uľahčuje výstup sadeníc. Zvyšuje tiež vstup vzduchu a vody na zem.
Priehrada pomáha zlepšovať pôdu zmierňovaním kyslosti a toxicity hliníka, čím sa prispôsobuje plodine na sodíkové pôdy.
Pri výrobe iných zlúčenín
Sulfát vápenatý reaguje s hydrogenuhličitom amónnym za vzniku síranu amónneho. Používa sa tiež v procese výroby kyseliny sírovej.
Ashidro sulfát vápnika sa zmieša s bridlicom alebo štíhlom a keď sa zmes zahrieva, uvoľňuje sa trioxid síry. Oxid síry je prekurzor kyseliny sírovej.