Estery
- 2574
- 297
- Adrián Fajnor
 Esteres sú organické zlúčeniny, ktoré majú zložku kyseliny karboxylovej a ďalší alkohol
Esteres sú organické zlúčeniny, ktoré majú zložku kyseliny karboxylovej a ďalší alkohol Čo sú estery?
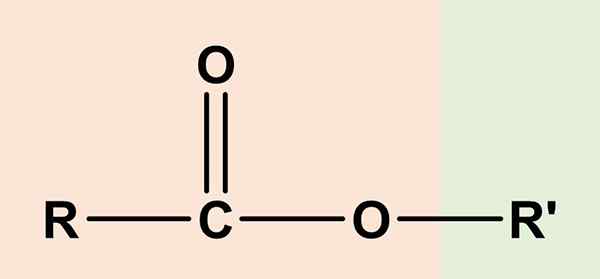
Ten estery Sú to organické zlúčeniny, ktoré majú zložku karboxylovej kyseliny a ďalší alkohol. Jeho všeobecný chemický vzorec je RCO2R' alebo rcoor'. Pravá strana, rcoo, zodpovedá karboxylovej skupine, zatiaľ čo vpravo, alebo' Je to alkohol. Obaja zdieľajú atóm kyslíka a zdieľajú určitú podobnosť s étermi (ror ').
Z tohto dôvodu etylový oct3Kočiary2Chvály3, Najjednoduchší estery sa považoval za Kyselina kyselina octic alebo ocot, A odtiaľ etymologický pôvod mena „ester“. Takže ester spočíva v nahradení kyslého vodíka skupiny COOH, požičovňou alkoholu z alkoholu.
Kde sú estery?
Z pôd organickej chémie existuje veľa prírodných zdrojov. Príjemná vôňa ovocia, ako sú banány, hrušky a jablká, je produktom interakcie esterov s mnohými ďalšími komponentmi. Nachádzajú sa tiež vo forme triglyceridov v olejoch alebo tukoch.
Naše telo vyrába triglyceridy z mastných kyselín, ktoré majú dlhé sýtené reťazce a alkohol glycerol. To, čo odlišuje niektoré estery od iných, leží v R, v reťazci kyslej zložky, ako v R ', v reťazci alkoholickej zložky.
Ester s nízkou molekulovou hmotnosťou musí mať málo uhlíkov v R a R ', zatiaľ čo iné, ako napríklad vosky, majú veľa uhlíkov, najmä v r', alkoholickej zložke, a teda vysokých molekulových hmotnostiach.
Nie všetky estery sú však prísne organické. Ak je atóm Carbonyl Group nahradený jedným z fosforu, potom bude mať RPOOR '. Toto je známe ako fosfátový ester a majú zásadný význam v štruktúre DNA.
Vždy, keď sa dá atóm účinne spájať s uhlíkom alebo kyslíkom, ako je síra (RSOOR '), môže následne tvoriť anorganický ester.
Vlastnosti ESTRES
Estery nie sú kyseliny alebo alkoholy, takže sa ako také správajú. Napríklad jeho body topenia a varu sú nižšie ako tie, ktoré majú podobné molekulové hmotnosti, ale bližšie k hodnotám aldehydov a ketónov.
Kyselina butánová, Cho3Chvály2Chvály2CoOH, má bod varu 164 ° C, zatiaľ čo etylacetát, ch3Kočiary2Chvály3, zo 77.1. c.
Okrem nedávneho príkladu varu 2-metylbután3Chváli3)2Chvály3, Metylacetát, Cho3Kočiary3, a 2-butanol, Cho3,Ch (oh) ch2Chvály3, Sú to nasledujúce: 28, 57 a 99 ° C. Tieto tri zlúčeniny majú molekulové hmotnosti 72 a 74 g/mol.
Estery s nízkym molekulárnym pesosom majú tendenciu byť prchavé a majú príjemné pachy, a preto im ich obsah v ovocí dáva svoje rodinné vône. Na druhej strane, keď sú ich molekulové hmotnosti vysoké, sú bezfarebné a bez zápachu kryštalických tuhých látok alebo v závislosti od ich štruktúry, môžu vykazovať mastné vlastnosti.
Rozpustnosť
Karboxylové kyseliny a alkoholy sú zvyčajne rozpustné vo vode, pokiaľ nemajú vo svojich molekulárnych štruktúrach vysoký hydrofóbny charakter. To isté platí pre estery. Ak sú R alebo R 'krátke reťazce, ester môže interagovať s molekulami vody prostredníctvom dipól-dipolo a síl londýnskych síl.
Môže vám slúžiť: chemická zlúčeninaJe to preto, že estery sú akceptory vodíkového mosta. Ako? Pre svoje dva atómy kyslíka RCOOR “. Molekuly vody môžu tvoriť vodíkové mosty s ktorýmkoľvek z týchto kyslíkov. Ale keď sú reťaze R alebo R veľmi dlhé, odrazujú vodu vo svojom okolí, čo znemožňuje ich rozpustenie.
Zjavný príklad sa to vyskytuje u triglyceridných esterov. Ich bočné reťazce sú dlhé a vo vode vytvárajú oleje a tuky, pokiaľ nie sú v kontakte s menším polárnym rozpúšťadlom, viac súvisí s týmito reťazcami.
Hydrolýza
Esteres môže tiež reagovať s molekulami vody v tzv. Hydrolýznej reakcii. Vyžadujú však kyslé alebo základné prostredie na podporu mechanizmu uvedenej reakcie:
Rcoor ' + H2Ani RcoOh + R'oH
(Kyslá polovica)
Molekula vody sa pridá do karbonylovej skupiny, c = o. Kyslá hydrolýza je zhrnutá pri nahradení každého r 'alkoholickej zložky OH z vody. Všimnite si tiež, ako sa ester „zlomí“ vo svojich dvoch komponentoch: kyselina karboxylová, RCOOH a R'OH alkohol.
Rcoor ' + Oh- => RCOAni- + R'oH
(Základné médium)
Keď sa hydrolýza vykonáva v základnom médiu, vyskytuje sa ireverzibilná reakcia známa ako zľavivosť. Toto je veľmi zamestnané a je základným kameňom pri vypracovaní remeselníckych alebo priemyselných mydiel.
RCOO- Je to karboxylátový anión, stabilný, ktorý je elektrostaticky spojený s prevládajúcim katiónom v strede.
Ak je použitá základňa NaOH, vytvorí sa soľ. Ak je ester triglycerid, ktorý má podľa definície tri bočné reťazce R, tvoria sa tri mastné kyseliny, RCOONE a alkohol glycerolu.
Redukčná reakcia
Estery sú vysoko oxidované zlúčeniny. To znamená, že má niekoľko kovalentných väzieb s kyslíkom. Elimináciou väzieb C-O dochádza k zlomeniu, ktoré končí oddelením kyseliny a alkoholických zložiek; A ešte viac, kyselina sa redukuje na menej oxidovaný spôsob na alkohol:
RCoor '=> rch2Oh + r'oh
Toto je redukčná reakcia. Je potrebné silné redukčné činidlo, ako je lítium a hydrid hliníka, Liah4, a kyslého média, ktoré podporuje migráciu elektrónov. Alkoholy sú najmenšie formy, to znamená, že tie, ktoré majú menej kovalentných väzieb s kyslíkom (iba jedna: C-oh).
Dva alkoholy, rch2Oh + r'OH, poďte z dvoch príslušných reťazcov pôvodného esteru RCOOR '. Toto je metóda syntézy alkoholov s pridanou hodnotou z jeho esterov.
Napríklad, ak by ste chceli vyrábať alkohol exotických esterov, bola by to dobrá cesta na tento účel.
Transterifikačná reakcia
Estery sa môžu transformovať na ostatných, ak reagujú na kyslé alebo základné médiá s alkoholmi:
Rcoor ' + R "Oh RcoAlebo „ + R'oH
Esterová štruktúra
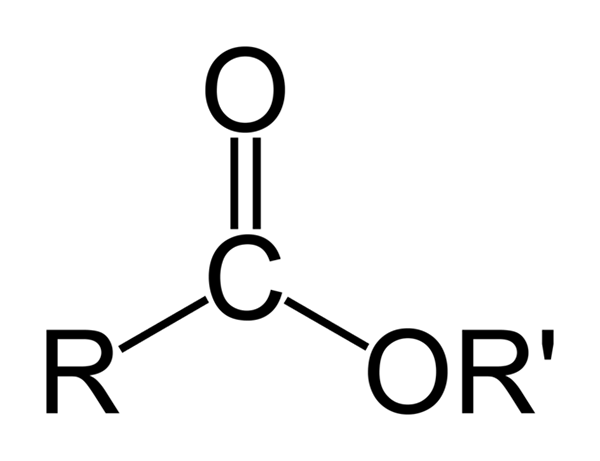 Všeobecná chemická štruktúra organických esterov. Zdroj: Ben Mills Via Wikipedia
Všeobecná chemická štruktúra organických esterov. Zdroj: Ben Mills Via Wikipedia Vynikajúci obraz predstavuje všeobecnú štruktúru všetkých organických esterov. Všimnite si, že r, karbonylová skupina C = o a ', tvoria plochý trojuholník, produkt hybridizácie SP2 centrálneho atómu uhlíka. Iné atómy však môžu prijať ďalšie geometrie a ich štruktúry závisia od vnútornej povahy R alebo R '.
Môže vám slúžiť: dusičnany: vlastnosti, štruktúra, nomenklatúra, školenieAk sú r alebo r 'jednoduché reťazce alqulicas, napríklad typu (zvoľte2)nChvály3, Vyzeráte zigzagueady vo vesmíre. Toto je prípad pentilo butanaotu3Chvály2Chvály2Kočiary2Chvály2Chvály2Chvály2Chvály3.
Ale v ktoromkoľvek z uhlíkov týchto reťazcov bolo možné nájsť vetvu alebo nenasýtenie (C = C, C≡C), ktorá by modifikovala globálnu štruktúru esteru. A z tohto dôvodu sa jeho fyzikálne vlastnosti, ako je rozpustnosť a body varu a fúzie, sa menia pri každej zlúčenine.
Napríklad nenasýtené tuky majú vo svojich R reťazcoch dvojité spojenia, ktoré negatívne ovplyvňujú intermolekulárne interakcie. V dôsledku.
Akceptor vodíka
Aj keď obraz kostry esterov vyniká viac, sú to reťazce R a R zodpovedné za rozmanitosť svojich štruktúr.
Štrukturálna charakteristika esterov sa však zaslúži s trojuholníkom: sú to akceptory vodíkového mosta. Ako? Podľa kyslíka skupín karbonyl a alcoxidov (-orer ').
Majú páry voľných elektrónov, ktoré môžu priťahovať čiastočne pozitívne atómy vodíka molekúl vody.
Preto ide o špeciálny typ interakcií dipólov-dipól. Molekuly vody sa blížia k esteru (ak reťazce R O R 'nezabránia a mosty sa tvoria c = o-h2Alebo, alebo oh2-O-r '.
Nomenklatúra esterov
Aby sme primerane pomenovali ester, je potrebné. Tiež akúkoľvek možnú vetvu, substituent alebo nenasýtenie.
Akonáhle sa to stane, pridá sa názov r 'skupiny Alcoxid Group -alebo' -ilo, Zatiaľ čo reťazec skupiny Carboxilo -Coor R, prípona -Ato. Po prvé, je uvedená časť R, po ktorej nasleduje slovo „z“ a potom názov sekcie R 'sekcia'.
Napríklad Cho3Chvály2Chvály2Kočiary2Chvály2Chvály2Chvály2Chvály3 Má päť uhlíkov na pravej strane, to znamená, že sú to tie, ktoré zodpovedajú R '. A na ľavej strane sú štyri atómy uhlíka (vrátane karbonylovej skupiny C = O).
Preto je r 'skupinou Pentil a r a bután (za zahrnutie karbonylu a vzhľadom na hlavný reťazec). Potom, aby ste pomenovali zlúčeninu, stačí pridať zodpovedajúce prípony a pomenovať ich v správnom poradí: butánAto úbohýilo.
Ako pomenovať nasledujúcu zlúčeninu: ch3Chvály2Cooc (ch3)3? Reťazec -c (CHO3)3 zodpovedá rekto-butylovému alquilitnému substituentovi. Pretože ľavá strana má tri uhlíky, je to „propán“. Jeho meno je potom: propánAto z terc-but-butilo.
Ako sa tvoria estery?
Esterifikácia
Existuje veľa trás na syntézu esteru, z ktorých niektoré môžu byť dokonca nové. Všetci sa však zbližujú v tom, že musí byť vytvorený trojuholník obrazu štruktúry, to znamená Co-O Link. Z tohto dôvodu musí začať od zlúčeniny, ktorá má predtým karbonylovú skupinu: ako karboxylová kyselina.
A čo by mala byť spojená karboxylová kyselina? Na alkohol, inak by nemal alkoholický komponent, ktorý charakterizuje estery. Karboxylové kyseliny však vyžadujú teplo a kyslosť, aby sa umožnil pokračovať reakčný mechanizmus. Vyššie uvedená chemická rovnica predstavuje:
Môže vám slúžiť: hydrid hliníka (ALH3): štruktúra, vlastnosti, použitiaRCOOH + R'OH RCOOR ' + H2Ani
(Kyslá polovica)
Toto je známe ako esterifikácia.
Napríklad mastné kyseliny môžu esterifikovať metanolom, Cho3Och, aby nahradili svoje kyseliny metylovými skupinami, takže táto reakcia sa dá považovať za ako metylácia. Toto je dôležitý krok pri určovaní profilu mastných kyselín určitých olejov alebo tukov.
Estery z kyslých chloridov
Ďalším spôsobom, ako syntetizovať estery, je z acylchloridov, RCOCL. V nich je namiesto toho, aby nahradil skupinu OH hydroxylovej skupiny, atóm CL je nahradený:
Rcocl + r'OH => rCoor ' + hcl
A na rozdiel od sterifikácie kyseliny karboxylovej sa voda nevydáva, ale kyselina chlorovodíková.
Ďalšie metódy sú k dispozícii vo svete organickej chémie, ako je oxidácia Baeyer-Villiger, ktorá používa peroxy kyseliny (RCOOOH).
Estres používa
 Esteres sa používajú pre rôzne veci, ako je výroba sviečok
Esteres sa používajú pre rôzne veci, ako je výroba sviečok Medzi hlavné použitia esterov patrí:
- V vypracovávaní sviečok alebo sviečok, ako napríklad vynikajúci obraz. Na tento účel sa používajú veľmi dlhé estery postranného reťazca.
- Ako liek konzervačné látky alebo jedlo. Je to kvôli pôsobeniu parabénov, ktoré nie sú ničím iným ako estery kyseliny para-hydroxibenzoovej. Aj keď si zachovávajú kvalitu produktu, existujú štúdie, ktoré spochybňujú jeho pozitívny vplyv na telo.
- Podávajú na výrobu umelých vôní, ktoré napodobňujú vôňu a chuť mnohých ovocia alebo kvetov. Takže estery sú prítomné v dobrotách, zmrzline, parfumoch, kozmetike, mydlách, šampónoch, okrem iných komerčných výrobkov, ktoré si zaslúžia arómy alebo atraktívne príchute.
- Estery môžu tiež poskytnúť pozitívny farmakologický účinok. Z tohto dôvodu sa farmaceutický priemysel venoval syntéze esterov odvodených z kyselín prítomných v tele na vyhodnotenie akéhokoľvek možného zlepšenia pri liečbe chorôb. Aspirín je jedným z najjednoduchších príkladov týchto esterov.
- Kvapalné estery, ako je etylacetát, sú primeranými rozpúšťadlami pre určité typy polymérov, ako je nitrocelulóza a široký spektrum živíc.
Príklady esterov
Niektoré ďalšie príklady esterov sú nasledujúce:
- Butanato de pentilo, ch3Chvály2Chvály2Kočiary2Chvály2Chvály2Chvály2Chvály3, ktoré vonia ako albicoque a hrušky.
- Vinylacetát, Cho3Kočiary2= CH2, z ktorého dochádza k polyvinylacetátu.
- Izopentilo pentanoa, ch3Chvály2Chvály2Chvály2Kočiary2Chvály2Chváli3)2, ktoré napodobňujú chuť jabĺk.
- Etylpanoát, ch3Chvály2Kočiary2Chvály3.
- Propyl metanoate, hcooch2Chvály2Chvály3.
Odkazy
- Tón.W. Graham Solomons, Craight B. Fryhle. Organická chémia. (Desiate vydanie, s. 797-802, 820) Wiley Plus.
- Carey, f. Do. Organic Chemistry (2006) Šieste vydanie. Redakcia MC Graw Hill-
- Chémia librettexts. Nomenklatúra eserov. Získané z: Chem.Librettexts.orgán
- Správca. (19. september 2015). Estery: jeho chemická povaha, vlastnosti a použitia. Prevzaté z: čisto-chemického.com
- Organická chémia v našom každodennom živote. (9. marca 2014). Aké sú použitia esterov? Získané z: Gen2ChemistAssignment.Slečna.com
- Chemický materiál.Net (2018). Príklady esterov. Obnovené z: chemiky.slepo
- Paz María de Lourdes Cornejo arteaga. Hlavné aplikácie esterov. Prevzaté z: UAEH.Edu.mx
- Jim Clark. (Január 2016). Úvod. Zobraté z: Chemguide.co.Uk

