Zloženie, typy a príklady kryštaloidných roztokov
- 3926
- 242
- Gabriel Bahna
Ten Kryštaloidné roztoky Sú to tie, ktoré tvoria rozpustenie elektrolytu a iných malých molekúl rozpustných vo vode, ktoré sa používajú v klinických rutinných postupoch, ako je napríklad upravujúci objem tekutiny obehového systému. Z jednoduchého chemického hľadiska: Tieto roztoky nie sú ničím iným ako vodnými a zriedenými ťažobnými riešeniami.
Kryštaloidné roztoky hrajú dôležitú úlohu v klinických terapiách, ako sú intravenózne infúzie tekutín pre prípady krvácania, dehydratácie, hypovolémie a infekcií. Zvyčajne je jej koncentrácia soľného roztoku izotonická, čo znamená, že počet jeho rozpustených iónov je porovnateľný s hodnotou krvnej plazmy.
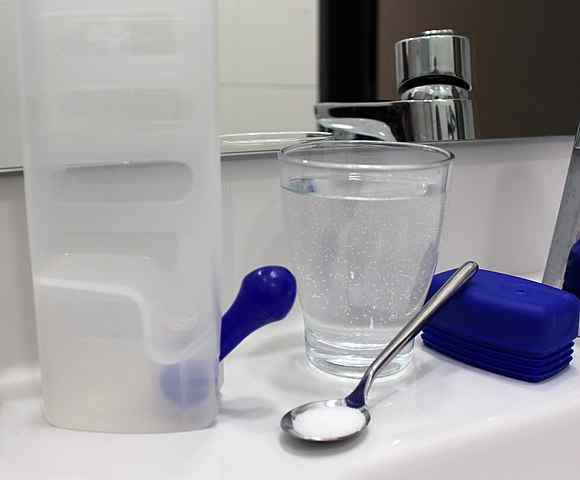
 Kryštaloidný roztok sa dá pripraviť jednoducho rozpustením soli a iných rozpustených látok vo vode v miernej koncentrácii. Zdroj: Rillke/CC By-SA (https: // creativeCommons.Org/licencie/By-SA/3.0)
Kryštaloidný roztok sa dá pripraviť jednoducho rozpustením soli a iných rozpustených látok vo vode v miernej koncentrácii. Zdroj: Rillke/CC By-SA (https: // creativeCommons.Org/licencie/By-SA/3.0) Kryštaloidné roztoky preto nespôsobujú osmotické zmeny, ale poskytujú správny objem kvapaliny tak, aby krv pokračovala v zavlažovaní obehovým systémom. Týmto spôsobom sa dosahuje, že srdce pumpuje zriedenú krv a môže do tkanív dodávať kyslík.
Príkladom kryštaloidného roztoku je normálny roztok soľného roztoku, ktorý obsahuje NaCl pri koncentrácii 0,9%. V závislosti od klinického prípadu sa však môžu zvoliť ďalšie roztoky s rôznymi komponentmi, koncentráciami a typmi tonicity.
[TOC]
Zloženie kryštaloidných roztokov
Všetky kryštaloidné roztoky sú založené na sterilizovaných alebo mikroorganizmoch, takže je to jeho obľúbené rozpúšťadlo. Inak nemohli integrovať zdravé do nášho tela a spôsobiť žiadnu nežiaducu reakciu. Ako roztok alebo riešenie, ktoré je, má tiež rozpustené látky, ktoré sú v podstate minerálne soli alebo silné elektrolyty.
Predaj môže byť niekoľko, pokiaľ prispievajú v miernych koncentráciách NA iónov+, Ac2+, Klimatizovať+ a cl-. Okrem anorganických solí môžu mať aj veľmi rozpustné organické rozpustené látky vo vode, ako sú octany, glukonáty a laktáty. Niektoré z týchto roztokov tiež obsahujú glukózu (dextróza).
Môže vám slúžiť: hydroxyapatitKoncentrácie týchto solí alebo rozpustených látok sú veľmi rozmanité a sú vyjadrené buď v percentách, miligrammi decilitrmi (mg/dl), molaritami alebo osmolaritami. Výber jedného alebo druhého bude závisieť od klinických kritérií.
Chlapci
Na začiatku sa povedalo, že kryštaloidné roztoky sa často používajú na zabezpečenie objemu kvapaliny do obehového systému. V tomto procese v závislosti od jej tonicity trpí krvná plazma alebo neosmotické zmeny, ktoré u pacienta podporujú alebo uprednostňujú určité požadované stavy.
Jedinou vecou, ktorá odlišuje kryštaloidné roztok od iného, nie je chemická povaha jeho rozpustenej látky, ale jeho tonicita; to znamená, že ak je to hypertonické, izotonické alebo hypotonické riešenie.
Hypertonický
Hypertonický kryštaloidný roztok je taký, že ktorého koncentrácia soľného roztoku je lepšia ako koncentrácia v krvnej plazme. Preto voda migruje z vnútra buniek do plazmy, ktorá zvýšila svoju tonicitu v dôsledku prítomnosti hypertonického kryštaloidného roztoku. Príkladom tohto typu roztoku je 3% NaCl, najmä koncentrovanejší ako 0,9% normálny soľný roztok.
Tieto roztoky sú kontraindikované pre väčšinu klinických prípadov, s výnimkou tých, ktoré prezentujú neurologické následky.
Izotonický
Izotonický kryštaloidný roztok je ten, ktorého koncentrácia soľného roztoku je porovnateľná alebo identická s koncentráciou krvnej plazmy a koncentrácie bunkového interiéru. Preto medzi týmito dvoma médiami nedochádza k výmene vody. Príkladom tohto typu roztoku je 0,9%NaCl, už je uvedený vyššie.
Hypotonický
A nakoniec, hypotonický kryštaloidný roztok je ten, ktorého koncentrácia soľného roztoku je nižšia ako koncentrácia krvnej plazmy a intracelulárneho kompartmentu alebo priestoru. Tentoraz sa voda presúva do interiéru buniek až do dosiahnutia rovnováhy. Príkladom tohto typu roztoku je 0,45% NaCl.
Môže vám slúžiť: zásadné kovyRovnako ako v prípade hypertonických kryštaloidných roztokov, hypotonické sú kontraindikované pre väčšinu klinických prípadov, najmä pre tie, kde existuje riziko mozgového edému.
Príklady kryštaloidných roztokov
Nižšie sa uvádzajú a sú opísané niektoré príklady kryštaloidných roztokov. Rozdiel medzi jedným a druhým bude ležať v identite jeho elektrolytov alebo rozpustených soli.
Normálny roztok soľného roztoku
Normálny roztok soľného roztoku má 0,9%zloženie NaCl, je izotonický a je tiež najbližším kryštaloidným roztokom, pretože slúži na liečbu infinícií bežných prípadov dehydratácie; ako napríklad tie, ktoré sú spôsobené hnačkou, šokom, zvracaním, krvácaním,. Vyhýba sa však použitiu u pacientov s obličkami alebo srdcovými problémami.
Laktát
Tiež známy ako Ringer alebo Hartmann roztok (hoci sa mierne líšia v ich iónových koncentráciách), je to tak, ktorý sa skladá zo zmesi chloridu sodného, laktátu sodného, chloridu vápenatého a chloridu draselného.
Jeho soľné zloženie je zloženie, ktorá sa podobá zloženiu krvnej plazmy, takže je izotonický typ. Používa sa ako nastavovacia tekutina alebo tekutina pre prípady popálenín, traumy, elektrolytickej nerovnováhy, metabolickej acidózy. Je však kontraindikovaný pre pacientov trpiacich hyperkalciémiou.
Laktát sa v našom tele metabolizuje a končí transformovaním na hydrogenuhličitan. Tento roztok môže obsahovať aj anión glukonátu, ako aj určité množstvá horčíka, mg2+.
Glukóza
Tiež známy ako dextróza kryštaloidný roztok, je dodávaný v dvoch koncentráciách: 5 a 10% (D5 alebo D10). Toto je spočiatku hypotonické, ale po absorbovaní glukózy sa transformuje na izotonický. Aj keď poskytuje značné množstvo kalórií, je kontraindikovaný pre pacientov trpiacich hyperglykémiou.
Môže vám slúžiť: kyselina elagová: štruktúra, vlastnosti, získanie, umiestnenie, použitieNa rozdiel od iných kryštaloidných roztokov sú to sladké. Najsladšie majú koncentrácie väčšie ako 10% (D20, D30, D50 atď.) A sú určené pre pacientov s pľúcnym a opuchom mozgu. Na druhej strane znižujú katabolizmus bielkovín, chránia pečeň a pomáhajú bojovať proti zrúteniu obehov.
Hypertonické a hypotonické soľné roztoky
Hypertonické roztoky soľného roztoku (3 a 5% NaCl) sa používajú na dodávku tekutiny spaľujúcim pacientom, vyvolanie hyperosmolarity a zmiernenie renálnych nedostatkov. Na druhej strane, hypotonické roztoky soľného roztoku (0,45% NaCl alebo nižšie koncentrácie), kontrola hypernatrémie a sú kontraindikované pre spaľujúcich pacientov.
Preto človek dodáva účinky v rozpore s druhým; Ak je hypertonický roztok nevyhnutný, hypotonický je neschvaľovaný a naopak.
Mechanizmus za všetkými kryštaloidnými roztokmi je založený na osmotickej a vodnej rovnováhe medzi intra a extracelulárnymi tekutinami.
Odkazy
- Lewis Sr a kol. (3. augusta 2018). Koloidy alebo kryštaloidy na výmenu tekutín u kriticky ľudí. Spolupráca Cochrane. Získané z: Cochrane.orgán
- Epstein Em, Waseem m. (29. novembra 2019). Kryštaloidné tekutiny. In: Statpearls. Treasure Island (FL): Statpearls Publishing 2020 -. Získané z: NCBI.NLM.NIH.Vláda
- Wikipedia. (2020). Expandér objemu. Zdroj: In.Wikipedia.orgán
- Elsevier B.Vložka. (2020). Kryštaloid. Vedecký. Zdroj: ScienceDirect.com
- Sheila Bouie. (2020). Kryštaloidy: Definícia a príklad. Štúdium. Získané z: štúdie.com

