Cheritalita
- 2500
- 369
- Tomáš Klapka
 Chiralita je spojená s asymetriou a stane sa, keď sa prvok nedá prekrývať v zrkadle v zrkadle. Zdroj: Gabriel Bolívar
Chiralita je spojená s asymetriou a stane sa, keď sa prvok nedá prekrývať v zrkadle v zrkadle. Zdroj: Gabriel Bolívar Čo je to chiralita?
Ten cheritalita Je to geometrická vlastnosť, v ktorej môže mať objekt dva obrázky: jeden vpravo a jeden vľavo, ktoré nie sú zameniteľné. To znamená, že sú priestorovo odlišné, aj keď zvyšok ich vlastností sú identické. Objekt, ktorý vykazuje chiralitu, sa jednoducho hovorí, že je „chirálny“.
Pravá a ľavá ruka sú chirály: jedným je odraz (zrkadlový obraz) druhého, ale nie sú to isté, pretože keď dajú na druhú stranu, nezhodujú sa s palcami.
Viac ako zrkadlo, aby ste vedeli, či je objekt chirálny, musí sa položiť nasledujúca otázka: Máte „verzie“ pre ľavú aj pravú stranu?
Napríklad doppit pre ľavú ruku a ďalší pre pravé pravé sú chirálne objekty. Dve vozidlá toho istého modelu, ale s volantom vľavo alebo vpravo, pár topánok, rovnako ako chodidlá. Slimákové schody v ľavom smere a v správnom smere atď.
A v chémii nie sú molekuly výnimkou: môžu to byť aj chirals. Na hornom obrázku je zobrazený pár molekúl s tetraedrálnou geometriou.
Aj keď je vľavo otočená a gule modrej a fialovej, hnedá a zelená farba „vyzerajú z lietadla z lietadla.
Ako určiť molekulárnu chiralitu?
S molekulami nie je také jednoduché definovať, ktorá je ľavou alebo pravou „verziou“, ktorá sa na ne len pozerá.
Z tohto dôvodu sa organické chemikálie uchýlia k konfiguráciám (R) alebo (S) Cahn-Ingold-Prelog alebo sú založené na optickej vlastnosti týchto chirálnych látok na otáčanie polarizovaného svetla (čo je tiež chirálny prvok).
Môže vám slúžiť: lítium: História, štruktúra, vlastnosti, riziká a použitieNie je však ťažké určiť, či je molekula alebo zlúčenina chirál iba pozorovaním jej štruktúry. Aká pozoruhodná zvláštnosť má krútiaci moment horného obrázka?
Má štyri rôzne substituenty, z ktorých každý má vlastnú charakteristickú farbu, a tiež geometria okolo centrálneho atómu je tetraedrálny.
Ak je v štruktúre atóm so štyrmi rôznymi substituentmi, je možné potvrdiť (vo väčšine prípadov), že molekula je chirálna.
Potom sa hovorí, že v štruktúre je centrum chirality alebo Stereogénne centrum. Kde je jeden, bude tu niekoľko stereoizomérov známych ako enantioméry.
Dve molekuly obrazu sú enantioméry. Čím väčší počet chirálnych centier, ktoré majú zlúčeninu, tým väčšia je jej priestorová diverzita.
Centrálny atóm je zvyčajne atóm uhlíka vo všetkých biomolekulách a zlúčeninách s farmakologickou aktivitou. Môže to však byť aj fosfor, dusík alebo kov.
Príklady chirality
Chirálne centrum je pravdepodobne jedným z najdôležitejších prvkov pri určovaní, či je zlúčenina chirálna alebo nie.
Existujú však ďalšie faktory, ktoré môžu zostať bez povšimnutia, ale v 3D modeloch ukazuje zrkadlový obraz, ktorý sa nedá prekrývať.
Pre tieto štruktúry sa hovorí, že namiesto centra majú ďalšie prvky chirality.
Z tohto dôvodu už nestačí prítomnosť asymetrického centra so štyrmi substituentmi, ale aj zvyšok štruktúry sa musí starostlivo analyzovať, a preto je schopný rozlíšiť stereoizomér od iného.
Môže vám slúžiť: zinkový hydroxid (Zn (OH) 2)Axiálny
 Štruktúry alela a bifenylovej zlúčeniny. Zdroj: Wikimedia Commons
Štruktúry alela a bifenylovej zlúčeniny. Zdroj: Wikimedia Commons V horných obrazových zlúčeninách, ktoré sa môžu zdať ploché voľným okom, ale v skutočnosti nie sú.
Vľavo máte všeobecnú štruktúru Alena, kde R označuje štyri rôzne substituenty. A vpravo, všeobecná štruktúra bifenylovej zlúčeniny.
Koniec, kde sa nájdu r3 a r4 Dalo by sa to vizualizovať ako „plutva“ kolmo na lietadlo, kde ležia1 a r2.
Ak pozorovateľ analyzuje takéto molekuly, ktoré umiestnia oko pred prvý uhlík spojený s r1 a r2 (Pre Aleno), uvidíte r1 a r2 na ľavej a pravej strane a R4 a r3 hore a dole.
Áno r3 a r4 Zostávajú pevne pevne, ale r1 Napravo a r2 Vľavo bude ďalšia „vesmírna verzia“.
To je miesto, kde pozorovateľ môže dospieť k záveru, že našiel osi chirality pre Aleno. To isté platí pre bifenyl, ale s aromatickými krúžkami zapojenými do videnia.
Prstene alebo skrutky helicity
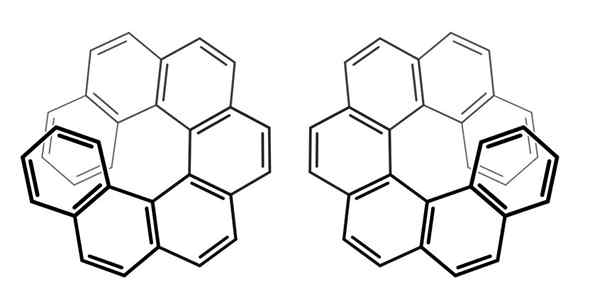
 Os chirality v hepthelicicenos. Zdroj: Wikimedia Commons
Os chirality v hepthelicicenos. Zdroj: Wikimedia Commons Všimnite si, že v predchádzajúcom príklade je os chirality ležaná v kostre c = c = c, pre Aleno a v AR-AR Link, pre bifenyl.
Pre zlúčeniny vyššie, nazývané hepthehelicenos (pre sedem krúžkov), jej osi chirality je os, vrtule.
Preto, aby ste rozlíšili z jedného enantimeru druhého, musíte pozorovať tieto molekuly zhora (najlepšie).
Týmto spôsobom je možné podrobne opísať, že heptheliicen sa točí v smere k ihlám hodiniek (ľavá strana obrázka) alebo v smere antihorária (pravá strana obrázka).
Môže vám slúžiť: hydroxid sodný (NaOH): štruktúra, vlastnosti, použitia, syntézaPlán
Predpokladajme, že už neexistuje helicenus, ale molekula s nekoplanárnymi krúžkami, to znamená, že jeden je nad alebo pod druhým (alebo nie je v rovnakej rovine).
Tu chirálna postava v kruhu tak veľmi nespočíva, ale vo svojich substituentoch, pretože práve títo definujú každý z týchto dvoch enantiomérov.
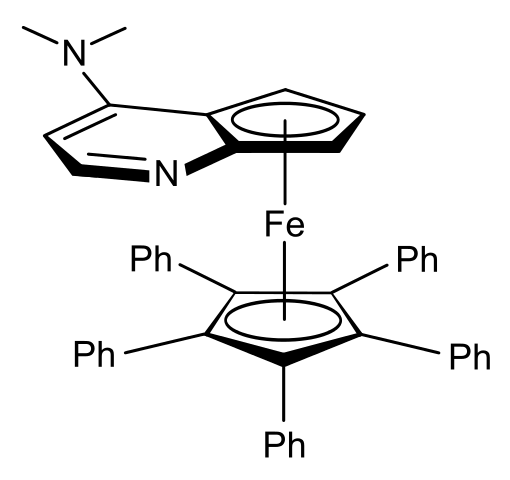
 Planárska chiralita. Zdroj: Wikimedia Commons
Planárska chiralita. Zdroj: Wikimedia Commons Napríklad vo ferroen horného obrázka máte, že krúžky, ktoré „vkladajú“ atóm viery, sa nemenia, ale priestorová orientácia kruhu s atómom dusíka a skupinou -n (Cho (Chore (Chore3)2.
Na obrázku skupina -n (cho3)2 ukazuje naľavo, ale vo svojom enantiómero bude ukazovať doprava.
Ďalší
Pre makromolekuly alebo pre tých, ktorí majú jedinečné štruktúry, sa panorama začína zjednodušiť. Je to preto, že z jeho 3D modelov môžete vidieť let vtákov, ak sú chirálmi alebo nie, ako v prípade predmetov pôvodných príkladov.
Napríklad uhlíková nanotrubica môže ukázať zákruty zákrut vľavo, a preto je chirálna, ak existuje rovnaká, ale s otočením doprava.
To isté platí pre ďalšie štruktúry, kde napriek tomu, že nemali centrá chirality, priestorová dispozícia všetkých jeho atómov môže prijať chirálne formy.
Potom sa hovorí o inherentnej chiralii, ktorá nezávisí od atómu, ale od celej sady.
Chemicky silná forma rozlíšenia „ľavého obrazu“ od obrazu vpravo je cez stereoselektívnu reakciu, to znamená, že môže prejsť iba s enantiomérom, zatiaľ čo s ostatnými nie.
Odkazy
- Chiralita (chémia). Získaný z.Wikipedia.orgán
- Chirmosť. Zotavené z chémie.com

