Zákon o ochrane vecí
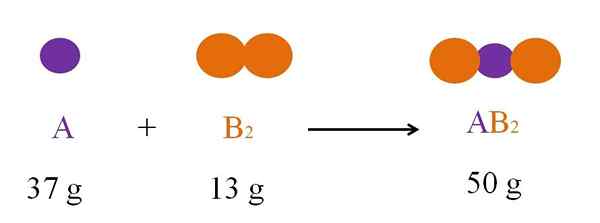
- 2984
- 485
- MUDr. Miloslav Habšuda
Aký je zákon ochrany hmoty?
Ten Zákon o zachovaní hmoty alebo omše Je to ten, ktorý ustanovuje, že pri každej chemickej reakcii sa hmota nevytvorí ani zničí. Tento zákon je založený na skutočnosti, že atómy sú v tomto type reakcií nedeliteľné častice; Zatiaľ čo v jadrových reakciách sú atómy fragmentované, preto sa nepovažujú za chemické reakcie.
Ak sa atómy nezničia, potom, keď reaguje prvok alebo zlúčenina, musí byť počet atómov konštantný pred a po reakcii; čo sa premieta do konštantného množstva hmotnosti medzi príslušnými reagenciami a výrobkami.
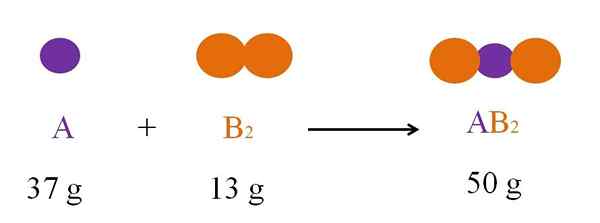 Chemická reakcia medzi A a B2. Zdroj: Gabriel Bolívar
Chemická reakcia medzi A a B2. Zdroj: Gabriel Bolívar Vždy je to tak, ak nedochádza k úniku, ktorý spôsobuje straty hmoty; Ale ak je reaktor pevne zatvorený, „nezmizne“ žiadny atóm, a preto sa zaťažená hmota musí po reakcii rovnať hmotnosti.
Ak je produkt solídny, na druhej strane, jeho hmotnosť sa bude rovnať súčtu činidiel zapojených pre ich tvorbu. Podobne sa vyskytuje pri kvapalných alebo plynných výrobkoch, ale je pravdepodobnejšie, že urobí chyby pri meraní ich výsledných hmotností.
Tento zákon sa zrodil z experimentov v minulých storočiach a posilňoval sa k príspevkom niekoľkých slávnych chemikálií, ako je Antoine Lavoisier.
Zvážte reakciu medzi A a B2 Na vytvorenie AB2 (horný obrázok). Podľa zákona o zachovaní hmoty masa AB2 Musí sa rovnať súčtu masy a a b2, respektíve. Takže, ak 37 g reakcie s 13 g B2, Produkt AB2 Musíte vážiť 50 g.
Preto v chemickej rovnici hmotnosť reagencií (A a B2) sa musí vždy rovnať hmotnosti výrobkov (AB2).
Príklad veľmi podobný novo opísaným je tvorba oxidov kovov, ako je moč alebo hrdza. Hrdza je ťažšia ako železo (aj keď sa zdá), pretože kov reagoval s kyslíkovou hmotnosťou, aby sa vytvoril oxid.
Ako sa tento zákon uplatňuje v chemickej rovnici?
Zákon o zachovaní hromadnej ochrany má transcendentálny význam v stechiometrii, pričom druhá sa definuje ako výpočet kvantitatívnych vzťahov medzi činidlami a produktmi prítomnými v chemickej reakcii.
Princípy stechiometrie uviedli v roku 1792 Jeremiáš Benjamín Richter (1762-1807), ktorý ho definoval ako vedu, ktorá meria kvantitatívne proporcie alebo masové vzťahy chemických prvkov, ktoré sú zapojené do reakčnej reakcie.
Pri chemickej reakcii dochádza k modifikácii látok, ktoré sa do nej zapojili. Zistilo sa, že sa konzumujú činidlá alebo reaktanty, aby spôsobili výrobky.
Môže vám slúžiť: železné kovyPočas chemickej reakcie existujú väzby medzi atómami, ako aj tvorba nových spojení; Ale počet atómov zapojených do reakcie zostáva nezmenený. To je známe ako zákon ochrany hmoty.
Základné princípy
Tento zákon naznačuje dva základné zásady:
-Celkový počet atómov každého typu je rovnaký v činidlách (pred reakciou) a v produktoch (po reakcii).
-Celkový súčet elektrických nábojov pred a po reakcii zostáva konštantný.
Je to preto, že počet subatomických častíc zostáva konštantný. Tieto častice sú neutróny bez elektrického náboja, protónov kladného zaťaženia (+) a negatívne (-) elektróny (-). Takže elektrický náboj sa počas reakcie nemení.
Chemická rovnica
Po tom, čo je uvedené vyššie, keď predstavujú chemickú reakciu prostredníctvom rovnice (napríklad hlavný obraz), musia sa základné princípy rešpektovať. Chemická rovnica používa symboly alebo reprezentácie rôznych prvkov alebo atómov a ako sú zoskupené do molekúl pred alebo po reakcii.
Ako príklad sa znova použije nasledujúca rovnica:
A+B2 => Ab2
Dolný index je číslo, ktoré je umiestnené na správnej časti prvkov (b2 a ab2) v spodnej časti, čo naznačuje počet atómov prvku prítomných v molekule. Toto číslo sa nedá zmeniť bez výroby novej molekuly, ktorá sa líši od pôvodného.
Stechiometrický koeficient (1, v prípade A a zvyšku druhu) je číslo, ktoré je umiestnené naľavo od atómov alebo molekúl, čo naznačuje ich počet zapojený do reakcie.
V chemickej rovnici, ak je reakcia nezvratná, je umiestnená jedna šípka, ktorá naznačuje význam reakcie. Ak je reakcia reverzibilná, existujú dve šípky v opačnom smere. Vľavo od šípok sú činidlá alebo reaktanty (A a B2), zatiaľ čo vpravo sú výrobky (AB2).
Výkyvný
Vyváženie chemickej rovnice je postup, ktorý umožňuje počet atómov chemických prvkov prítomných v činidlách s výrobkami.
Inými slovami, počet atómov každého prvku musí byť rovnaký na strane reagencií (pred šípkou) a na strane reakčných produktov (po šípke).
Hovorí sa, že keď je reakcia vyvážená, rešpektuje sa hmotnosť hmotnostného pôsobenia.
Preto je nevyhnutné vyvážiť počet atómov a elektrických nábojov na oboch stranách šípky v chemickej rovnici. Podobne aj súčet mas reagencií sa musí rovnať súčtu masy výrobkov.
Môže vám slúžiť: Zákon ideálnych plynov: vzorec a jednotky, aplikácie, príkladyV prípade reprezentovanej rovnice je už vyvážená (rovnaký počet A a B na oboch stranách šípky).
Experimenty, ktoré demonštrujú zákon
Spaľovanie kovu
Lavoiser, pozorujúci spaľovanie kovov, ako je olovo a cínu v uzavretých nádobách s obmedzeným príjmom vzduchu, opravil, že kovy boli pokryté kalcinovanou; A navyše, že hmotnosť kovu v určitom okamihu zahrievania bola rovná počiatočnej.
Ako kovový spaľovanie prírastku na váhe si Lavoiser myslel, že pozorovaná nadváha sa dá vysvetliť určitou hmotnosťou niečoho, čo je extrahované zo vzduchu počas spaľovania. Z tohto dôvodu cesto zostalo konštantné.
Tento záver, ktorý by sa mohol posudzovať s trochou solídneho vedeckého základu, nie je taký, vzhľadom na vedomie, že Lavoiser mal o existencii kyslíka v okamihu, keď vyhlásil svoj zákon (1785).
Uvoľňovanie kyslíka
Kyslík objavil Carl Willhelm Scheele v roku 1772. Následne ho Joseph Priesley objavil nezávisle a uverejnil výsledky svojho výskumu, tri roky predtým, ako Scheele uverejnil svoje výsledky o tom istom plyne.
Priesley oxid ortuť oxid a zdvihol plyn, ktorý spôsobil zvýšenie brilancie plameňa. Okrem toho zavedením myší do nádoby s plynom sa stali aktívnejšími. Priesley nazval tento plynový plyn.
Priesley oznámil svoje pozorovania Antoine Lavoiser (1775), ktorý opakoval svoje experimenty, čo dokazuje, že plyn bol vo vzduchu a vo vode. Lavoiser rozpoznal plyn ako nový prvok, ktorý mu dáva názov kyslíka.
Keď Lavoisier použil ako argument na vyjadrenie svojho zákona, že nadmerná hmota pozorovaná pri spaľovaní kovov bola spôsobená niečím, čo bolo extrahované zo vzduchu, myslel na kyslík, prvok, ktorý sa kombinuje s kovmi počas incilácie.
Príklady (praktické cvičenia)
Rozklad oxidu oxidu
Ak sa zahrieva 232,6 oxidu ortuti (HGO), rozkladá sa v ortuti (HG) a molekulárnom kyslíku (alebo2). Na základe zákona o zachovaní hmotnosti a atómových hmotností: (Hg = 206,6 g/mol) a (o = 16 g/mol), označujú hmotnosť Hg a O2 To sa formuje.
HGO => HG +O2
232,6 g 206,6 g 32 g
Výpočty sú veľmi priame, pretože presne jeden mol HGO sa rozkladá.
Spaľovanie horčíkovej pásky
 Páska horčíka. Zdroj: Capt. John Yossarian [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0) alebo gfdl (http: // www.GNU.Org/copyleft/fdl.html)], z Wikimedia Commons
Páska horčíka. Zdroj: Capt. John Yossarian [CC BY-SA 3.0 (https: // creativeCommons.Org/licencie/By-SA/3.0) alebo gfdl (http: // www.GNU.Org/copyleft/fdl.html)], z Wikimedia Commons Horčík 1,2 g sa spálil v uzavretej nádobe obsahujúcej 4 g kyslíka. Po reakcii bolo 3,2 g kyslíka bez reakcie. Koľko sa vytvorilo oxid horečnatý?
Môže vám slúžiť: Zmeny štátu: Typy a ich charakteristiky (s príkladmi)Prvá vec na výpočet je hmotnosť kyslíka, ktorá reagovala. Toto sa dá ľahko vypočítať pomocou odčítania:
Hmotnosť O2 ktoré reagovali = počiatočná hmotnosť alebo2 - záverečná hmotnosť O2
(4 - 3,2) g alebo2
0,8 g z O2
Na základe zákona o hromadnej ochrane môžete vypočítať vytvorenú hmotu MGO.
MGO hmotnosť = mg hmotnosť + hmotnosť O
1,2 g+0,8 g
2,0 g mgo
Hydroxid vápenatý
Hmotnosť 14 g oxidu vápenatého (CAO) reagovala s 3,6 g vody (H2O), ktorý bol úplne spotrebovaný pri reakcii na 14,8 g hydroxidu vápenatého, CA (OH)2:
Aké množstvo oxidu vápenatého reagovalo na tvorbu hydroxidu vápenatého?
Aké množstvo oxidu vápenatého skončil?
Reakcia môže byť schematizovaná podľa nasledujúcej rovnice:
CAO + H2O => CA (OH)2
Rovnica je vyvážená. Preto je v súlade so zákonom o hromadnej ochrane.
Hmotnosť CAO zapojená do reakcie = hmotnosť CA (OH)2 - hmotnosť h2Ani
14,8 g - 3,6 g
11,2 g CAO
Preto sa CAO, ktorý nereagoval (ten, ktorý zostal nad), vypočíta pomocou odčítania:
Sperantná hmotnosť CAO = hmotnosť prítomná v reakcii - hmotnosť, ktorá zasiahla v reakcii.
14 g Cao - 11,2 g Cao
2,8 g CAO
Oxid medi
Koľko oxidu medi (CUO) sa vytvorí, keď 11 g medi (Cu) s kyslíkom (alebo2)? Koľko kyslíka je potrebný pri reakcii?
Prvým krokom je vyváženie rovnice. Vyvážená rovnica je nasledovná:
2CU + O2 => 2Cuo
Rovnica je vyvážená, takže je v súlade so zákonom o zachovaní hromadnej ochrany.
Atómová hmotnosť Cu je 63,5 g/mol a ko -molekulová hmotnosť je 79,5 g/mol.
Musíte určiť, koľko COO sa tvorí z úplnej oxidácie 11 g Cu:
Cuo hmotnosť = (11 g Cu) ∙ (1 mol Cu/63,5 g Cu) ∙ (2 mol Cuo/2mol Cu) ∙ (79,5 g Cuo/mol Cuo)
Cuo Mass Formdated = 13,77 G
Preto rozdiel v hmotnostiach medzi CUO a CU poskytuje množstvo kyslíka zapojeného do reakcie:
Hmotnosť kyslíka = 13,77 g - 11 g
1,77 g o2
Tvorba chloridu sodného
Hmotnosť chlóru (CL2) 2,47 g sa reagovalo s dostatočným množstvom sodíka (NA) a vytvorilo sa 3,82 g chloridu sodného (NaCl). Koľko Na reagovalo?
Vyvážená rovnica:
2NA + CL2 => 2Nacl
Podľa zákona o hromadnej ochrane:
Na = NaCl Hmotnosť - CL Hmotnosť2
3,82 g - 2,47 g
1,35 g na
Odkazy
- Národný polytechnický inštitút. (s.F.). Zákon o zachovaní omše. Cgfie. Získané z: AEV.Cgfie.IPN.mx
- Zákon o zachovaní omše. Zotavené z: Thoughtco.com

