Joseph Thomson

- 1459
- 394
- Valentín Dula
 J.J. Thomson
J.J. Thomson Joseph John Thomson (1856-1940) Bol to britský chemik vysoký. V roku 1906 získal Nobelovu cenu vo fyzike.
Narodil sa 18. decembra 1856 v Anglickom okrese Cheetam, okrese Manchester. Tiež známy ako „j.J.„Thomson študoval inžinierstvo na Owens College, v súčasnosti súčasťou University of Manchester, a potom matematiky v Cambridge.
V roku 1890, j.J. Thomson sa oženil s Rose Elizabeth Paget, dcérou doktora Sir Edward George Paget, s ktorou mala dve deti: dievča menom Joan Paget Thomson a dieťa, George Paget Thomson.
Ten by sa stal slávnym vedcom, ktorý by v roku 1937 získal Nobelovu cenu vo fyzike za svoju prácu s elektrónmi.
Od mladého veku Thomson zameral svoje štúdie na štruktúru atómov, čím objavil existenciu elektrónov a izotopov, medzi mnohými inými príspevkami.
V roku 1906 získal Thomson Nobelovu cenu vo fyzike, „uznáva veľkú zásluhu o jeho teoretickom a experimentálnom výskume vedenia elektrickej energie prostredníctvom plynov“, ako ustanovila porota vo verdikte vyššie uvedenej ceny.
V roku 1908 bol vymenovaný za rytiera britskou korunou a pôsobil ako čestný profesor fyziky v Cambridge a Royal Institute v Londýne.
Zomrel 30. augusta 1940 vo veku 83 rokov v meste Cambridge v Anglicku. Fyzik bol pochovaný vo Westminsterskom opátstve, neďaleko hrobky Sira Isaaca Newtona.
Príspevky Josepha Thomsona do vedy a chémie
Odhalenie elektrónov
V roku 1897 J.J. Thomson objavil novú svetlú častice ako vodík, ktorý bol pokrstený „elektrón“.
Môže vám slúžiť: Stanovenie popola: metódy a príkladyVodík sa považoval za jednotku merania atómovej hmotnosti. Až do tej doby bol atóm najmenším rozdelením hmoty.
V tomto zmysle bol Thomson prvým, kto objavil negatívne zaťažené korpuskulárne subatomické častice.
Thomson Atomic Model
Thomsonov atómový model bol štruktúra, ktorú anglický fyzik pripisoval atómom. Pre vedca boli atómy kladnou guľou.
Vložili sa rovnomerne rozložené elektróny rovnomerne na tomto kladnom oblaku zaťaženia, to znamená neutralizovanie pozitívneho zaťaženia atómového cesta.
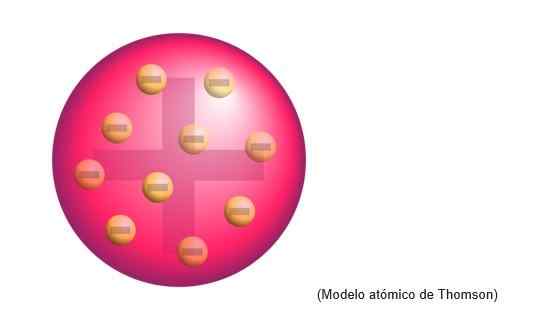
Tento nový model nahrádza rozpracovaného Daltonom a neskôr ho vyvrátil Rutherford, Thomsonov učeník v Cavendish Laboratories v Cambridge.
Oddelenie atómov
Thomson použil pozitívne alebo anodické lúče na oddelenie atómov od inej hmotnosti. Táto metóda mu umožnila vypočítať elektrinu transportovanú každým atómom a počet molekúl na kubický centimeter.
Fyzik, ktorý je schopný rozdeliť atómy rôznej hmoty a zaťaženia, objavil existenciu izotopov. Týmto spôsobom, so štúdiom pozitívnych lúčov, priniesol veľký pokrok smerom k hromadnej spektrometrii.
Objav izotopov
J.J. Thomson zistil, že neónové ióny mali rôzne masy, to znamená inú atómovú hmotnosť. Takto Thomson ukázal, že neón má dva podtypy izotopov, Neon-20 a Neon-22.
Izotopy, študované dodnes, sú atómami toho istého prvku, ale ich jadrá majú odlišné číslo hmotnosti, pretože sa skladajú z rôznych množstiev neutrónov v ich strede.
Pokusy s katódovými lúčmi
Katódové lúče sú elektrónové prúdy vo vákuových skúmavkách, to znamená sklenené trubice s dvoma elektródami, jedna pozitívna a jedna negatívna.
Môže vám slúžiť: chrómový hydroxid: štruktúra, vlastnosti, syntéza, použitieKeď sa záporná elektróda zahrieva, nazývaná tiež katódia, vyžaruje žiarenie, ktoré je nasmerované na pozitívnu elektródu alebo anódu, v priamej čiare, ak sa na tejto trase nevyskytuje žiadne magnetické pole.
Ak sú sklenené steny trubice pokryté fluorescenčným materiálom, prevrat katód proti tejto vrstve vytvára projekciu svetla.
Thomson študoval správanie katódových lúčov a dospel k záverom, že lúče sa šíria rovno.
Dospel tiež k záveru, že tieto lúče sa dajú odkloniť od ich trajektórie prítomnosťou magnetu, to znamená magnetického poľa. Okrem toho by lúče mohli pohybovať čepeľami s pevnosťou elektrónov cirkulujúcich, čo dokazuje, že elektróny mali hmotnosť.
J.J. Thomson zažil plyn vo vnútri trubice katódy, ale správanie elektrónov sa nemenilo. Podobne katódové lúče zahriali objekty, ktoré sa vkladajú na cestu medzi elektródami.
Na záver, Thomson ukázal, že katódové lúče mali svetlo, mechanické, chemické a tepelné účinky.
Rúrky s katódovým lúčom a ich svetlé vlastnosti boli transcendentálne pre následný vynález trubice televízie (CTR) a videokamier.
Hmotnostný spektrometer
J.J. Thomson vytvoril prvý prístup k Hmotnostný spektrometer. Tento nástroj umožnil štúdiu vedcov.
Pri tomto vyšetrovaní dospel k záveru, že katódové lúče boli zložené z negatívnych zaťaženia, ktoré sú vo vnútri atómov, a tak postulujú deliteľnosť atómu a vedú k vzniku elektrónovej postavy.
Môže vám slúžiť: kyselina maslová: vzorec, vlastnosti, riziká a použitiaPokroky v hmotnostnej spektrometrii pokračovali aj dodnes a vyvíjali sa v rôznych metódach na oddelenie elektrónov od atómov.
Okrem toho Thomson ako prvý navrhol Sprievodca prvou vlnou v roku 1893. Tento experiment pozostával zo šírenia.
Wave Guides by sa v budúcnosti, dokonca aj dnes, používajú s prenosom údajov a optickým vláknom.
Thomsonovo dedičstvo
Thomson (TH) bol založený ako jednotka hromadného zaťaženia v hmotnostnej spektrometrii, ktorú navrhli Cooks a Rockwood Chemicals, na počesť Thomsona.
Táto technika umožňuje určiť distribúciu molekúl látky podľa ich hmoty a uznať tým, ktoré sú prítomné vo vzorke hmoty.
Thomson Formula (TH):
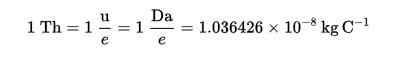
Vynikajúce diela
- Discarge elektriny prostredníctvom plynov, elektrina cez plyny (1900).
- Korpuskulárna teória hmoty, elektrón v chémii a spomienky a odrazy (1907).
- Za elektrónom (1928).
Odkazy
- Nobel Media AB (2014). J. Thomson - Biografický. Nobelová cena.orgán. Nobelová cena.orgán.
- Thomson, Joseph J., Elektrina prostredníctvom plynov. Cambridge, University Press, 1903.
- Menchaca Rocha, Arturo. Diskrétne kúzlo elementárnych častíc.
- Christen, Hans Rudolf, Základy všeobecnej a anorganickej chémie, zväzok 1. Barcelona, Španielsko. Vydania Reverté s.Do., 1986.
- Arzani, Aurora Cortina, Elementárna všeobecná chémia. Mexiko, redakcia Porúa, 1967.
- R. G. Kuchári, a. L. Rockwood. Rýchla komunikácia. Hmotnostné spektrom. 5, 93 (1991).

