Hydrofilné použitie pojmu, charakteristiky, príklady

- 3803
- 696
- Mgr. Pravoslav Mokroš
A hydrofyl alebo hydrofilný Je to molekulárny segment alebo zlúčenina, ktorá sa vyznačuje silnou afinitou k vode a polárnym rozpúšťadlám. Etymologicky to znamená „milovníci vody“, čo znamená, že hydrofilný bude schopný rozpustiť alebo efektívne interagovať s molekulami vody.
Preto hydrofilné látky majú tendenciu byť rozpustné alebo miešateľné s vodou. Avšak hydrofilita, to znamená jej afinita k vode a inému polárnemu rozpúšťadlu.
 Sklo je hydrofilný materiál, pretože sa ľahko zvlhčí a kvapky, ktoré sa na ňom ukladajú. Zdroj: pexels.
Sklo je hydrofilný materiál, pretože sa ľahko zvlhčí a kvapky, ktoré sa na ňom ukladajú. Zdroj: pexels. Hydrofilné povrchy sa teda ľahšie mokrujú alebo navlhčia ako hydrofóbne, tie, ktoré nenávidia vodu alebo ju odpudzujú. Prvá ploššia voda klesá do riadkov, zatiaľ čo druhá ich otočí a prominentne. Vizualizácia týchto kvapiek je jedným z hlavných faktorov na rozlíšenie hydrofilného materiálu od hydrofóbneho.
Koncept hydrofilnosti je nevyhnutný pre pochopenie povrchovej chémie, roztokov, rozhraní a amfifylického charakteru látok, ako sú proteíny a mastné kyseliny.
[TOC]
Použitie hydrofilného alebo hydrofilného pojmu
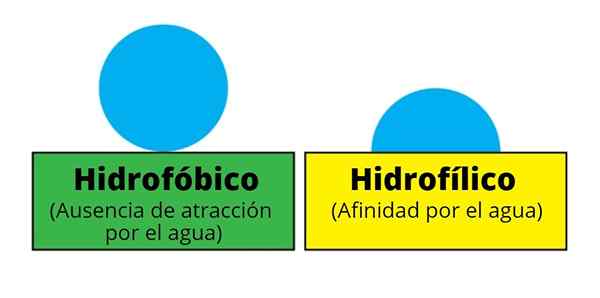
„Hydrofilné“ a „hydrofilné“ pojmy sú označené ako molekuly aj štrukturálne časti rovnakých. „Hydrofilný“ sa však používa hlavne na označenie akejkoľvek molekuly alebo zlúčeniny, ktorá má veľa afinity k vode.
Preto existuje hydrofilná alebo hydrofilná molekula, ak je jej afinita k vode veľmi vysoká podľa určitých úvah. Napríklad sacharóza je hydrofilná zlúčenina, ktorá je rovnaká ako tvrdenie, že je hydrofilná, pretože jej kryštály sa ľahko rozpúšťajú v akomkoľvek objeme vody.
Môže vám slúžiť: TritioDotknutá molekula môže prezentovať hydrofilné segmenty alebo časti, ktoré môžu byť vytvorené sýteným kostrom alebo jednoducho polárnou skupinou. Pokiaľ ide o skupinu, zvyčajne hovoríme, že ide o hydrofilnú skupinu, ktorá prispieva k hydrofilnosti molekuly alebo povrchu, ku ktorej patrí.
Zvyčajne sa „hydrofilný“ používa častejšie ako „hydrofilný“, pretože posledne uvedené si zvyčajne rezervuje viac ako čokoľvek pre molekuly alebo zlúčeniny, ktoré sú úplne hydrofilné; to znamená, že nemajú vo svojich molekulárnych štruktúrach hydrofóbne oblasti. To platí najmä vtedy, keď sú opísané makromolekuly alebo polymérne tuhé látky.
Charakteristiky hydrofilných látok
Kovalencia
Hydrofilné látky sú kovalentné zlúčeniny, čo znamená, že ich jednotky pozostávajú z molekúl a nie z iónových sietí. Preto, hoci soli majú tendenciu byť veľmi rozpustné vo vode, dokonca viac ako mnoho hydrofilných.
Na druhej strane nie všetky soli sú rozpustné vo vode, ako je chlorid strieborného, AGCL, a preto ich nemožno klasifikovať ako hydrofilný.
Polarita
Aby bola molekula hydrofilná, musí mať určitú polaritu. To je možné iba vtedy, ak majú polárne skupiny ako -oh, -sh, -nh vo svojej štruktúre2, -Cooh atď., aby prispievali k ich trvalému dipólovému momentu, a teda k ich hydrofilnosti.
Interakcie
Hydrofily sa rozpoznávajú nad ostatnými zlúčeninami kvôli ich schopnosti tvoriť vodíkové mosty s molekulami vody. Všimnite si, že vyššie uvedené polárne skupiny majú schopnosť darovať vodíny alebo ich prijať, aby vytvorili také mosty, ktoré sú špeciálnym typom dipólových dipolo interakcií.
Tuhé stavy
Hydrofily môžu byť plynné, kvapalné alebo tuhé látky, najbežnejšie sú tieto posledné dve.
Môže vám slúžiť: diferenciálny elektrónHydrofilné tekutiny sú miešateľné s vodou, takže keď je zmiešaná, nebudú vidieť dve fázy.
Medzitým sa hydrofilné tuhé látky rozpúšťajú vo vode alebo ich veľmi ľahko absorbujú; Ale okrem toho majú niektorí schopnosť namočiť sa alebo navlhčiť bez toho, aby sa vôbec rozpustili, pretože hoci je jeho povrch hydrofilný, nie je to celkom jej vnútorná hmota. Toto je prípad mnohých polymérnych materiálov, ako sú chemicky modifikované silikóny.
Hydrofilné povrchy
Hydrofilné povrchy sú vystavené štúdiám povrchovej chémie. Nie sú rozpustné vo vode, ale môžu zvlhčiť a vyrovnať kvapky vody, ktoré sa na ňu ukladajú. Je to preto, že majú externé hydrofilné skupiny, ktoré efektívne interagujú s molekulami vody.
Kvapka vody tvorí hydrofilným povrchom uhol kontaktu menší ako 90 °, čo sa rovná tvrdeniu, že predstavuje sploštený, malý sférický alebo okrúhly tvar.
To je teda, že sa kvapká konca rozširujúce sa a beží ako tekuté rady. Napríklad táto vlastnosť sa používa na zabránenie hmly poškodeného povrchu, pretože sa sotva dotkne kondenzuje voda a skĺzne nadol.
Naša pokožka je hydrofilná, pretože na nej majú kvapky tendenciu sploštenie a skĺznutie; s výnimkou prípadov, keď je to emecká olej alebo smotana. Potom budú vodné kvapky okrúhle a definované, pretože povrch sa dočasne stal hydrofóbne.
Príklady hydrofilných látok
Amoniak
Amoniak, NH3, Je hydrofilný, pretože jej molekula môže tvoriť niekoľko vodíkových mostov s vodou. Vďaka tomu je vo vode veľmi rozpustný v plynnom aj kvapalnom stave.
Kyselina
Kyselina oxalová, h2C2Ani4, Je to hydrofil.
Môže vám slúžiť: Petriho boxu: Charakteristika, funkcie, použite príkladyMetanol
Metanol, ch3Och, je to hydrofilné vďaka svojej skupine Oh.
Alkoholy
Alkoholy sú zvyčajne hydrofilné látky, pokiaľ ich uhlíková kostra nie je príliš veľká. Napríklad, 1-propanol a 2-propanol sú miešateľné s vodou, ale nestane sa to s 1-butanolom, ktorého miešateľnosť sa stáva nižšou kvôli svojmu uhlíkovému reťazcu s väčšou dĺžkou.
Škrob
Škrob je príkladom hydrofilného polyméru, pretože jeho glukózové jednotky majú viac skupín OH, s ktorými sa vodíkové mosty tvoria s molekulami vody.
Drevo
Drevo je hydrofilné a hoci sa nerozpúšťajú vo vode, rýchlo sa zvlhčuje, ak nie je ošetrené hydrofóbnymi povlakmi.
Bielkovina
Proteíny majú polárne skupiny veľmi príbuzné s vodou. Preto sú jeho interakcie s molekulami vody účinné. To však neznamená, že všetky proteíny sú rozpustné vo vode, pretože ich štruktúry (terciárna a kvartérna) zohrávajú základnú úlohu v uvedenom procese rozpustenia.
Pohár
Sklo je hydrofylové materiály, pretože hoci nepotýka molekúl, ale SIO siete2 Tri -dimenzionálne, ich atómy kyslíka môžu akceptovať vodíkové mosty. To je dôvod, prečo sa sklenené nádoby potia vo vlhkých prostrediach.
Odkazy
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. (10th Vydanie.). Wiley Plus.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Morrison a Boyd. (1987). Organická chémia. (Piate vydanie). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Hydrofilový. Zdroj: In.Wikipedia.orgán
- David L. Chváfka. (16. júla 2013). Vysvetlené: Hydrofóbne a hydrofilné. Obnovené z: noviniek.miznúť.Edu
- Gélové. (2020). Hydrofilné materiály. Získané z: GeLest.com
- Ahmad Darem a kol. (5. september 2018). Hydrofilné a hydrofóbne materiály a aplikácie. Taylor & Francis online. doi.org/10.1080/15567036.2018.1511642
- « Vojnové zázemie Chaco, príčiny, vývoj, dôsledky
- Život načítava koncept, charakteristiky, príklady »

