Štruktúra glykogénu, syntéza, degradácia, funkcie
- 800
- 170
- Valentín Dula
On Glykogén Je to úložný uhľohydrát väčšiny cicavcov. Sacharidy sa bežne nazývajú cukry a tieto sa klasifikujú podľa počtu odpadu spôsobených hydrolýzou (monosacharidy, disacharidy, oligosacharidy a polysacharidy))))).
Monosacharidy sú najjednoduchšie uhľohydráty, ktoré sú klasifikované podľa počtu uhlíkov obsiahnutých v ich štruktúre. Potom existujú Triosas (3C), Tetrosas (4C), Pentosas (5c), hexozózne (6c), heptosáza (7c) a Octosas (8c).
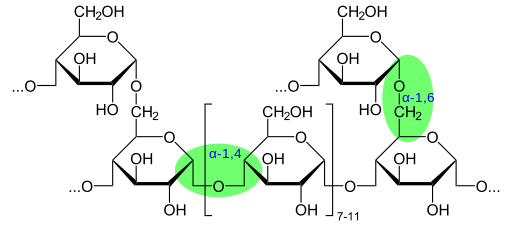
 Chemická štruktúra glykogénu vykazujúce glykozidické väzby (zdroj: glykogen.SVG: Neurotoger Derivative Work: Marek M [Public Domain] Via Wikimedia Commons)
Chemická štruktúra glykogénu vykazujúce glykozidické väzby (zdroj: glykogen.SVG: Neurotoger Derivative Work: Marek M [Public Domain] Via Wikimedia Commons) Podľa prítomnosti skupiny aldehydov alebo skupiny Cetona sú tieto monosacharidy tiež klasifikované ako aldies alebo ketosas.
Disacharidy spôsobujú hydrolýzu, dva jednoduché monosacharidy, zatiaľ čo oligosacharidy produkujú 2 až 10 jednotiek monosacharidov a polysacharidov viac ako 10 monosacharidov.
Glykogén je z biochemického hľadiska polysacharid zložený z rozvetvených reťazcov šesť -karbonového aldózy, to znamená hexóza známa ako glukóza. Graficky môže byť znázornený glykogén ako strom glukózy. Toto sa tiež nazýva Animal Starch.
Glukóza v rastlinách sa ukladá ako škrob a zvieratá ako glykogén, ktorý sa ukladá predovšetkým v pečeni a svalovom tkanive.
V pečeni môže glykogén stanoviť 10% svojej hmoty a 1% svalovej hmoty. Rovnako ako u 70 kg muža, pečeň váži asi 1800 g a svaly asi 35 kg, celkové množstvo svalového glykogénu je oveľa väčšie ako pečeň.
[TOC]
Štruktúra
Molekulová hmotnosť glykogénu môže dosiahnuť 108 g/mol, čo zodpovedá molekulám glukózy 6 x 105. Glykogén sa skladá z viacerých rozvetvených reťazcov a-d-glykózy. Glukóza (C6H12O6) je aldohexosa, ktorá môže byť reprezentovaná lineárnym alebo cyklickým spôsobom.
Glykogén má veľmi rozvetvenú a kompaktnú štruktúru s reťazcami 12 až 14 glukózovým odpadom vo forme a-d-glukózy, ktoré sú spojené s a- (1 → 4) glukozidnými väzbami. Výsledky reťazca sú tvorené a- (1 → 6) glukozidnými väzbami.
Glykogén, rovnako ako škrob, ktorý sa požiti v strave, poskytuje väčšinu uhľohydrátov, ktoré telo potrebuje. V čreve sa tieto polysacharidy degradujú hydrolýzou a potom sa absorbujú smerom k obehovému torrentu hlavne ako glukóza.
Tri enzýmy: ß-amyláza, a-amyláza a amylo-a- (1 → 6) -glukozidáza sú zodpovedné za degradáciu čreva glykogénu aj škrobu.
A-amyláza náhodne hydrolyzuje a- väzby (1 → 4) bočných reťazcov glykogénu a škrobu, a preto dostáva názov endogysidázy. Ss-amyla je exogliklicozidáza, ktorá uvoľňuje ß-maltózový dímeros, ktorý lámal a- (1 → 4) glykozidné väzby z koncov vonkajších reťazcov bez toho, aby dosiahli následky následkom dôsledkov.
Vzhľadom na skutočnosť, že ani ß-amyláza, ani a-amyláza degradujú vetvy, konečný produkt jej pôsobenia je vysoko rozvetvená štruktúra asi 35 až 40 glukózových zvyškov, ktoré sa nazývajú limit dextrine.
Limitný dextrín sa konečne hydrolyzuje v bodoch vetvy, ktoré majú väzby a- (1 → 6) cez amyle-a- (1 → 6) -glukozidázu, tiež známe ako „hanobý“ enzým. Reťazce uvoľnené týmto defloatom sú po degradovaných ß-amyláze a a-amyláze.
Keď požitý glykogén vstupuje ako glukóza, ten, ktorý sa nachádza v tkanivách, musí syntetizovať organizmus z glukózy.
Môže vám slúžiť: Puríny: Charakteristiky, štruktúra, funkcieSyntéza
Syntéza glykogénu sa nazýva glykogenéza a prebieha najmä vo svale a pečeni. Glukóza, ktorá vstupuje do organizmu s diétou, prechádza do obehového torrentu a odtiaľ vo vnútri buniek, kde je okamžite fosforylovaný enzýmom nazývaným glykoquináza.
Glukoquináza fosforyyyl až glukóza v uhlíku 6. ATP poskytuje pre túto reakciu fosfor a energiu. Výsledkom je, že sa vytvorí glukóza 6-fosfát a uvoľní sa ADP. Potom sa 6-fosfát glukóza stáva glukózou 1-fosfát pôsobením fosfoglukomutázy, ktorá bahí fosfor z polohy 6 do polohy 1.
1-fosfát glukóza je aktivovaná pre syntézu glykogénu, čo znamená účasť súboru troch ďalších enzýmov: UDP-glykózová pyrofosforyláza, syntetický glykogén a amilo- (1,4 → 1.6) -glicozyltransferáza.
Glukóza-1-fosfát, spolu s trfosfátovým uridínom (UTP, nukleozidom uridín trifosfátu) a pôsobením UDP-glykóz-pyrofosforylasu, tvoria komplex difosfát-glukóz. V procese sa hydrolyzuje pyrofosfátový ión.
Potom syntetizovaný glykogénový enzým tvorí glukozidickú väzbu medzi C1 komplexu GLC UDP a C4 glugénového terminálneho zvyšku a UDP UDP sa uvoľňuje z komplexu glukózy aktivovaného UDP UDP. Aby sa táto reakcia vyskytla, musí existovať existujúca molekula glykogénu nazývaná „primárny glykogén“.
Primordiálny glykogén sa syntetizuje na primingovom proteíne, glykogeníne, ktorý má 37 kDa a glysila v tyrozínovom zvyšku pomocou komplexu UDP GLC. Odtiaľ sú spojené s a-d-glukózovým odpadom s 1 → 4 odkazmi a tvorí sa malý reťazec, na ktorom pôsobí syntezáza glykogén.
Akonáhle sa počiatočný reťaz spojí najmenej 11 glukózových zvyškov, vetvenie alebo amile enzým- (1,4 → 1,6) -glicozyltransferáza prenesie reťazový kus glukózového odpadu 6 alebo 7 do susedného reťazca v polohe 1 → 6, ktorý stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu, ktorá stanovuje vetvu reťazový kus 6 alebo 7 glukózového odpadu do susedného reťazca v polohe 1 → 6 bod. Takto postavená molekula glykogénu rastie pridaním glukózových jednotiek s glykozidnými väzbami 1 → 4 a viac dôsledkov.
Degradácia
Degradácia glykogénu sa nazýva glukogenolýza a nie je rovnocenná s opačnou cestou jeho syntézy. Rýchlosť tejto trasy je obmedzená rýchlosťou reakcie katalyzovanej fosforylázovou glykogénom.
Glykogén fosforylázy je zodpovedný za rozdelenie (fosforolýza) odkazov 1 → 4 z glykogénových reťazcov, uvoľňovanie glukózy 1-fosfátu. Enzymatický účinok sa začína na koncoch najvzdialenejších reťazcov a sú odstránené postupne, až kým na každej strane dôsledkov zostávajú 4 zvyšky glukózy 4 glukózy.
Potom ďalší enzým, a- (1 → 4) → a- (1 → 4) Glucano prenosy, opúšťa bod vetvy exponovaného prenosom trisacharidovej jednotky z jednej vetvy do druhej. To umožňuje hydrolys amilo- (1 → 6) -glukozidázy (neúnosný enzým). Kombinované pôsobenie týchto enzýmov končí úplne rozdelenie na glykogén.
Pretože počiatočná reakcia fosfomutázy je reverzibilná, 6-fosfátová glukóza sa môže tvoriť z glukózových zvyškov 1-fosfátu rozdelených z glykogénu. V pečeni a obličkách, ale nie vo svale, je enzým, glukóza-6-fosfatáza, schopná zhromažďovať sa na 6-fosfátovú glukózu a premeniť ju na voľnú glukózu.
Môže vám slúžiť: FotolýzaDefosforylovaná glukóza sa môže šíriť do krvi, a to tak, ako sa pečeňová glykogenolýza odráža vo zvýšení hodnôt glukózy v krvi (glykémia).
Regulácia syntézy a degradácie
Syntézy
Tento proces sa uplatňuje na dvoch základných enzýmoch: glykogén syntezázy glykogénu a fosforylázy, takže keď je jeden z nich aktivovaný, druhý je v jeho neaktívnom stave. Táto regulácia bráni proti protichodným reakciám syntézy a degradácie súčasne.
Aktívna forma a neaktívna forma oboch enzýmov je veľmi odlišná a interkonverzia aktívnych a neaktívnych foriem fosforylázy a syntetického glykogénu je vystavená prísnej hormonálnej kontrole.
Adrenalín je hormón, ktorý sa uvoľňuje z drene nadobličiek a glukagón je ďalší, ktorý sa vyskytuje v endokrinnej časti pankreasu. Endokrinná pankreas produkuje inzulín a glukagón. Langerhans Islets α sú tie, ktoré syntetizujú glukagón.
Adrenalín a glukagón sú dva hormóny, ktoré sa uvoľňujú, keď je potrebná energia v reakcii na zníženie hladín glukózy v krvi. Tieto hormóny stimulujú aktiváciu fosforylasového glykogénu a inhibujú glykogén syntézy, čím stimulujú glykogenolýzu a inhibujú glykogenézu.
Zatiaľ čo adrenalín uplatňuje svoje pôsobenie na sval a pečeň, glukagón pôsobí iba na pečeň. Tieto hormóny sú spojené s špecifickými membranálnymi receptormi v bielej bunke, ktorá aktivuje ademilát cykly.
Aktivácia cyklázovej adenylátu začína enzymatický vodopád, ktorý na jednej strane aktivuje proteinquinázu závislú od AMPC, ktorý neaktívnym až syntetickým glykogénom a aktivuje fosforylázu glykogénu fosforyláciou (priamo a nepriamo).
Kostrový sval má ďalší mechanizmus na aktiváciu fosforylázového glykogénu prostredníctvom vápnika, ktorý sa uvoľňuje v dôsledku depolarizácie svalovej membrány na začiatku kontrakcie.
Degradácia
Enzymatické vodopády opísané vyššie, čím sa zvyšujú hladiny glukózy a keď dosiahnu určitú úroveň, aktivuje sa glykogenéza a glukogenolýza je inhibovaná, tiež inhibuje ďalšie uvoľňovanie adrenalínu a glukagónu.
Glykogenéza je aktivovaná aktiváciou fosforylázy fosfatázy, enzýmu, ktorý reguluje syntézu glykogénu niekoľkými mechanizmami, čo naznačuje inaktiváciu kinázovej fosforylázy a fosforylázy a, ktorá je syntézou glykogénovej inhibície.
Inzulín podporuje vstup glukózy do svalových buniek, čím sa zvyšuje hladiny 6-fosfátovej glukózy, čo stimuluje defosforyláciu a aktiváciu syntézy glykogen. Začína sa teda syntéza a degradácia glykogénu je inhibovaná.
Funkcia
Sval glykogén predstavuje energetickú rezervu pre sval, ktorý, rovnako ako rezervné tuky, umožňuje svalovi plniť svoje funkcie. Ako zdroj glukózy sa používa svalové glykogén počas cvičenia. Tieto rezervácie sa zvyšujú pri telesnej školení.
V pečeni predstavuje glykogén tiež dôležitý zdroj rezerv pre funkcie orgánu, ako aj pre príspevok glukózy k zvyšku tela.
Táto funkcia glykogénu pečene je spôsobená skutočnosťou, že pečeň obsahuje 6-fosfatázovú glukózu, enzým schopný eliminovať skupinu 6-fosfátu fosfátu a premeniť ju na voľnú glukózu. Voľná glukóza, na rozdiel od fosforylovanej glukózy, sa môže šíriť cez hepatocytovú membránu (pečeňové bunky).
Môže vám slúžiť: sporulácia: v rastlinách, v húb a baktériáchTakto môže pečeň poskytnúť glukózu na obeh a udržiavať stabilné hladiny glukózy, dokonca aj v predĺžených podmienkach pôstu.
Táto funkcia má veľký význam, pretože mozog sa vyživuje takmer výlučne z glukózy v krvi, takže závažná hypoglykémia (veľmi nízka koncentrácia glukózy v krvi) môže spôsobiť stratu vedomostí.
Súvisiace choroby
Choroby súvisiace s glykogénom dostávajú generický názov „choroby ukladania glykogénu“.
Tieto choroby tvoria skupinu dedičných patológií charakterizovaných ložiskom v tkanivách abnormálnych množstiev alebo typov glykogénu.
Väčšina chorôb na ukladanie glykogénu je spôsobená deficitom genetického povahy ktoréhokoľvek z enzýmov zapojených do metabolizmu glykogénu.
Sú klasifikované do ôsmich typov, z ktorých väčšina má svoje vlastné mená a každá z nich je produkovaná iným enzymatickým deficitom. Niektoré sú smrteľné vo veľmi raných štádiách života, zatiaľ čo iné sú sprevádzané svalovou slabosťou a deficitom počas cvičenia.
Vynikajúce príklady
Niektoré z najvýznamnejších chorôb súvisiacich s glykogénom sú nasledujúce:
- Von Gierkeho choroba alebo ochorenie skladovania glykogénu typu I sa vyrába deficitom glukózy 6-fosfatázy v pečeni a obličkách.
Vyznačuje sa abnormálnym rastom pečene (hepatomegália) v dôsledku prehnanej akumulácie glykogénu a hypoglykémie, pretože pečeň nie je schopná zabezpečiť glukózu do obehu. Pacienti s týmto stavom majú zmeny rastu.
- Pompe alebo ochorenie typu II je spôsobené a-deficitom (1 → 4) -glucano 6-glykozyltransferá v pečeni, srdcových a kostrových svaloch. Táto choroba, ako je Andersen alebo typ IV, je smrteľná pred dvoma rokmi života.
- Mcardle alebo ochorenie typu V má deficit svalovej fosforylázy a je sprevádzaný svalovou slabosťou, zníženou toleranciou cvičenia, abnormálnou akumuláciou svalového glykogénu a neprítomnosti laktátu počas cvičenia počas cvičenia.
Odkazy
- Bhattacharya, K. (2015). Vyšetrovanie a riadenie chorôb na ukladanie glykogénu v pečeni. Translačná pediatria, 4(3), 240-248.
- Dagli, a., Sentner, C., & Weinstein, D. (2016). Glykogénové ukladanie choroby typu III. Recenzie génov, 1-16.
- Guyton, a., & Hall, J. (2006). Učebnica lekárskej fyziológie (11. vydanie.). Elsevier Inc.
- Mathews, C., Van Holde, K., & Ahern, K. (2000). Biochémia (3. vydanie.). San Francisco, Kalifornia: Pearson.
- McKiernan, P. (2017). Patobiológia túžby z ukladania glykogénu pečene. Curs Patobiol Rep.
- Murray, r., Bender, D., Botham, K., Kennelly, P., Rodwell, V., & Weil, P. (2009). Harperova ilustrovaná biochémia (28. ED.). McGraw-Hill Medical.
- Nelson, D. L., & Cox, M. M. (2009). Lehninger princípy biochémie. Vydanie omega (5. vydanie.).
- Rawn, J. D. (1998). Biochémia. Burlington, Massachusetts: Vydavatelia Neil Patterson.
- Tarnopolsky, m. Do. (2018). Myopatie súvisiace s poruchami metabolizmu glykogénu. Neuroterapeutika.
- « História argónovej, štruktúra, vlastnosti, použitie
- Bijektívna funkcia Čo je, ako sa to robí, príklady, cvičenia »

