Oxidačné fosforylačné štádiá, funkcie a inhibítory
- 1446
- 142
- Tomáš Mydlo
Ten Oxidačná fosforylácia Je to proces, v ktorom sú molekuly ATP syntetizované z ADP a PJo (Anorganický fosfát). Tento mechanizmus sa vykonávajú baktériami a eukaryotickými bunkami. V eukaryotických bunkách sa fosforylácia vykonáva v mitochondriálnej matrici ne -fotosyntetických buniek.
Výroba ATP je riadená prenosom elektrónov z koenzýmov NADH alebo FADH2 tiež2. Tento proces predstavuje najväčšiu výrobu energie v bunke a je odvodený od degradácie uhľohydrátov a tukov.
 Zdroj: Robot8a [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)]
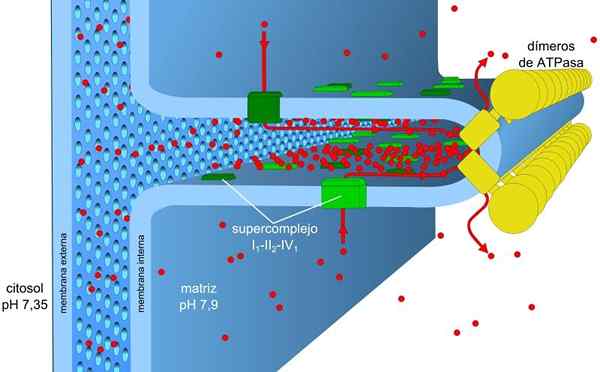
Zdroj: Robot8a [CC BY-SA 4.0 (https: // creativeCommons.Org/licencie/By-SA/4.0)] Energia uložená v zaťažení a gradientoch pH, tiež známa ako protonická motorická sila, umožňuje vykonanie tohto procesu. Generovaný gradient protónov spôsobuje, že vonkajšia časť membrány bude mať kladnú záťaž v dôsledku koncentrácie protónov (H+) a mitochondriálna matrica je negatívna.
[TOC]
Kde dochádza k oxidačnej fosforylácii?
Elektrónové transporty a oxidačné fosforylačné procesy sú spojené s membránou. V prokaryotoch sa tieto mechanizmy vykonávajú cez plazmovú membránu. V eukaryotických bunkách sú spojené s mitochondriou membránou.
Počet mitochondrií nachádzajúcich sa v bunkách sa líši podľa typu bunky. Napríklad u erytrocytov cicavcov chýba tieto organely, zatiaľ čo iné typy buniek, ako sú svalové bunky, môžu mať milióny z nich.
Mitochondriálna membrána pozostáva z jednoduchej vonkajšej membrány, trochu zložitejšej vnútornej membrány a v strede z intermembranálneho priestoru, kde sa nachádza mnoho enzýmov závislých od ATP.
Vonkajšia membrána obsahuje proteín nazývaný porina, ktorý tvorí kanály pre jednoduchú difúziu malých molekúl. Táto membrána je zodpovedná za udržiavanie štruktúry a tvaru mitochondrií.
Vnútorná membrána má väčšiu hustotu a je bohatá na proteín. Je tiež vodotesná pre molekuly a ióny, takže na ich kríženie potrebujú intermembranálne proteíny, ktoré ich transportujú.
V matrici sa rozširujú záhyby vnútornej membrány a vytvárajú hrebene, ktoré mu umožňujú mať v malom objeme veľkú plochu.
Bunková energia centrálna
Mitochondrie sa považujú za centrum bunkovej energie. V ňom sú enzýmy zapojené do procesov cyklu kyseliny cytrovej, oxidácie mastných kyselín a redoxných enzýmov a proteínov elektrónového transportu a fosforylácie PhD.
Koncentračný gradient protónov (gradient pH) a gradient zaťaženia alebo elektrického potenciálu vo vnútornej membráne mitochondrií sú príčinou protevnej motorickej sily. Malá priepustnosť vnútornej membrány pre ióny (iné ako H+) umožňuje mitochondriám mať stabilný gradient napätia.
Elektronický transport, protóny čerpanie a ATP získanie súčasne v mitochondriách vďaka protonickej motorickej sile. Gradient pH udržuje kyslé podmienky v intermembránovej a mitochondriálnej matrici s alkalickými podmienkami.
Za každé dva elektróny prenesené do O2 Približne 10 protónov je čerpaných membránou, čím vytvára elektrochemický gradient. Energia oddelená v tomto procese sa vyrába postupne prechodom elektrónov cez dopravný reťazec.
Etapa
Energia uvoľnená počas oxidových redukčných reakcií NADH a FADH2 Je značne vysoký (asi 53 kcal/mol pre každú dvojicu elektrónov), aby sa použil pri výrobe molekúl ATP, musí sa postupne produkovať s priechodom elektrónov cez transportéry.
Sú organizované v štyroch komplexoch umiestnených vo vnútornej mitochondriálnej membráne. Spojenie týchto reakcií na syntézu ATP sa vykonáva v piatom komplexe.
Môže vám slúžiť: B lymfocyty: Charakteristiky, štruktúra, funkcie, typyPrepravná reťazec
NADH prenáša niekoľko elektrónov, ktoré vstupujú do komplexu I elektrónového transportného reťazca. Elektróny sa prenášajú do mononukleotidu Flaviny a potom do ubikinónu (koenzým Q) cez dopravník na železo-cukr. Tento proces uvoľňuje veľké množstvo energie (16,6 kcal/mol).
Ubquinona transportuje elektróny cez membránu do komplexu III. V tomto komplexe elektróny prechádzajú cytochrómami B a C1 Vďaka transportérovi železnému cukru.
Z komplexu III elektróny prechádzajú do komplexu IV (cytochróm C oxidáza), prenesené jeden cytochróm C (proteín periférnej membrány). V komplexe IV elektróny prechádzajú cez pár medených iónov (Cudo2+), potom do cytochrómu Cdo, potom do iného páru medených iónov (cub2+) a z toho do cytochrómu do3.
Nakoniec sa elektróny prenášajú na O2 čo je posledný akceptor a tvorí molekulu vody (h2O) pre každú dvojicu prijatých elektrónov. Priechod elektrónov z komplexu IV do O2 Generuje tiež veľa voľnej energie (25,8 kcal/mol).
Sukcinato coq reduktáza
Komplex II (sukcinácia CoQ reduktázy) prijíma dvojicu elektrónov z cyklu kyseliny citrónovej v dôsledku oxidácie sukcinátovej molekuly fumarátu. Tieto elektróny sa prenášajú na výstrelok a potom prechádzajú cez skupinu železo-azufre do ubichinony. Z tohto koenzýmu idú do komplexu III a sledujú cestu opísanú skôr.
Energia uvoľnená v reakcii na prenos elektrónov na výstrelok nestačí na zvýšenie protónov cez membránu, takže v tomto kroku reťazca neexistuje žiadna protevná motorická sila, a preto FADH poskytuje menej H+ ako Nadh.
Energetické spojenie alebo prenos
Energia vytvorená v predtým opísanom procese prenosu elektrónov by sa mala použiť na produkciu ATP, reakcia katalyzovaná ATP syntázou alebo komplexným enzýmom V. Ochrana takejto energie je známa ako energetické spojenie a mechanizmus je ťažké charakterizovať.
Bolo opísaných niekoľko hypotéz na opis tejto energetickej prenosu. Najlepšie akceptované je hypotéza chemosmotického spojenia, opísaná nižšie.
Chemosmotické spojenie
Tento mechanizmus navrhuje, aby energia použitá na syntézu ATP pochádza z protonického gradientu v bunkových membránach. Tento proces zasahuje do mitochondrií, chloroplastov a baktérií a je spojený s transportom elektrónov.
Komplexy elektronickej transportu I a IV pôsobia ako protónové čerpadlá. Trpia konformačnými zmenami, ktoré im umožňujú pumpovať protóny do intermembranského priestoru. V komplexe IV pre každú dvojicu elektrónov sú dva protóny čerpané mimo membrány a ďalšie dva zostávajú v matrici tvoriacej H2Ani.
Ubquinona v komplexe III prijíma protóny komplexov I a II a oslobodzuje ich mimo membrány. Komplexy I a III umožňujú priechod štyroch protónov pre každý pár transportných elektrónov.
Mitochondriálna matrica má nízku koncentráciu protónov a negatívny elektrický potenciál, zatiaľ čo intermembranálny priestor predstavuje inverzné podmienky. Tok protónov touto membránou znamená elektrochemický gradient, ktorý ukladá potrebnú energiu (± 5 kcal/mol protón) na syntézu ATP.
Syntéza ATP
Enzým syntetázy ATP je piaty komplex zapojený do oxidačnej fosforylácie. Je zodpovedný za využitie energie elektrochemického gradientu na vytvorenie ATP.
Tento transmembraálny proteín pozostáva z dvoch zložiek: f0 a f1. Komponent f0 umožňuje návrat protónov do mitochondriálnej matrice fungujúce ako kanál a f1 katalyzuje syntézu ATP prostredníctvom ADP a PJo, využívanie energie uvedeného návratu.
Môže vám slúžiť: membránové dopravníky proteíny: Funkcie a typyProces syntézy ATP vyžaduje štrukturálnu zmenu v F1 a zostavenie komponentov f0 a f1. Translokácia protónov prostredníctvom f0 Spôsobuje konformačné zmeny v troch podnetách f1, čo umožňuje pôsobiť ako rotačný motor, usmerňuje tvorbu ATP.
Podjednotka, ktorá je zodpovedná za spojenie ADP s PJo prechádza zo slabého stavu (L) do aktívneho (T). Keď sa vytvorí ATP, druhá podjednotka prechádza do otvoreného stavu (O), ktorý umožňuje uvoľňovanie tejto molekuly. Po prepustení ATP prechádza táto podjednotka z otvoreného stavu do neaktívneho stavu (L).
Molekuly ADP a PJo Pripojia sa k podjednotke, ktorá prešla zo štátu alebo štátu L.
Produkty
Elektrónový dopravný reťazec a fosforylácia produkujú molekuly ATP. Oxidácia NADH produkuje asi 52,12 kcal/mol (218 kJ/mol) voľnej energie.
Globálna reakcia na oxidáciu NADH je:
NADH+1⁄2 alebo2 +H+ ↔ h2O+NAD+
Prenos elektrónov z NADH a FADH2 Vyskytuje sa prostredníctvom niekoľkých komplexov, čo umožňuje, aby sa zmenila voľnej energie ° ° rozdelila na menšie „balíčky“, ktoré sú spojené s syntézou ATP.
Oxidácia molekuly NADH generuje syntézu troch molekúl ATP. Zatiaľ čo oxidácia molekuly FADH2 Je pripojený k syntéze dvoch ATP.
Tieto koenzýmy pochádzajú z procesov glykolýzy a cyklu kyseliny citrónovej. Pre každú degradovanú molekulu glukózy končí 36 alebo 38 molekúl ATP, v závislosti od umiestnenia buniek. V mozgu a kostrovom svale sa produkuje 36 ATP, zatiaľ čo 38 ATP sa vytvára vo svalovom tkanive.
Funkcia
Všetky organizmy, jednobunkové a mnohobunkové, potrebujú v bunkách minimálnu energiu na vykonávanie procesov v nich a zase udržiavajú životne dôležité funkcie v úplnom tele.
Metabolické procesy si vyžadujú vykonávanie energie. Väčšina použiteľnej energie sa získa degradáciou uhľohydrátov a tukov. Táto energia je odvodená z procesu oxidačnej fosforylácie.
Oxidačná fosforylácia
Rýchlosť použitia ATP v bunkách, riadi ich syntézu a následne v dôsledku spojenia oxidačnej fosforylácie pomocou elektrónového transportného reťazca tiež všeobecne reguluje rýchlosť elektronickej transportu.
Oxidačná fosforylácia má prísnu kontrolu, ktorá zaisťuje, že ATP sa nevytvára rýchlejšie, ako sa spotrebuje. V procese elektrónovej transportu sú určité kroky a spojená fosforylácia, ktorá reguluje mieru výroby energie.
Koordinovaná kontrola výroby ATP
Hlavné trasy výroby energie (bunky ATP) sú glykolýza, cyklus kyseliny citrónovej a oxidačnej fosforylácie. Koordinovaná kontrola týchto troch procesov reguluje syntézu ATP.
Riadenie fosforylácie pomocou pomeru hmotností ATP závisí od presného príspevku elektrónov v dopravnom reťazci. To zase závisí od vzťahu [NADH]/[NAD+], ktoré je zachované zvýšené pôsobením glykolýzy a cyklu kyseliny citrónovej.
Táto koordinovaná kontrola sa vykonáva reguláciou kontrolných bodov glykolýzy (citrát inhibované PFK) a cyklu kyseliny cytrovej (dehydrogenáza pyruvát, citrate cuteázy, stitchitrátdehydrogenáza a a-zeglutaráte dehydrogenáza).
Ovládanie akceptorom
IV komplex (cytochróm C oxidáza) je enzým regulovaný jedným zo substrátov, to znamená, že jeho aktivita je regulovaná zníženým cytochrómom C (C (C (2+), ktorý je zase v rovnováhe so vzťahom koncentrácií medzi [NADH]/[NAD+] a pomer hmotnostného pôsobenia [ATP]/[ADP] + [PJo].
Môže vám slúžiť: Tón: Charakteristiky a funkcieČím vyššie je [NADH]/[NAD+] a znížte [ATP]/[ADP]+[PJo], viac koncentrácie bude cytochróm [c2+] a väčšia bude aktivita komplexu IV. Toto sa interpretuje napríklad, ak porovnávame organizmy s rôznymi odpočinkovými činnosťami a vysokou aktivitou.
U jednotlivca s vysokou fyzickou aktivitou, konzumácia ATP, a teda jej hydrolýza na ADP + PJo Bude to veľmi vysoké, čím sa vytvorí rozdiel v mierovom pomere, ktorý spôsobuje zvýšenie [c2+a preto zvýšenie syntézy ATP. U odpočinkového jednotlivca nastane opačná situácia.
Nakoniec sa rýchlosť oxidačnej fosforylácie zvyšuje s koncentráciou ADP v mitochondriách. Táto koncentrácia závisí od translokátorov ADP-ATP zodpovedných za transport adenínových nukleotidov a pJo Z cytosolu na mitochondriálnu matricu.
Dekakoplantáty
Oxidačná fosforylácia je ovplyvnená určitými chemickými činidlami, ktoré umožňujú elektronický transport pokračovať bez fosforylácie ADP, pričom oddeľuje výrobu a ochranu energie.
Tieto látky stimulujú rýchlosť spotreby kyslíka mitochondrie v neprítomnosti ADP, čo tiež spôsobuje zvýšenie hydrolýzy ATP. Konajú odstránením sprostredkovateľa alebo prerušením stavu energie z reťazca elektrónového dopravníka.
2,4-dinitrofenol, slabá kyselina, ktorá prechádza mitochondriálnymi membránami, je zodpovedná za rozptyl protónov, pretože sa k nim spájajú na kyslej strane a uvoľňujú ich na základnej strane.
Táto zlúčenina sa použila ako „štíhla tabletka“, pretože sa zistilo, že spôsobila zvýšenie dýchania, a preto zvýšenie rýchlosti metabolizmu a súvisiaceho úbytku hmotnosti. Ukázalo sa však, že jeho negatívny účinok by mohol dokonca spôsobiť smrť.
Rozptyl protonického gradientu vytvára teplo. Bunky hnedého tukového tkaniva používajú oddelenie, hormonálne kontrolované, na výrobu tepla. Hibernácie cicavcov a novorodencov, ktorí nemajú vlasy, pozostávajú z tohto tkaniva, ktoré im slúži ako druh tepelnej prikrývky.
Inhibítory
Inhibičné zlúčeniny alebo činidlá bránia tak spotrebe alebo2 (elektronický transport), ako je súvisiaca oxidačná fosforylácia. Títo agenti sa vyhýbajú tvorbe ATP pomocou energie vyrobenej pri elektronickej preprave. Preto sa dopravný reťazec zastaví, pretože taká spotreba energie nie je usporiadaná.
Oligomicín antibiotikum funguje ako inhibítor fosforylácie v mnohých baktériách, pričom bráni stimulácii ADP syntézy ATP ADP.
Existujú aj ionoforistické látky, ktoré tvoria komplexy rozpustné v tukoch s katiónmi, ako sú K+ a na+, a prejsť mitochondriálnou membránou s týmito katiónmi. Mitochondrie potom využívajú energiu vyrobenú v elektronickom transporte do katiónov na čerpanie namiesto syntetizovania ATP.
Odkazy
- Alberts, b., Bray, D., Hopkin, k., Johnson, a., Lewis, J., Raff, m., Roberts, K. & Walter, P. (2004). Základná bunková biológia. New York: Garland Science.
- Cooper, G. M., Hausman, r. A. & Wright, n. (2010). Bunka. (PP. 397-402). Marbán.
- Devlin, T. M. (1992). Učebnica biochémie: s klinickými koreláciami. John Wiley & Sons, Inc.
- Garrett, R. H., & Grisham, C. M. (2008). Biochémia. Thomson Brooks/Cole.
- Ubytovňa, h., Darnell, J. A., Berk, a., Kaiser, C. Do., Krieger, m., Scott, m. P., & Matsudaira, P. (2008). Biológia mäkkýšov. Macmillan.
- Nelson, D. L., & Cox, M. M. (2006). Lehninger princípy biochémie 4. vydanie. Ed Omega. Barcelona.
- Voet, D., & Voet, J. G. (2006). Biochémia. Edimatizovať. Pan -American Medical.
- « Charakteristiky Euglenophyta, reprodukcia, výživa, klasifikácia
- Tréning, funkcie a typy/skupiny glukosidov »

