Tekutý stav

- 1318
- 232
- Tomáš Klapka
Vysvetlíme, aký je tekutý stav, aké sú jeho charakteristiky, a uvádzame niekoľko príkladov.
 Voda je v tekutom stave
Voda je v tekutom stave Aký je tekutý stav?
On tekutý stav Je to jeden z hlavných fyzikálnych stavov, ktorý sa prijal a ktorý sa hojne pozoruje v hydrosfére Zeme, ale nie s ohľadom na vesmír a jej žiarovky alebo teploty mrazu. Vyznačuje sa tečením a kompaktnejším ako plyny. Napríklad moria, rieky, jazerá a oceány tokujú a sú v tekutom stave.
Kvapalina je „most“ medzi tuhými a plynnými stavmi pre špecifickú látku alebo zlúčeninu; Most, ktorý môže byť malý alebo v extrémne širokej, čo ukazuje, ako stabilná je kvapalina vo vzťahu k plynu alebo tuhej látky a stupeň jeho súdržných síl medzi jeho atómami alebo prispôsobenými molekulami.
Potom je to chápané tekutinou všetko, čo je materiál, prírodný alebo umelý, schopný voľne prúdiť v prospech alebo proti gravitácii. Vo vodopádoch a riekach je možné vidieť tok čerstvých prúdov, ako aj v mori posunutie ich šumivých hrebeňov a ich lámanie na pobreží.
Voda je pozemská tekutina par excellence a chemickú reč je zo všetkých najvýhodnejších. Avšak stanovili požadované fyzikálne podmienky, akýkoľvek definovaný prvok alebo zlúčenina môžu prejsť do tekutého stavu; Napríklad soli a kvapalné plyny alebo žiaruvzdorná forma naplnená roztaveným zlatom.
Charakteristiky tekutého stavu

Nemajú žiadnu definovanú formu
Na rozdiel od tuhých látok potrebujú kvapaliny povrch alebo nádobu na získanie premenných tvarov.
Preto z dôvodu nezrovnalostí terénu, rieky „hadí“ alebo ak sa na podlahu rozlieva tekutina. Kvapaliny tiež naplnia kontajnery sýtiny alebo nádoby akejkoľvek geometrie alebo dizajnu, majú svoje formy, ktoré zaberajú celý svoj objem.
Môže vám slúžiť: Stanislao CannizzaroMajú dynamický povrch
Pevné látky tiež prijímajú povrchy, ale sú prakticky (pretože môžu erodovať alebo bežať) nezávisle od svojho okolia alebo kontajnera, ktorý ich ukladá. Na druhej strane, povrch kvapalín sa vždy prispôsobuje šírke nádoby a jej oblasť sa môže rozkladať, ak sa mieša alebo dotkne sa.
Kvapalné povrchy sú dynamické, pohybujú sa neustále, aj keď ho nedá pozorovať voľným okom. Ak je kameň hodený do rybníka v zjavnom pokoji, uvažuje sa o výskyte sústredných vĺn, ktoré cestujú z bodu, kde padol kameň smerom k okrajom rybníka.
Sú nepochopiteľné
Aj keď existujú výnimky, väčšina tekutín je nepochopiteľná. To znamená, že na zníženie objemov v značnom režime sú potrebné obrovské tlaky.
Sú molekulárne dynamické
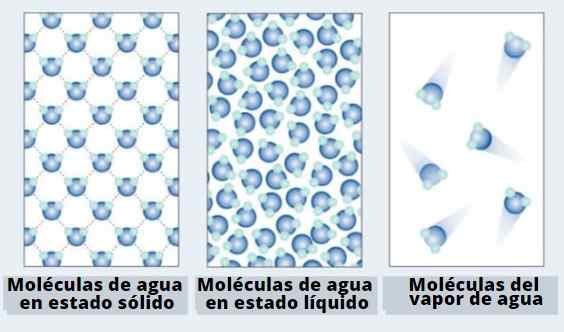
Atómy alebo molekuly majú slobodu pohybu v tekutinách, takže ich intermolekulárne interakcie nie sú dostatočne silné na to, aby ich udržali pevne vo vesmíre. Tento dynamický znak im umožňuje interagovať solubilizáciu alebo nie plyny, ktoré sa zrážajú s ich povrchmi.
Majú povrchové napätie

Kvapalné častice interagujú vo väčšej miere navzájom ako s časticami plynu, ktoré sú okolo jeho povrchu. V dôsledku toho častice, ktoré definujú povrch kvapaliny, zažívajú silu, ktorá ich priťahuje na dno, čo je proti zvýšeniu ich oblasti.
Preto sú kvapaliny pri rozliatí na povrch, ktorý nemôžu byť mokrý, usporiadané ako kvapky, ktorých tvary sa snažia minimalizovať svoju plochu, a teda povrchové napätie.
Môže vám slúžiť: rozsiahle vlastnosti hmotySú makroskopicky homogénne, ale môžu byť molekulárne heterogénne
Kvapaliny vyzerajú homogénne, pokiaľ nejde o nejaké emulzie, suspenzie alebo zmes nemiešateľných tekutín. Napríklad, ak sa Galio topí, budeme mať striebornú tekutinu, kdekoľvek sa pozriete. Molekulárne vystúpenia však môžu byť zavádzajúce.
Kvapalné častice sa pohybujú voľne, bez toho, aby boli schopné vytvoriť štrukturálny vzorec s dlhým rozdielom. Takéto svojvoľné a dynamické dispozície sa môže považovať za homogénnu, ale v závislosti od molekuly by kvapalina mohla umiestniť regióny vysokej alebo nízkej hustoty, ktoré by sa distribuovali heterogénne; Aj keď sa tieto regióny pohybujú.
Zmrazujú alebo odparujú

Kvapaliny môžu bežné dvojfázové zmeny: na pevnú látku (zmrazenie) alebo na sódu (odparovanie). Teploty, na ktoré sa tieto fyzické zmeny uskutočňujú, sa nazývajú fúzne alebo varné body.
Keď častice zamrznú, strácajú energiu a sú fixované vo vesmíre, teraz orientované svojimi intermolekulárnymi interakciami. Ak je takáto výsledná štruktúra pravidelná a usporiadaná, hovorí sa, že viac ako zmrazenie, kryštalizovala (ako v prípade ľadu).
Zmrznutie je zrýchlené v závislosti od rýchlosti, s akou sú tvary kryštalizačných jadier; to znamená, malé kryštály, ktoré budú rásť, až kým sa stanú robustnými.
Medzitým sa odparovanie zlomí so všetkými poriadkami: častice získavajú energiu cez teplo a unikajú plynovej fáze, kde cestujú s väčšou slobodou. Táto fázová zmena sa zrýchli, ak je zvýraznený rast bublín vo vnútri kvapaliny, čo prekonáva vonkajší tlak a ktorý vyvíja samotná kvapalina.
Príklady tekutín
Vodná voda
Na planéte Zem nachádzame vo veľkom množstve za najpodivnejšiu a prekvapujúcu tekutinu zo všetkých: Voda. Toľko tvorí to, čo je známe ako hydosféra. Oceány, moria, jazerá, rieky a vodopády predstavujú príklady tekutín pri maximálnom vyjadrení.
Môže vám slúžiť: Sigma odkazLáva

Ďalšou známym tekutinou je aj láva, ktorá horí na červenú nažive, čo predstavuje charakteristiku tečenia a stekala po sopkách.
Ropa
Môžeme tiež spomenúť olej, kvapalinu, komplex, čiernu a mastnú zmes zloženú väčšinou z uhľovodíkov; a nektár kvetov, ako med.
V kuchyni
Pri varení sú prítomné tekutiny. Medzi nimi máme: ocot, vína, anglickú omáčku, olej, vaječnú bielu, mlieko, pivo, kávu,. A ak sa varí v tme, roztavený vosk sviečok tiež hovorí ako príklad tekutiny.
V laboratóriách
Všetky rozpúšťadlá používané v laboratóriách sú príkladmi tekutín: alkoholy, amoniak, parafíny, toluén, benzín, titánové tetrachlorid, chloroforma, disulfid uhlíka, medzi inými.
Plyny, ako je vodík, hélium, dusík, argón, kyslík, chlór, neón atď., Môžu kondenzovať vo svojich kvapalinách, ktoré sa vyznačujú použitím na kryogénne účely.
Podobne existuje ortuť a bróm.
Odkazy
- Chémia. (8. vydanie.). Učenie sa.
- Fyzika: pre vedu a inžinierstvo s modernou fyzikou. Zväzok 2. (Siedme vydanie). Učenie sa.
- Tekutý. Zdroj: In.Wikipedia.orgán
- Definícia kvapaliny v chémii. Zotavené z: Thoughtco.com

