Glykosidic Link Čo je, charakteristiky, typy, nomenklatúra
- 3674
- 672
- Ing. Ervín Petruška
Ten Glykozidické odkazy Sú to kovalentné väzby, ktoré sa vyskytujú medzi cukrami (uhľohydráty) a inými molekulami, ktoré môžu byť inými monosacharidmi alebo inými molekulami rôznorodej povahy.
Tieto prepojenia umožňujú existenciu viacerých základných komponentov pre život, a to nielen pri tvorbe rezervných palív a štrukturálnych prvkov, ale aj základných informácií o transportoch informácií pre bunkovú komunikáciu.
Tvorba polysacharidov v zásade závisí od vytvorenia glykozidných dlhopisov medzi alkoholmi alebo bezplatnými hydroxylovými skupinami jednotlivých monosacharidových jednotiek.
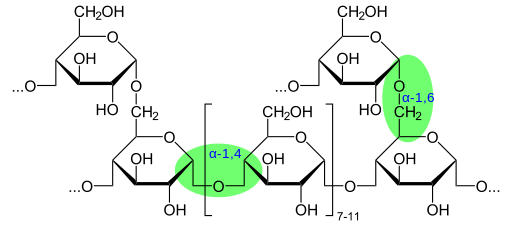 Príklad glykozidickej väzby v glykogéne (zdroj: glykogen.SVG-Neurotkerrivatívna-work-marek-m-public-doména cez Wikimedia Commons)
Príklad glykozidickej väzby v glykogéne (zdroj: glykogen.SVG-Neurotkerrivatívna-work-marek-m-public-doména cez Wikimedia Commons) Glykozidické väzby sa vyskytujú vo viacerých bunkových kontextoch, vrátane zväzku polárnej hlavy skupiny niektorých sfingolipidov, základných zložiek bunkových membrán mnohých organizmov a tvorby glykoproteínov a proteoglykánov.
Dôležité polysacharidy, ako je celulóza, chitín, agar, glykogén a škrob, by neboli možné bez glukozidných väzieb. Podobne proteín glykozylácia, ktorá sa vyskytuje v endoplazmatickom retikule a v Golgiho komplexe, je nanajvýš dôležitá pre aktivitu mnohých proteínov.
Charakteristika
Glykozidické väzby sú oveľa rôznorodejšie ako ich analógy v proteínoch a nukleových kyselinách, pretože v zásade sa môžu dve molekuly cukru v mnohých ohľadoch spojiť, pretože majú viac skupín -OH, ktoré sa môžu zúčastniť na tvorbe spojenia.
Okrem toho izoméry monosacharidov, tj jednej z dvoch orientácií, ktoré môže mať hydroxylová skupina v cyklickej štruktúre vzhľadom na anomérny uhlík, poskytujú ďalšiu úroveň diverzity.
Izoméry majú rôzne trojrozmerné štruktúry, ako aj rôzne biologické aktivity. Celulóza a glykogén pozostávajú z opakovaných jednotiek d-glukózy, ale líšia sa z hľadiska typu glukozidnej väzby (a1-4 pre glykogén a p1-4 pre celulózu), a preto majú rôzne vlastnosti a funkcie.
Rovnako ako polypeptidy majú polaritu s jedným koncom N- a druhým C- a polynukleotidmi majú 5 'a 3' konce, oligo-alebo polysacharidy majú polaritu definovanú znížením koncov a neznižujú sa.
Redukčný koniec má voľné anomerické centrum, ktoré nevytvára glykozidné spojenie s inou molekulou, takže si zachováva chemickú reaktivitu aldehydu.
Môže vám slúžiť: externé oplodnenieGlukozidická väzba je najflexibilnejšou oblasťou oligo-alebo polysacharidu.
Tvorba glykozidických väzieb
Glukozidická väzba sa môže spojiť s dvoma molekulami monosacharidov cez jednu a hydroxylovú skupinu druhej. To znamená, že hemiacetálna skupina jedného cukru reaguje s alkoholom inej skupiny aretál acetálu.
Všeobecne platí, že tvorba týchto odkazov sa vyskytuje kondenzačnými reakciami, kde sa uvoľňuje molekula vody s každým vytvoreným odkazom.
Avšak v niektorých reakciách kyslík neopustí molekulu cukru ako vodu, ale ako súčasť difosfátovej skupiny difosfátového uridínového nukleotidu.
Reakcie, ktoré vedú k vzniku glukozidných väzieb, sa katalyzujú triedou enzýmov známych ako glykozyltransferázy. Vytvárajú sa medzi kovalentne modifikovaným cukrom pridaním fosfátovej skupiny alebo nukleotidom (napríklad 6-fosfát glukóza, UDP-galaktóza), ktorá sa viaže na rastový reťazec v pestovateľskom polyméri.
Hydrolýza glykozidnej väzby
Glykozidické väzby môžu ľahko hydrolyzovať v mierne kyslých prostrediach, ale odolávajú pomerne zásaditých prostrediach.
Enzymatická hydrolýza glukozidných väzieb je sprostredkovaná enzýmami známymi ako glykozidázy. Mnoho cicavcov nemá tieto enzýmy na degradáciu celulózy, takže nie sú schopní extrahovať energiu z tohto polysacharidu, napriek tomu, že sú základným zdrojom vlákien.
Prežúvatelia, ako sú napríklad kravy, majú baktérie spojené s ich črevami, ktoré produkujú enzýmy schopné degradovať celulózu, ktorú jedia, čo im umožní využiť výhody energie zachovanej v rastlinných tkanivách.
The smooth enzyme, produced in the tears of the eye and by some bacterial viruses, is capable of destroying bacteria thanks to its hydrolytic activity, which breaks the glucosidic bond between the N-acetylglucosamine and the N-acetylmuramic acid in the cell wall of the baktéria.
Rôznorodosť
Oligosacharidy, polysacharidy alebo glykány sú veľmi rozmanité molekuly a je to kvôli viacerým spôsobom, akými sa môžu monosacharidy spojiť vytvorením štruktúr vyššieho poriadku.
Táto rozmanitosť začína od skutočnosti, ako je uvedené vyššie, že cukry majú hydroxylové skupiny, ktoré umožňujú rôzne oblasti Únie a že väzby sa môžu vyskytnúť medzi dvoma možnými stereoizomérmi vzhľadom na anomérny uhlík cukru (a alebo β).
Môže vám slúžiť: blastozoosGlykozidické väzby sa môžu tvoriť medzi cukrom a akoukoľvek hydroxylovanou zlúčeninou, ako sú alkoholy alebo aminokyseliny.
Okrem toho môže monosacharid tvoriť dve glukozidické väzby, takže môže slúžiť ako pobočkový bod, ktorý predstavuje potenciálnu zložitosť v štruktúre glykánov alebo polysacharidov v bunkách.
Chlapci
Pokiaľ ide o typy glukozidných väzieb, môžu sa diferencovať dve kategórie: glukozidné väzby medzi monosacharidmi, ktoré tvoria oligo- a polysacharidy, a glukozidné väzby, ktoré sa vyskytujú v gluproteínoch alebo glukolipidoch, ktoré sú proteínmi alebo lipidmi s karbohydrátom.
O-glukozidické odkazy
O-glykozidické väzby sa vyskytujú medzi monosacharidmi, tvoria sa reakciou medzi hydroxylovou skupinou molekuly cukru a anomérnym uhlíkom iného.
Disacharidy sú z najbežnejších oligosacharidov. Polysacharidy majú viac ako 20 jednotiek monosacharidov spojených lineárne a niekedy majú viac dôsledkov.
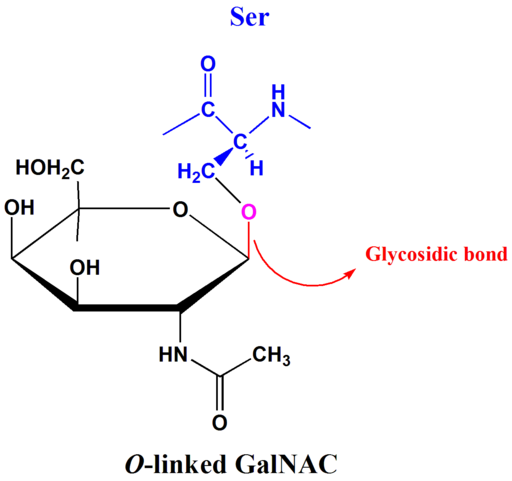 Príklad O-glukozidického odkazu (Zdroj: Tpirojsi [verejná doména] cez Wikimedia Commons)
Príklad O-glukozidického odkazu (Zdroj: Tpirojsi [verejná doména] cez Wikimedia Commons) U disacharidov, ako je maltóza, laktóza a sacharóza, je najbežnejšou glukozidnou väzbou O-glykozidický typ. Tieto spojenia sa môžu vyskytnúť medzi uhlíkmi a -OH izomérnych foriem a alebo p.
Tvorba glukozidných väzieb v oligo- a polysacharidoch bude závisieť od stereochemickej povahy cukrov, ktoré sú spojené, ako aj od ich počtu atómov uhlíka. Všeobecne platí, že pre cukry so 6 uhlíkom sa medzi uhlíkmi 1 a 4 alebo 1 a 6 vyskytujú lineárne väzby.
Existujú dva hlavné typy O-glykozidy, ktoré sú v závislosti od nomenklatúry definované ako a a β alebo 1,2-Cis a 1.2-previesť-glykozidy.
Odpad 1.2-Cis glykozylované, a-glykozidy pre d-glykózu, d-galaktózu, L-fukoza, d-xilosa alebo p-glykozidy pre D-manosa, l-yarabinosa; ako aj 1.2-previesť (P-glykozidy pre D-glukózu, D-galaktózu a a-glykozidy pre D-many atď.), majú veľký význam pre mnoho prírodných komponentov.
O-glykozylácia
Jednou z najbežnejších post -translačných modifikácií je glykozylácia, ktorá spočíva v pridávaní glucidovej časti k rastúcemu peptidu alebo proteínu. Mucíny, sekrécie proteínov, môžu obsahovať veľké množstvo oligosacharidových reťazcov spojených s O-glukozidnými väzbami.
Proces O -glykozylácie sa vyskytuje v Golgiho komplexe eukaryotov a pozostáva z spojenia proteínov s glucidálnou časťou glukozidnou väzbou medzi skupinou -OH aminoacidového zvyšku serínu alebo treonínu a anomerickým uhlíkom cukru.
Môže vám slúžiť: glukolipidy: čo sú, klasifikácia, štruktúra, funkcieTvorba týchto väzieb medzi uhľohydrátmi a hydroxylisínom a hydroxilisínom a fenolová skupina odpadu tyrozínu sa tiež pozorovala.
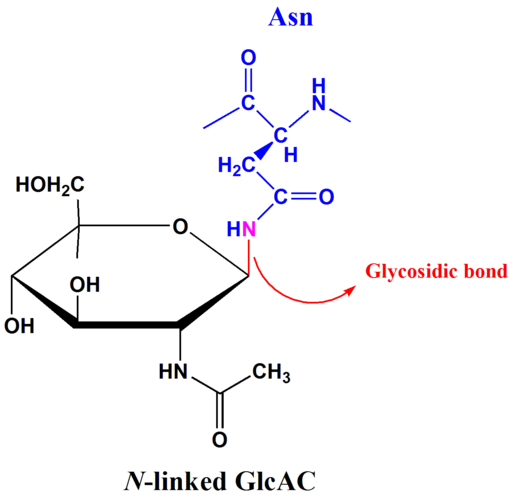
N-glukozidické odkazy
N-glycykozidické väzby sú najbežnejšie medzi glykozylovanými proteínmi. N-glykozylácia sa vyskytuje hlavne v endoplazmatickom retikule eukaryotov, s následnými modifikáciami, ktoré sa môžu vyskytnúť v Golgiho komplexe.
 Príklad n-glukozidického odkazu (Zdroj: Tpirojsi [verejná doména], cez Wikimedia Commons)
Príklad n-glukozidického odkazu (Zdroj: Tpirojsi [verejná doména], cez Wikimedia Commons) N-glykozylácia závisí od prítomnosti konsenzuálnej sekvencie série ASN-XXX/THR. Glykozidická väzba sa vyskytuje medzi uprostred dusíka bočného reťazca asparagínu a anomérnym uhlíkom cukru, ktorý sa viaže na peptidový reťazec.
Tvorba týchto väzieb počas glykozylácie závisí od enzýmu známeho ako oligosacariltransferáza, ktorá prenáša oligosacharidy z fosfátového dolicolu do uprostred dusíka asparagínového odpadu.
Iné typy glukozidných odkazov
S-glukozidické odkazy
Vyskytujú sa tiež medzi proteínmi a uhľohydrátmi, boli pozorované medzi peptidmi s N-terminálnymi cysteínmi a oligosacharidmi. Peptidy s týmto typom odkazov boli pôvodne izolované z proteínu v moči a ľudských erytrocytoch spojených s glukózovými oligosacharidmi.
C-glukozidické odkazy
Najprv boli pozorované ako post -translačná modifikácia (glykozylácia) v tryptofánovom zvyšku v RNASA 2 prítomným v ľudskom moči a v erytrocyte 2. Ruka sa viaže na uhlík z polohy 2 aminokyselinového jadra pomocou c-glukozidnej väzby.
Menovanie
Termín glykozid sa používa na opis akéhokoľvek cukru, ktorého anomérna skupina je nahradená skupinou -alebo (O -glykozidy), -sr (tioglykozidy), -ser (selenoglukozidy), -nr (N -glykozidy alebo glukozamíny) alebo dokonca -cr. (C-glukozidy).
Môžu byť pomenované tromi rôznymi spôsobmi:
(1) Nahradenie terminálu „-o“ názvu zodpovedajúcej cyklickej formy monosacharidu „-ido“ a písanie skôr, ako iné slovo, názov náhradnej skupiny R Group R.
(2) Použitie výrazu „glycosyloxi“ ako predpona názvu monosacharidu.
(3) Použitie tohto pojmu Ani-glykozil, N-glykozil, Siež-glykozil alebo C-glykozil ako predpona názvu hydroxylovanej zlúčeniny.
Odkazy
- Nelson, D. L., & Cox, M. M. (2009). Lehninger princípy biochémie. Vydanie omega (5. vydanie.).
- Nomenklatúra uhľohydrátov (odporúčania 1996). (Devätnásť deväťdesiat šiestich). Zdroj z www.Qmul.Ac.Uk
- « Branchiopoda Čo je, charakteristiky, reprodukcia, jedlo
- Tichomorská púšť, čo je, charakteristika, klíma, flóra, fauna »

