Štruktúra sodného sodného (SDS) dodecilu, vlastnosti, používa
- 4591
- 205
- MUDr. Žigmund Boška
On Sodný sulfát dodecyl (SDS), je aniónový, syntetický a amfifylický organická soľ. Apolárna a hydrofóbna časť zodpovedá uhľovodíkovému reťazcu; Zatiaľ čo polárna a hydrofilná časť je spôsobená sulfátom, s negatívnym zaťažením.
SDS je povrchovo aktívna látka: jeho molekuly sú umiestnené na povrch vodných roztokov, čo spôsobuje zníženie povrchového napätia. Táto funkcia umožňuje jeho použitie v šampóne, zubných krémoch, mydlách a iných článkoch osobnej starostlivosti a čistenia domácnosti.
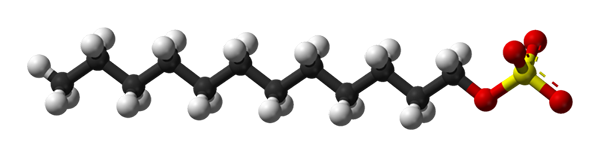
 Dodecilná štruktúra síranu sodného. Zdroj: Benjah-Bmm27 Via Wikipedia.
Dodecilná štruktúra síranu sodného. Zdroj: Benjah-Bmm27 Via Wikipedia. Dodecylsulfát sodný sa viaže na proteín a vytvára jeho rozvíjanie a získa predĺžený tvar. Skupiny síranu sú vystavené vode a získavajú proteíny negatívneho zaťaženia, ktorých počet je úmerný ich molekulovej hmotnosti.
Z tohto dôvodu SDS umožňuje stanovenie molekulových hmotností proteínov prostredníctvom elektroforézy v polyakrylamide.
Aj keď bol podozrivý karcinogénny účinok SDS, nebolo presvedčivo preukázané, že je to tak. SDS môže produkovať, rovnako ako iné detergenty, podráždenie pokožky a očí.
[TOC]
Štruktúra SDS
Na prvom obrázku bola molekula SDS zobrazená s guľovými a stĺpcovými modelmi. Ako je vidieť, má hydrofóbny a apolárny uhlíkový chvost (čiernobiele gule); A zároveň polárna hlava, vďaka prítomnosti skupiny -so4- (žlté a červené gule).
Aj keď to nie je znázornené, mala by existovať fialová guľa predstavujúca Na katión+, Hneď vedľa skupiny -SO4-, elektrostaticky interakcie.
To znamená, že je to chápané voľným okom, prečo je táto zlúčenina amfifylikálna; a tiež aniónové napätie, pretože zaťaženie SDS je negatívne a môže okrem NA prilákať ďalšie katióny+.
Molekula vyvoláva falošný dojem, že je tuhá, nehnuteľná lineárna štruktúra. Je to však naopak. SDS možno porovnávať s „červom“, ktorého uhlíkový chvost predstavuje viac vibrácií a rotácií svojich jednoduchých spojení. Vďaka tomu je schopný prijať rôzne konformácie alebo záhyby v strede; Napríklad.
Kryštály
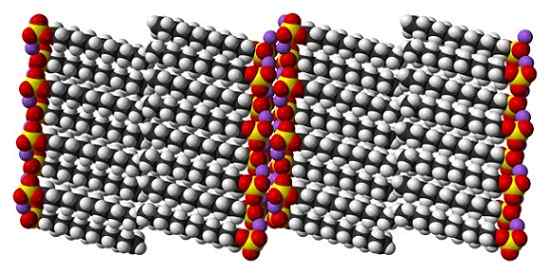 Kryštalická štruktúra sulfátu dodecylového sodného. Zdroj: Benjah-Bmm27 [verejná doména]
Kryštalická štruktúra sulfátu dodecylového sodného. Zdroj: Benjah-Bmm27 [verejná doména] Aj keď je pravda, že dodecyl sulfátu sodného je dynamická molekula, v tuhom stave sa nemusí príliš pohybovať, správajúc sa ako „jednoduchý“ stĺpec. A tak je každá molekula alebo stĺčka umiestnená takým spôsobom, že interakcie medzi sýtenými frontami a súčasne sa zvyšujú interakcie svojich iónových zaťažení.
Môže vám slúžiť: chlorit sodný (NACLO2): Štruktúra, vlastnosti, použitia, rizikáVýsledkom je tvorba monoklinického kryštálu, kde sú molekuly SDS zabalené do niekoľkých stĺpcov stĺpcov (horný obrázok). Intermolekulárne sily, ktoré ich spájajú, sú také, že tieto kryštály vyžadujú teplotu 206 ° C na roztavenie kvapalnej fázy.
Miclá
Mimo pohodlia jeho kryštálov už molekula SDS už nemôže zostať v pokoji; Začnite krútiť chvostom, aby sa zvýšila alebo znížila interakcie s vonkajším prostredím.
Ak je toto médium voda, dochádza k javu nazývaným tvorba mikelle: uhlíkové a hydrofóbne chvosty sa viažu na obklopenie, zatiaľ čo polárne hlavy, skupiny -so4-, Zostávajú na povrchu interagujú s molekulami H2Ani.
Potom micella získa obláčnu elipsoidnú morfológiu (napríklad Zem, ale viac rozdrvená). V kryštáli sú ako barové bloky a vo vodnom médiu ako elipsoidné micely. Čo keby médium bolo olejom? Myce by sa investovali: polárne hlavy tak4- Išli by do jadra, zatiaľ čo ich sýtené chvosty by boli vystavené rope.
Vlastnosti
Mená
- Dodecilsulfát sodný (SDS).
- Laulsulfát sodný (SLS).
Molekulárna receptúra
C12H25Ani4SNA.
Molárna hmota
288 378 g/mol.
Fyzický popis
Niekoľko prezentácií: suchý prach, tekutina alebo vlhká pevná látka. Jeho kryštály majú biele alebo krémové sfarbenie.
Vôňa
Otec vôňa tukových látok, toaleta.
Bod topenia
206 ° C.
Rozpustnosť
1 · 105 mg/l. 1 g rozpustený v 10 ml opalescentného roztoku.
Hustota
1,01 g/cm3.
Stabilita
Je stabilný za odporúčaných podmienok skladovania.
Rozklad
Keď sa zahrieva na rozklad emituje biely dym oxidu síry a oxidu sodného.
Povrchové napätie
39,5 Dynas/cm pri 25 ° C.
Kritická koncentrácia moláru
Je 8,2 mm v čistej vode pri 25 ° C.
Žiadosti
Osobná starostlivosť a čistenie doma
Sulfát Doddecyl je povrchovo aktívna látka, ktorá sa používa v mnohých výrobkoch, ako sú toaletné mydlá, penové kúpele, krém na holiace strojčeky atď. Používa sa tiež na odstránenie škvŕn z ťažkostí na odstránenie, pri čistení podlah a kúpeľní, chlpatého kuchynského tovaru atď.
Môže vám slúžiť: olej alebo benzín éter: vzorec, štruktúra, použitieVeterinárny a ľudský lekár
Používa sa ako repelent blchov a kliešťov, prítomných u zvierat. Používa sa tiež ako zvlhčovač v niektorých antibiotikách na ústne alebo lokálne použitie.
SDS je mikrobicíd proti vírusom s obalom, ako sú HIV, typy 1 a 2 a herpes jednoduchý herpes vírus (HSV-2). Pôsobí tiež na vírus bez zabalenia: papilomavírus, reovírus, rotavírus a poliovírus. Toto použitie však nie je schválené.
Použitie SDS bolo navrhnuté ako vaginálna sprcha, ktorá poskytuje ochranu pred sexuálne prenosným vírusom. Tiež pri spracovaní materského mlieka na odstránenie alebo zníženie možnosti prenosu HIV prostredníctvom dojčenia.
SDS okrem svojho antivírusového pôsobenia pôsobí na patogénne baktérie a huby. SDS eliminuje rezistenciu na lieky a faktory sexuálnej rezistencie z e. coli; a blokuje rast početných pozitívnych gramových baktérií.
V laboratóriu
SDS sa viaže na proteíny spôsobujúce ich denaturáciu, poskytuje negatívne zaťaženie a konformačnú zmenu. To umožňuje stanovenie jeho molekulových hmotností elektroforézou v polyakrylamide.
SDS sa tiež používa pri príprave vzoriek mozgového tkaniva na použitie v optickej mikroskopii. Používa sa tiež pri príprave vzoriek krvi na počet erytrocytov.
SDS sa používa pri čistení nukleových kyselín, kvôli ich schopnosti rozpustiť membrány a ich inhibičný účinok na aktivitu enzýmov ARNASA a DNAASA.
Okrem toho sa SDS používa pri charakterizácii kvartérnych amónnych zlúčenín.
Aditívna potravina
SDS sa používa ako emulgátor a zhrubnutie potravín. Zlepšuje stabilitu a textúru pečených výrobkov. Okrem toho sa používa ako pomocný v sušených vaječných výrobkoch.
Môže vám slúžiť: dusičnan zinku: štruktúra, vlastnosti, získanie, použitiaPriemysel
SDS sa používa v priemysle galvanoplastiky, najmä niklu a zinku; ako emulgácia a prenikajúci odstraňovač laku a maľby; pri formulácii výbušnení formovaných vstrekovaním; a v pevných raketách ako penenie.
Riziká
SDS Konštantná expozícia môže spôsobiť hyperpláziu pokožky u morčiat ošípaných. Králik a ľudské bytosti sú na tieto zranenia menej náchylné. Priamy kontakt s SDS pri koncentrácii ≤ 20%môže spôsobiť mierny zápal a podráždenie kože.
Na druhej strane, predĺžené vystavenie SDS môže produkovať dermatitídu, so znakmi začervenania, opuchov a tvorby ampúlov.
SDS môže produkovať podráždením kontaktného oka. Môže byť tiež veľmi reaktívny u niektorých ľudí a spôsobiť podráždenie inhalácie dýchacích traktov a dýchacích problémov.
Zriedkavo, požitie SDS môže spôsobiť žieravé lézie. Ale bolo hlásené u detí, ktoré požilo SDS, bohaté zvracanie rýchleho rozvoja, depresie CNS a dýchacie ťažkosti.
V SDS sa nenašiel žiadny dôkaz genotoxicity alebo teratogénneho pôsobenia. U 242 pacientov s ekzémnou dermatitídou bolo nájdených 6,4 % pacientov s alergiou, čo možno pripísať použitiu SDS.
Odkazy
- Štrukturálne údaje z L. Do. Smith, r. B. Hammond, K. J. Roberts, D. Machin, g. McLeod (2000). Stanovenie kryštálovej strupu bezvodého dodecylsulfátu sodného s použitím kombinácie difrakcie práškového žiarenia sychrotrónového žiarenia a technických molekulárnych modelovania. Časopis molekulárnej štruktúry 554 (2-3): 173-182. Doi: 10.1016/S0022-2860 (00) 00666-9.
- Wikipedia. (2019). Dodecylsulfát sodný. Zdroj: In.Wikipedia.orgán
- Národné centrum pre biotechnologické informácie. (2019). Dodecylsulfát sodný. Databáza pubchem. CID = 3423265. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Hammouda B. (2013). Teplotný účinok na nanoštruktúru miciel SDS vo vode. Journal of Research of Národný inštitút štandardov a technológie, 118, 151-167. Doi: 10.6028/jres.118.008
- Elsevier. (2019). Dodecylsulfát sodný. Vedecký. Zdroj: ScienceDirect.com
- Kumar, s., TheJaJenuo, j. Klimatizovať. a Tsipila, T. (2014). Toxikologické účinky dodecylsulfátu sodného. Journal of Chemical and Pharmaceutical Research 6 (5): 1488 - 1492.
- Toxikologická dátová sieť. (s.F.). Laurylsulfát sodný. Tónovanie. Získané z: Toxnet.NLM.NIH.Vláda
- « Terciárna štruktúra hlavných charakteristík
- Fosfatidilserínová štruktúra, syntéza, funkcie, umiestnenie »

