Štruktúra dimetylanylínu, vlastnosti, syntéza, používa
- 3994
- 972
- JUDr. Rudolf Čapkovič
Ten dimetylanylín o Dimetilfenyllamín je organická zlúčenina, ktorá je tvorená benzénovým kruhom s aminoskupinou nahradenou dvoma metylovými skupinami. Jeho chemický vzorec je C8HjedenásťN.
Je tiež známy ako N, N-Dimetylanylin, pretože je to derivát Anylin, v ktorom sa aminoskupina hydrogény nahradí dvoma metylovými skupinami. Vďaka tomu je terciárny amín.
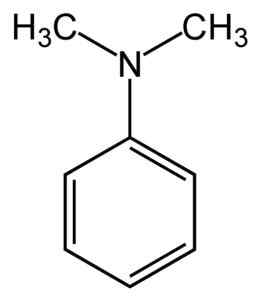 Štruktúra N, N-dimetylanylín. Nie je k dispozícii žiadny strojovo čitateľný autor. MySID predpokladal (na základe nárokov na autorské práva). [CC BY-SA 3.0 (http: // creativeCommons.Org/licencie/By-SA/3.0/]]. Zdroj: Wikipedia Commons.
Štruktúra N, N-dimetylanylín. Nie je k dispozícii žiadny strojovo čitateľný autor. MySID predpokladal (na základe nárokov na autorské práva). [CC BY-SA 3.0 (http: // creativeCommons.Org/licencie/By-SA/3.0/]]. Zdroj: Wikipedia Commons. N, n-dimetylanylín je bledožltá až hnedá mastná tekutina s charakteristickou vôňou amínov. Je to základná zlúčenina a reaguje s kyselinou dusnou tvoriacou nitrosokomosponovanú. Keď je vystavený vzduchu, zhnedne.
Používa sa na výrobu farbív na maľby. Používa sa tiež ako aktivátor polymerizačných katalyzátorov a v zmesiach používaných na zaznamenávanie obrazu. Na druhej strane sa používa v syntéze antibakteriálnych zlúčenín alebo antibiotík ako určité cefalosporíny odvodené z penicilínu. N, N-dimetylanylín je tiež základom pre získanie ďalších chemických zlúčenín.
Je to horľavá kvapalina a keď sa zahrieva, až kým rozklad nevyjadruje toxické výpary. Akútna expozícia ľudskej bytosti N, N-dimetylanylínu môže viesť k negatívnym účinkom, ako sú bolesti hlavy, závraty, zníženie kyslíka v krvi a sfarbenie modrej pokožky, okrem iných príznakov.
[TOC]
Štruktúra
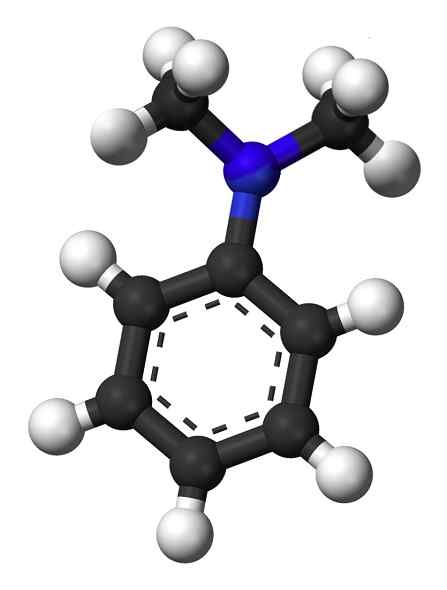
Nasledujúci obrázok ukazuje priestorovú štruktúru N, N-dimetylanylínu:
 Priestorová štruktúra N, N-dimetylanylínu. Esquilo [verejná doména]. Zdroj: Wikipedia Commons.
Priestorová štruktúra N, N-dimetylanylínu. Esquilo [verejná doména]. Zdroj: Wikipedia Commons. Menovanie
- N, n-dimetylanylín
- Dimetylanylín
- Dimetylfenyllamín
- N, N-dimetyl-Bencenamín
N je umiestnený v názve, čo naznačuje, že dve metylové skupiny (-ch3) sú pripojené k dusíku (N) a nie k prsteňu Benncénico.
Vlastnosti
Fyzický stav
Bledá až hnedá tekutina.
Molekulová hmotnosť
121,18 g/mol.
Môže vám slúžiť: anión: školenie, vlastnosti a typyBod topenia
3 ° C.
Bod varu
194 ° C.
Bod vzplanutia
63 ° C (metóda zatvoreného pohára). Je to minimálna teplota, pri ktorej sa môžete vypnúť výpary, ak sa na ňu prenesie plameň.
Tlak vodnej pary
0,70 mm Hg pri 25 ° C.
Teplota
371 ° C. Je to minimálna teplota pri spontánne spaľujúcom atmosférickom tlaku, bez vonkajšieho zdroja tepla alebo plameňa.
Hustota
0,9537 g/cm3 pri 20 ° C.
Index lomu
1 5582 až 20 ° C.
Rozpustnosť
Vo vode je veľmi malé rozpustné: 1 454 mg/l A 25 ° C.
Voľne rozpustné v alkohole, chloroforme a éteru. Rozpustný v acetóne, benzéne a okysličených a chlórovaných rozpúšťadlách.
Konštantná základnosť
Klimatizovaťb 11.7, čo naznačuje ľahkosť, s akou táto zlúčenina prijíma vodíkový ión vody.
Chemické vlastnosti
N, N-dimetylanylín je základná zlúčenina. Reaguje s kyselinou octovou, čím sa získal oct.
Skupina -n (vyberte si3)2 N, N-dimetylanylín je silným aromatickým substitučným aktivátorom v tejto pozícii pre benzénového kruhu.
Reaguje s dusitanom sodným (nano2) V prítomnosti kyseliny chlorovodíkovej (HCL) tvoriace p-nitroso-N, N-dimetylanylín. Tiež s kyselinou dusnou vytvára rovnaké zlúčeniny nitrosado v polohe pre.
Pri reagovaní N, N,-dimetilanilínu s benzónskym chloridom, v jemne kyslom médiu, je azokomponovaný typ AR-N = N-AR ', kde AR je aromatická skupina. Molekuly s skupinami Azo sú silne zafarbené zlúčeniny.
Riziká
Keď sa zahrieva na jeho rozklad, emituje vysoko toxické výpary oxidov dusíka nieX.
Je to horľavá tekutina.
Pomaly sa rozkladá vo vode vystavenej slnečnému žiareniu. Nie je to biodegradované.
Je prchavý z mokrých pôd a vodných povrchov. Nevarte suchú pôdu a nepohybujte sa s tým. Nezhromažďuje sa v rybách.
Môže vám slúžiť: sulfid železa (ii): Vlastnosti, riziká a použitiaMôže byť absorbovaný pokožkou. Sa tiež rýchlo absorbuje inhaláciou. Expozícia človeka N, N, Nimetylanylín môže znížiť obsah kyslíka v krvi, čo vedie k modrej farbe pleti.
Akútna inhalácia tejto zlúčeniny môže viesť k negatívnym účinkom na centrálny nervový systém a obehový systém, s bolesťou bolesti, cyanózou a závrachmi.
Syntéza
Môže sa vyskytnúť niekoľkými spôsobmi:
- Z anilínu a metanolu pod tlakom v prítomnosti kyslých katalyzátorov, ako je H2SW4. Získava sa sulfát, ktorý sa stáva bázou pridaním hydroxidu sodného.
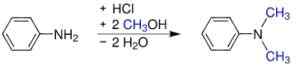 S syntéza, N-dimetylanylín. Werderkli - vlastná práca. Verejná doména. Zdroj: Wikipedia Commons.
S syntéza, N-dimetylanylín. Werderkli - vlastná práca. Verejná doména. Zdroj: Wikipedia Commons. - Prechádzanie anilínovou parou a dimetyléter na aktivovanom oxidu hlinitého.
- Zahrievanie zmesi anilínu, chloridu aninium a metanolu pod tlakom a potom destilácie.
Žiadosti
V priemysle sfarbenia
Na vlastníctvo reagovania s bencecenodiazónskym chloridom tvoriacim azokompiestos sa n-dimetylanylín používa ako sprostredkovateľ vo výrobe sfarbenia.
Je to surovina v syntéze farbív rodiny metylových fialových.
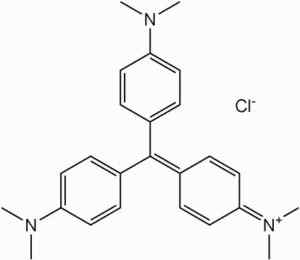 Sfarbenie metylovej fialovej farby. Nie je k dispozícii žiadny strojovo čitateľný autor. ShadDack predpokladal (na základe nárokov na autorské práva). [Verejná doména]. Zdroj: Wikipedia Commons
Sfarbenie metylovej fialovej farby. Nie je k dispozícii žiadny strojovo čitateľný autor. ShadDack predpokladal (na základe nárokov na autorské práva). [Verejná doména]. Zdroj: Wikipedia Commons Pri výrobe fotomatických zmesí
N, N,-dimetylanylín je súčasťou fotomaračnej zmesi, ktorá pociťuje reakciu vyliečenia v dôsledku vysokej citlivosti na viditeľné svetlo alebo zatvorené infračervené, takže sa dá použiť na zaznamenávanie obrazov alebo fotorestonovacích materiálov.
N, N-Dimetylanylín je jednou z zložiek zmesi, ktorá spôsobuje povedomie vlnových dĺžok, takže zloženie je vyliečené nízkoenergetickým svetlom na vlnovú dĺžku.
Môže vám slúžiť: benzénové derivátyOdhaduje sa, že funkcia N, N-dimetylinu je pravdepodobne na potlačenie ukončenej reakcie radikálnej polymerizácie spôsobenej kyslíkom.
Vo výrobe zo sklenených vlákien
N, N-dimetylanylín sa používa ako katalytický útočník v určitých živici zo sklenených vlákien.
Pri syntéze antibiotík
N, N-dimetylanylín sa podieľa na syntéze cefalosporínov na základe penicilínov.
Penicilín sulfoxidy sa premieňajú na cefemes, keď sa zahrievajú v prítomnosti základných katalyzátorov, ako je N, N-Dimetylanylin.
Tieto cefalosporíny vykazujú antibakteriálnu aktivitu proti grampozitívnym a gramnegatívnym organizmom, ako aj proti stafylokokom rezistentným na penicilín.
 Antibiotiká. Alina Kuptsová. Zdroj: Pixabay.
Antibiotiká. Alina Kuptsová. Zdroj: Pixabay. Malo by sa však poznamenať, že N, n-dimetylanylín zostáva v týchto antibiotikách ako nečistota.
Na chemické reakcie
N, N-dimetylanylín sa používa pri aktivácii katalyzátorov olefínových polymerizácií.
Používa sa spolu s pentafluorofenolom (c6F5OH), s ktorým tvorí iónovú zlúčeninu [HNPHME2]+[H (OC6F5)2]-. Táto iónová zlúčenina má jeden alebo dva aktívne protóny, ktoré aktivujú katalyzátor na základe prechodného kovu.
Navyše, v výrobe živíc, sa n-dimetylanylín používa ako polymerizačný urýchľovač alebo promótor pre polyesterové živice. Jeho akcia vytvára rýchle vytvrdzovanie živice.
V niekoľkých aplikáciách
Používa sa v syntéze iných chemických zlúčenín, napríklad vanilínu a ako sprostredkovateľ pre farmaceutické lieky.
Používa sa tiež ako rozpúšťadlo, ako alkylačné činidlo, ako stabilizátor a na výrobu maľieb a povlakov.
Odkazy
- Siež. Lekárska knižnica. (2019). N, N-dimetylanilín. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Morrison, r.Tón. a Boyd, r.N. (2002). Organická chémia. 6. vydanie. Hara.
- (2000). N, N-dimetylanilín. Zhrnutie. Zdroj z EPA.Vláda
- Zanaboni, P. (1966). Nenasýtené polyesterové živicové zloženie Havh stabilita a rýchle vytvrdzovanie pri nízkych teplotách pomocou zmesi dimetylanilu, trrenhanolamínu a difenylamínu. Alebo.Siež. Patent. 3 236 915. 22. februára 1966.
- Nudelman, a. a McCaully, r.J. (1977). Proces preusporiadania penicilínov pre cefalosporíny a ich stredné kompeny. Alebo.Siež. Patent. 4 010 156. 1. marca 1977.
- Kouji Inaishi (2001). Zloženie. Alebo.Siež. Patent. 6 171 759 B1. 9. januára 2001.
- Luo, l. a kol. (2012). Kyselina iónová bransted. Alebo.Siež. Patent. 8 088 952 B2. 3. januára 2012.
- « História Rodia, vlastnosti, štruktúra, použitie, riziká
- Charakteristiky akútnych zvukov a príklady »

