Kyselina chloro (HCLO2)
- 2813
- 196
- Gabriel Bahna
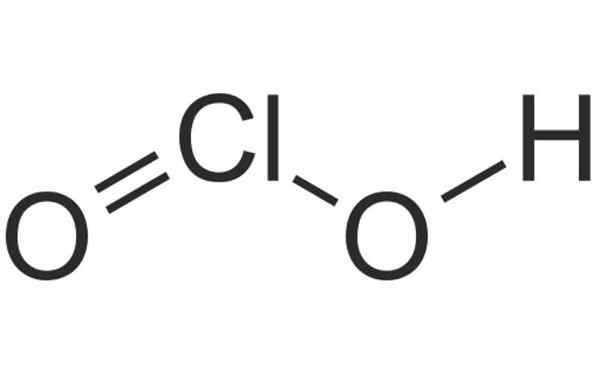
 Chemická štruktúra kyseliny chlórnej. Zdroj: HBF878, Wikimedia Commons
Chemická štruktúra kyseliny chlórnej. Zdroj: HBF878, Wikimedia Commons Čo je chloro?
On Kyselina chlór Je to anorganická zlúčenina HCLO vzorca2. Táto kyselina je jednou z oxacidových kyselín chlóru, kde sa nachádza s oxidačným stavom 3+.
Aj keď je v čistej látke ťažké získať kyselinu, konjugátová báza odvodená z týchto kyselín, ión chlorita, je stabilný. Príkladom soli tohto aniónu je chlorit sodný. Tento a ďalšie súvisiace soli sa niekedy používajú pri výrobe oxidu chloričitého.
Kyselina chloro je slabá kyselina. Čistá látka je nestabilná, neprimeraná s kyselinou hypoklorous (oxidačný stav Cl +1) a kyselina chlorovodíková (oxidačný stav CL +5):
2HCLO2 → HCLO + HCLO3
Kyselina chloro sa získa, spolu s chlorickou kyselinou, v rozkladu vodného roztoku oxidu chloritého.
Roztok kyseliny chlórovej sa najprv získal znížením kyseliny chlorovodíkovej kyselinou z tartarovej, avšak hlavnou metódou získania tejto kyseliny je ošetrenie suspenzie chloridu bária s kyselinou sírovou:
BA (CLO2)2 + H2SW4 → Baso4 + 2HCLO2
Kyselina chlór je silné oxidačné činidlo, hoci jej tendencia šíriť alebo disproporcie pôsobí proti jej oxidačnému potenciálu.
Chlór je jediný halogén, ktorý tvorí izolovateľnú kyselinu HXO kyseliny vzorec2. Ani kyselina bromous, ani kyselina jodóza neboli izolované. Niektoré soli vtipnej kyseliny, vtipy sú známe, ale s výnimkou sprostredkovateľov v reakciách neexistujú žiadne soli Yoditos.
Fyzikálne a chemické vlastnosti
- Kyselina chloro, keď je možné izolovať, je bezfarebná kvapalina bez charakteristickej arómy.
Môže vám slúžiť: cykloalcinos- Zlúčenina má molekulovú hmotnosť 68 456 g/mol. Má bod varu (vypočítaný) 502,07 ° C a 1 x 10 (vypočítaná) rozpustnosť vo vode6 mg/l.
- HCLO2 Je nestabilný v dôsledku disutačnej reakcie (alebo disproporcie) za vzniku chlorickej a hypokloróznej kyseliny, podobne ako u analógových kyselín brómov a jódu:
2HCLO2 → HCLO + HCLO3
- Kyselina chlór sa považuje za slabú kyselinu, hoci jej disociačná konštanta je v poradí 1 x 10-2, Čo to nerobí tak slabé ako iné kyseliny, ktoré majú PKA 1,96.
Riziká
Kyselina chlór je nestabilná zlúčenina a silné oxidačné činidlo nekompatibilné s redukčnými činidlami a alkalismi.
Kyselina chloro dráždi v prípade kontaktu s pokožkou a očami a je nebezpečná v prípadoch požitia a inhalácie.
V prípade kontaktu s očami musíte overiť, či sa používajú kontaktné šošovky, a okamžite ich odstráňte. Oči by mali byť opláchnuté tečúcou vodou najmenej 15 minút, pričom viečka sú otvorené. Môže sa použiť studená voda, ale nie očná masť.
Ak chemikália príde do styku s oblečením, zachovajte ju čo najrýchlejšie a chráňte svoje vlastné ruky a telo. Položte obeť pod bezpečnostnú sprchu.
Ak sa chemická látka hromadí v exponovanej pokožke obete, ako sú ruky, pokožka kontaminovaná tečúcou vodou a neabrazzívne mydlo je jemne umyté a opatrne.
Môže sa použiť studená voda. Ak podráždenie pretrváva, vyhľadajte lekársku pomoc. Pred opätovným použitím umyte kontaminované oblečenie.
Môže vám slúžiť: fosfátová skupinaAk je kožný kontakt vážny, mal by sa premyť dezinfekčným mydlom a pokožka kontaminovaná antibakteriálnym krémom.
V prípade vdýchnutia by sa obeť mala nechať stáť v dobre vetranej oblasti. Ak je inhalácia vážna, obeť sa musí čo najskôr evakuovať do bezpečnej oblasti. Voľné pevné oblečenie, ako je krk košele, opasky alebo kravata.
Ak je obeť ťažké dýchať, musí sa podávať kyslík. Ak obeť nedýcha, urobí sa resuscitácia úst v ústach. Vždy berúc do úvahy, že to môže byť nebezpečné pre osobu, ktorá poskytuje pomoc pri poskytovaní resuscitácie úst, keď je vdýchnutý materiál toxický, infekčný alebo korozívny.
V prípade požitia nevyvoláva zvracanie. Uvoľnite tesné oblečenie. Ak obeť nedýcha, urobte resuscitáciu úst v ústach. Vo všetkých prípadoch by sa mala hľadať okamžitá lekárska starostlivosť.
Žiadosti
- Uskutočnili sa štúdie, kde meta stabilné roztoky kyseliny chlóru/chlóru, ako je perorálne opláchnutie na zníženie dosiek.
Štúdia bola uskutočnená v skupine 18-27 rokov dobrovoľníkov. Jeho účinok na vývoj platne a počet bakteriálnych slinných slín sa testoval, čím sa znížilo zníženie skóre zubných doštičiek v porovnaní so skupinou s placebom až 34,5%.
- Kyselina chlór je zapojená do prípravy chlorita sodná, ktorá má antimikrobiálne vlastnosti a je určená na použitie hlavne ako sprej alebo ponorný roztok pre hydinu, mäso, zeleninu, ovocie a morské potraviny. Používa sa tiež vo vode chladiacej vtákov.
Môže vám slúžiť: degenerované orbitály- Chlorirát sodnálnej kyseliny sa vyrába pridaním kyseliny kvality potravy (napríklad kyselina citrónová, kyselina fosforečná, kyselina chlorovodíková, kyselina koleso alebo síran sulfát vodíka) do vodného roztoku chlorita sodného (Naclolovodíková (Naclo2).
Kombinácia kyseliny s roztokom chlorita sodného vedie k konverzii chloritov na kyselinu chlór meter (HCLO2).
Naclo2 + H+ ⇌ HCLO2 + Nat+
Tento roztok môže následne tvoriť zmes s chloritom (Clo2-), oxid chloričitého (CLO2) a chlorid (CLM). Reakcia generuje oxidačný roztok s oxychlovanými druhmi s antimikrobiálnymi vlastnosťami.
- Chlorón sodnálnej kyseliny je navrhnutý tak, aby sa použil ako súčasť integrovaného prístupu zameraného na reguláciu mikrobiálnych zaťažení v potravinách.
Roztok chlorita sodnej pôsobí na zníženie počtu patogénov (napríklad, Escherichia coli, A. Coli O157: H7, Salmonella spp., Campylobacter spp., a Listeria monocytogenes).
Odkazy
- Chlorózna kyselina. Zotavené z EBI.Ac.Uk.
- Národné centrum pre biotechnologické informácie. Obnovený z pubchem.

