Zložka elektrónového dopravného reťazca, sekvencia, inhibítory
- 629
- 10
- Václav Višňovský
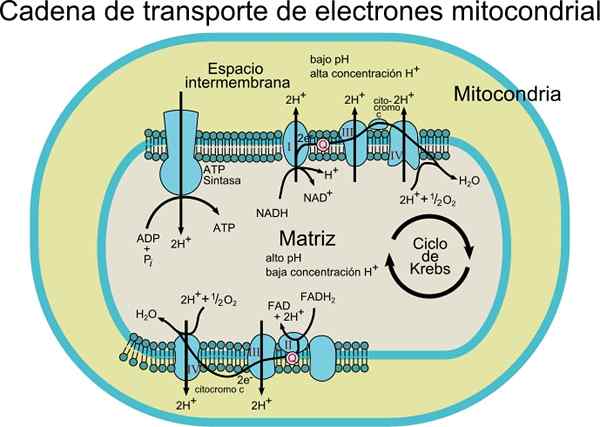
Ten elektrónový dopravný reťazec Skladá sa zo súboru proteínových a koenzýmových molekúl vo vnútri membrány. Ako už názov napovedá, je zodpovedný za transport elektrónov z koenzýmov NADH alebo FADH2 do konečného prijímača, ktorý je O2 (molekulárny kyslík).
V tomto transportnom procese je energia uvoľnená prenosom elektrónov z koenzýmov na molekulárny kyslík pomocou redoxných centier United s proteínmi spojená s výrobou energie (ATP). Táto energia sa získava vďaka protónovému gradientu, ktorý sa vytvára v mitochondriálnej vnútornej membráne.
 Zdroj: Používateľ: Rozsychan [CC BY-SA 2.5 (https: // creativeCommons.Org/licencie/By-SA/2.5)]
Zdroj: Používateľ: Rozsychan [CC BY-SA 2.5 (https: // creativeCommons.Org/licencie/By-SA/2.5)] Tento transportný systém pozostáva z rôznych komponentov, ktoré sa nachádzajú v najmenej v dvoch oxidačných stavoch. Každý z nich je účinne redukovaný a reoxyd počas pohybu elektrónov z NADH alebo FADH2 do O2.
NAD+ a FAD Coenzýmy sú redukované v oxidačných trasách mastných kyselín a cyklus kyseliny citrónovej v dôsledku oxidácie rôznych substrátov. Následne sú tieto koenzýmy oxidované v elektronickom transportnom reťazci.
Takže elektronický transportný systém pozostáva zo sekvencie reakcií oxidu redukcie, ktoré sú navzájom spojené.
[TOC]
Reťazové komponenty
V závislosti od typu organizmu je možné pozorovať 3 až 6 komponentov, ktoré tvoria reťazec elektrónového dopravníka. Proces transportu elektrónov a syntéza ATP oxidačnou fosforyláciou sú procesy, ktoré sa vyskytujú v membráne.
V prípade prokaryotických buniek (aeróbne baktérie) sa tieto procesy vyskytujú spojené s plazmatickou membránou. V bunkách Eukaryot sa vyskytuje v mitochondriálnej membráne, takže komponenty transportu elektrónov sa nachádzajú vo vnútornej časti membrány.
https: // giphy.com/gifs/htksbbedquk9z7co5e
Elektróny sa postupne prenášajú prostredníctvom štyroch komplexov, ktoré tvoria elektronický transportný reťazec.
Každý komplex má niekoľko proteínových zložiek spojených s protetickými skupinami (ne -aminokyselinové zložky konjugátových proteínov) redox, ktoré umožňujú zvýšenie ich redukcie potenciálov.
Okrem toho je tento transportný systém tvorený rôznymi molekulárnymi druhmi, ako je flavoproteín; koenzým, ktorý sa tiež nazýva ubichinona (COQ alebo UQ); rôzne cytochrómy, ako je cytochróm B, C, C1, A a A3; Proteíny s skupinami Fe-S a proteínmi spojenými s Cu. Tieto molekuly sú spojené s membránou, s výnimkou cytochrómu C.
Komplex i
https: // giphy.com/gifs/rlf1rl9gdc6356sj6w
Komplex i nazývaný NADH Coenzým chinona oxidortraduáza alebo NADH dehydrogenáza, pozostáva z približne 45 polypeptidových reťazcov a obsahuje mononukleotidovú molekulu flavínu (FMN) a osem až deviati. Ako už názov napovedá, tento komplex prenáša pár elektrónov z NADH Coenzým do COQ.
Funkcia komplexu NADH dehydrogenázy začína zväzom NADH do uvedeného komplexu na strane vnútornej mitochondriálnej membránovej matrice. Elektróny sa potom prepravujú z NADH do FMN. Následne elektróny prechádzajú zo zníženého flavínu (FMNH2) na proteíny FE-S.
FMNH2 funguje ako druh mostu medzi NADH a proteínmi FE-S, pretože tento môže prenášať iba jeden elektrón, zatiaľ čo NADH Coenzým prenáša dva, takže flavinas urobí tento prenos jedného elektrónu vďaka svojmu redoxu semi -cynonu.
Môže vám slúžiť: Monocytopoiesis: Fázy, charakteristiky, reguláciaNakoniec sa elektróny prenášajú zo zoskupení FE-S do koenzýmu q, čo je mobilný elektrónový dopravník s izopreneidným chvostom, vďaka ktorému je hydrofóbny, čo umožňuje prekročiť stred mitochondriálnej membrány.
Komplex II

Komplex II, známy ako sukcinát dehydrogenáza, je integrálny proteín mitochondriálnej vnútornej membrány a je enzým, ktorý zasahuje do cyklu kyseliny citrónovej.
Tento komplex pozostáva z dvoch hydrofilných podjednotiek a dvoch hydrofóbnych skupín s HEMO B, ktoré poskytujú väzbové miesto COQ, okrem flavoproteínu a proteínu s FE-S.
V cykle kyseliny citrónovej (Krebs alebo cyklus kyseliny trikarboxylovej) sa sukcinát konvertuje na fumarát sukcinátom dehydrogenázy, čím sa koenzýmový výstrelok znižuje na FADH2. Z tohto posledného koenzýmu sa elektróny prenášajú do centier FE-S, ktoré ich zase prenášajú do Coq.
Počas reakcií tohto prenosu elektrónov je štandardný redoxný potenciál veľmi nízky, čo bráni uvoľňovaniu potrebnej voľnej energie na syntézu ATP.
To znamená, že komplex II je jediným komplexom v elektrónovom transportnom reťazci, ktorý nie je schopný poskytnúť energiu pre syntézu ATP. Tento komplex je však v tomto procese kľúčom, pretože prenáša elektróny z FADH2 do zvyšku reťazca.
Komplex III
https: // giphy.com/gifs/cjg0raiuizjds2hkyuu
Komplex III, cytochrómový komplex BC1 alebo Coq Cytochróm C reduktáza, prenáša elektróny zo zníženého koenzýmu na cytochróm C. Tento prenos sa vyskytuje jedinou redoxnou cestou, ktorá je známa ako q cyklus.
Tento komplex pozostáva z proteínu s Fe-S a tromi rôznymi cytochrómmi, v ktorom sa atóm železa nachádza v skupine Hemo Cyklicky medzi zníženými stavmi (Fe2+) a oxidovanými (Fe3+).
Cytochrómy sú hemoproteíny elektronického transportu, ktoré majú redoxnú aktivitu. Sú prítomné vo všetkých organizmoch, s výnimkou niektorých povinných anaeróbov.
Tieto proteíny majú hemo skupiny, ktoré sa striedajú medzi dvoma oxidačnými stavmi (Fe2+ a Fe3+). Cytochróm C je mobilný elektrónový transportér slabo spojený s vnútornou membránou mitochondrií.
Cytochrómy nachádzajúce sa v tomto komplexe sú cytochrómy B, C a A, 3 sú aktívne redoxné proteíny so skupinami, ktoré máme rôzne charakteristiky, ktoré striedajú ich oxidačné stavy medzi Fe2+ a Fe3+.
Cytochróm C je proteín periférnej membrány, ktorý funguje ako „raketoplán“ elektrónu s cytochrómom C1 a s IV komplexom.
IV komplex
Cytochróm C a O2 sú konečné receptory elektrónov odvodených z oxidácie organického materiálu, takže komplex oxidázy Cytochrómu C je terminálny enzým v elektronickom transportnom procese. To akceptuje elektróny z cytochrómu C a prenáša ich na redukciu O2.
Komplexnou funkciou je katalyzovať oxidácie elektrónu štyroch po sebe idúcich molekúl redukovaného cytochrómu C, to znamená, že súčasne redukuje štyri elektróny molekuly O2, čo nakoniec produkuje dve molekuly H2O H2O.
Môže vám slúžiť: tkanivo epitelového povlakuSekvencia prenosu elektrónov
Elektróny sa prenášajú z komplexov I a II do komplexu III vďaka koenzýmu Q a odtiaľ prechádzajú do IV komplexu prostredníctvom cytochrómu C. Keď elektróny prechádzajú týmito štyrmi komplexmi, zvyšuje sa redukčný potenciál a uvoľňuje energiu, ktorá sa potom používa na syntézu ATP.
Celkovo prenos niekoľkých elektrónov spôsobuje translokáciu 10 protónov cez membránu; Štyri v komplexoch I a IV a dva z komplexu III.
NADH descidrogenasa
Tento enzým katalyzuje oxidáciu NADH koenzýmu koenzýmom, ktorý. Elektróny sa presúvajú z NADH do FMN, ktorý je pripevnený k hydrofilnému chvostu komplexu I. Zoskupenia FE-S sa prenášajú na elektróny naraz. Tieto skupiny FE-S sa znižujú na COQ, ktoré je vložené do membrány, na ubichinol (znížené COQ).
Počas prenosu elektrónov do COQ sa štyri protóny zase prenášajú vnútornou membránou do intermembranálneho priestoru. Mechanizmus, pomocou ktorého sú tieto protóny translokované, zahŕňa proteín umiestnený v hydrofóbnom chvoste komplexu I.
Proces prenosu elektrónov v tomto kroku uvoľňuje voľnú energiu, konkrétne -16,6 kcal/mol.
Coq-citokromo c reduktáza a q cyklus
Koenzým, ktorý je oxidovaný cytochrómom C, v reakcii katalyzovanej týmto koenzýmom. Oxidácia ubichinolu (znížená COQ) sa vyskytuje v určitom mieste komplexu (QO alebo oxidačné miesto) v mitochondriálnej membráne, prenáša dva elektróny, jeden do proteínu so skupinami FE-S a druhý do skupín Hemo skupiny a druhý do skupín Hemo.
V q cykle oxidácia COQ produkuje semi -liquinón, kde sa elektróny prenášajú do skupín HEMO B1 a BH. Aj keď sa vyskytuje tento prenos elektrónov, v lokalite QO oxiduje druhý COQ, opakuje sa cyklus.
Tento cyklus spôsobuje prenos dvoch elektrónov a zase translokáciu štyroch protónov do intermembranálneho priestoru s uvoľňovaním -10,64 kcal/mol voľnej energie.
Oxidáza citocroma c
Tento enzým (komplex IV) katalyzuje oxidáciu cytochrómu C (redukovaný) O2, čo je konečný akceptor elektrónov. Tento prenos vytvára molekulu H2O pre každý pár prenesených elektrónov okrem translokácie protónov cez membránu.
Elektróny sa presúvajú z jedného na jeden, z redukovaného cytochrómu C na pár CuA iónov, potom prechádzajú do skupiny Hemo A a nakoniec dosiahnu binukleárne centrum komplexu, ktorý obsahuje ióny Cub a Hemmo A3, kde prenos štyroch prenosu štyroch Elektróny sa vyskytujú kyslíkom.
V komplexe IV sa prvky prenášajú elektróny jedného po druhom, takže O2 sa postupne znižuje, takže uvoľňovanie niektorých toxických zlúčenín, ako je superoxid, peroxid vodíka alebo hydroxyl radikály, sa nevyskytuje.
Energia uvoľnená v tejto fáze zodpovedá -32 kcal/mol. Elektrochemický gradient generovaný počas procesu prenosu a energetické zmeny (AE) spôsobené niekoľkými elektrónmi pri prechádzaní štyrmi komplexmi zodpovedá v každej fáze voľnej energii potrebnej na výrobu molekuly ATP.
Môže vám slúžiť: teória skladania membrányVeľká dehydrogenáza
Ako už bolo spomenuté, tento komplex má jedinú, ale dôležitú funkciu zavedenia elektrónov FADH2 z cyklu kyseliny citrónovej do elektrónového transportného reťazca.
Tento enzým katalyzuje oxidáciu koenzýmu FADH2 koenzýmom Q (oxidovaný). V cykle kyseliny citrónovej pri sukcináte fumarátu sa na výstrelok prenesú dva elektróny a dva protóny. Následne FADH2 prenáša tieto elektróny, kým nie sú v centrách FE-S komplex.
Nakoniec sa z COQ elektróny prenášajú do komplexu III podľa krokov opísaných vyššie.
Reťazové komplexy sú nezávislé
Štyri komplexy, ktoré tvoria elektronický transportný reťazec, sú nezávislé, to znamená, že sú nezávisle a pôsobia v mitochcondriálnej vnútornej membráne a pohyb každej z nich v membráne nezávisí alebo je spojený s ostatnými komplexmi.
Komplexy I a II sa pohybujú v membráne prenosom svojich elektrónov na COQ, ktoré sa tiež šíria v membráne a prenáša ich do komplexu III, odkiaľ elektróny prechádzajú do cytochrómu C, ktorý je tiež mobilný v membráne a usadzuje elektróny v komplexe IV komplexu.
Inhibítory elektronického transportného reťazca
V elektronickom transportnom reťazci niektoré špecifické inhibítory pôsobia vo svojom procese. Rothenone je bežne používaný insekticíd, ktorý je stechiometricky spojený s komplexom I, čím sa vyhýba zníženiu COQ.
Niektoré lieky typu barbituráty, ako je piericídín a amytal, inhibujú komplex I, interferujúce s prenosom elektrónov zo skupín FE-S do Coq.
V komplexe II niektoré zlúčeniny, ako je Theoiltrifluoroacetón a malonát, pôsobia ako konkurencieschopné inhibítory sukcinátom, vyhýbajú sa ich oxidácii a zase prenos elektrónov na výstrelok.
Niektoré antibiotiká, ako je myxotiazol a stigmatelín, sa viažu na q miesto COQ, čo inhibujú prenos elektrónov z koenzýmu Q do centier FE-S proteínov.
Kyanid, azida (N3-), kyselina sírová a oxid uhoľnatý inhibujú IV komplex. Tieto zlúčeniny sa viažu na skupiny hemmo a vyhýbajú sa prenosu elektrónov do komplexného alebo kyslíka (O2) binukleárneho centra (O2).
Ak je inhibovaný elektrónový dopravný reťazec, výroba energie sa zastaví v dôsledku oxidačnej fosforylácie, čo spôsobuje vážne škody a dokonca aj smrť organizmu.
Odkazy
- Alberts, b., Bray, D., Hopkin, k., Johnson, a., Lewis, J., Raff, m., Roberts, K. & Walter, P. (2004). Základná bunková biológia. New York: Garland Science. 2. vydanie.
- Cooper, G. M., Hausman, r. A. & Wright, n. (2010). Bunka. (PP. 397-402). Edimatizovať. Marbán.
- Devlin, T. M. (1992). Učebnica biochémie: s klinickými koreláciami. John Wiley & Sons, Inc.
- Garrett, R. H., & Grisham, C. M. (2008). Biochémia. Edimatizovať. Thomson Brooks/Cole.
- Rawn, J. D. (1989). Biochémia (nie. 577.1 surové). Edimatizovať. Medziamerický-mcgraw-hill
- Voet, D., & Voet, J. G. (2006). Biochémia. Edimatizovať. Pan -American Medical.
- « Vlastnosti elektrickej anguily, biotop, reprodukcia
- Charakteristiky biozoos, morfológia, reprodukcia, výživa »

